MONOGRAFIA / MONOGRAPHY
Cordia verbenacea DC Boraginaceae
Resumo
As partes aéreas de Cordia verbenacea são usadas tradicionalmente como um antiinflamatório. A base científica deste uso é descrita em termos de botânica, farmacognosia, farmacologia e toxicologia visando o desenvolvimento de um medicamento fitoterápico.
- Palavras chave:
- Cordia verbenacea, erva-baleeira.
- planta medicinal.
- farmacologia.
- -humuleno.
- trans-cariofileno..
Abstract
The green parts of Cordia verbenaceae are traditionally used as an antiinflammatory drug. The scientific basis for this use are described in terms of botany, pharmacognosy, pharmacology and toxicology with a view to the development of a phytotherapy drug.
- Keywords:
- Cordia verbenacea. erva-baleeira.
- medicinal plant.
- pharmacology.
- -humulene.
- trans-caryophyllene..
Definição da droga vegetal
Há três derivados da planta em uso medicinal: folhas, hastes e raízes. O óleo essencial das folhas é o preferido para produção industrial.
Sinonímia
Cordia salicina DC, Cordia curassavica Jacq. (veja abaixo), Cordia cylindristachya (Ruiz & Pav.) Roem.&Schult., Lithocardium fresenii Kuntze, Lithocardium salicinum Kuntze, Lithocardium verbenaceum Kuntze (Lorenzi e Matos, 2002).
Nomes comuns
Baleeira, erva-baleeira, camarinha, catinga-de-barão, cordia, erva-balieira, balieiracambará, erva-preta, maria-milagrosa, maria-preta, salicinia, catinga-preta, mariarezadeira, camaramoneira-do-brejo (Lorenzi e Matos, 2002).
Variedades e espécies correlatas
Cordiasuperba Cham., CordiarufescensA. DC, Cordia sellowiana Cham., Cordia myxa L. (Barroso et al., 2009; Costa et al., 2008). Cordia monosperma Jacq. tem sido utilizada em substituição a C. verbenacea, em doenças da bexiga e como antiinflamatória (Souza et al., 2004).

História
Os indígenas utilizavam o extrato bruto das partes aéreas da Cordia verbenacea em processos antiinflamatórios por aplicação tópica.
Em 1819 foi identificada a espécie Cordia curassavica, algumas classificações consideram esta planta como sinonímia a Cordia verbenacea, mas ainda existem controvérsias porque há diferenças morfológicas entre elas (Carvalho, 2010).
O gênero Cordia é mencionado por Pio Corrêa (1952) por ser produtor de substâncias empregadas como medicamentos e por inúmeras espécies apresentarem usos medicinais. Existem várias publicações científicas na área de ensaios farmacológicos e toxicológicos para Cordia verbenacea DC. (Basile et al., 1989; Rapisarda et al., 1997; Sertié et al. 1988, 1990 e 1991). O desenvolvimento industrial, a partir desta planta foi desenvolvido o antiinflamatório de uso tópico Acheflan® pelo Laboratório Ache que causou um impacto importante no cenário da indústria farmacêutica brasileira (Queiroz et al., 2009).
Distribuição geográfica
O gênero Cordia é distribuído nas regiões tropical e subtropical do mundo, ocorrendo na Austrália, Nova Caledônia, América Central, Guiana e no Brasil (Rapisarda et al., 1997).
A espécie Cordia verbenacea é nativa do Brasil, encontrando-se do Ceará ao Rio Grande do Sul, preferencialmente na faixa de 500 a 1000m do litoral sempre acompanhando as áreas abertas da orla do Atlântico, onde é considerada planta daninha.
Cultivo e propagação
Propagada usualmente por sementes, pode sofrer alterações no teor do princípio ativo em função da variação genética existente (Lameira, et al., 1997) e provavelmente por outros fatores.
Descrição da planta
Arbusto muito ramificado, ereto e aromático, com hastes cobertas por casca fibrosa e com altura de 1,5-2,5m. Folhas simples, alternas, coriáceas, aromáticas, de 5-9cm de comprimento. As flores são pequenas, brancas e dispostas em inflorescências racemosas de 1015cm de comprimento (Lorenzi e Matos, 2002). Os frutos quando maduros apresentam a coloração vermelha.
Ventrella e colaboradores (2008) desenvolveram um estudo morfológico e histoquímico dos tricomas glandulares das folhas de Cordia verbenacea, reconhecendo duas classes, globular e reniforme. Os tricomas globulares caracterizam-se pela secreção de um óleo essencial terpenóide, enquanto que nos reniformes ela contém principalmente compostos fenólicos, como os flavonóides.
Material vegetal usado
Folhas
Souza et al. (2009), trabalhando com material de Montes Claros - MG, mostraram que o melhor horário para coleta das folhas para extrair o óleo essencial da planta é das 09 às 12 h e por volta das 18:00 h, pois nesses horários obteve-se maior produção.
Componentes químicos principais
Nas análises fitoquímicas foram identificados monoterpenos, sesquiterpenos, triterpenos, flavonóides e ácidos graxos.
írans-cariofileno
Uma análise das folhas frescas de C. verbenacea mostrou a presença de 0,23% (v/w) de óleo essencial, apresentando como maiores constituintes o α-pineno (29,7%), transcariofileno (25%), alo-aromadendreno (10%) e α-humuleno (4,6%). Também foram observados β-felandreno, citronelol acetato, β-elemeno, β-gurjuneno, biciclogermacreno, δ-cadineno, espatulenol e epoxicariofileno (Carvalho Jr. et al., 2004). Em outro trabalho Santos et al. (2006) encontraram no óleo essencial das folhas: monoterpenos (47,3%) e sesquiterpenos (43,9%), entre os quais α-pineno (20,5%), β-pineno (13,1%), (-)-trans-cariofileno (12,4%) e biciclogermacreno (13,8%) como compostos predominantes.
O α-humuleno é um importante constituinte do óleo da Cordia verbenacea e foi designado como principal marcador químico do mesmo. Vaz et al. (2006) avaliaram o teor mínimo 2,3% de α-humuleno encontrado em Cordia verbenacea, planta fresca, em quatro municípios paulistas. Além do trans-cariofileno foram identificados triterpenos do grupo damarano como a cordialina AeB(Veldeetal. 1982).
Flavonóides
Artemetina foi identificada por Sertié et al. (1990) e por Bayeux et al. (2002) em Cordia verbenacea. Também há outros flavonóides presentes descritos por (Ameira et al. 2009).
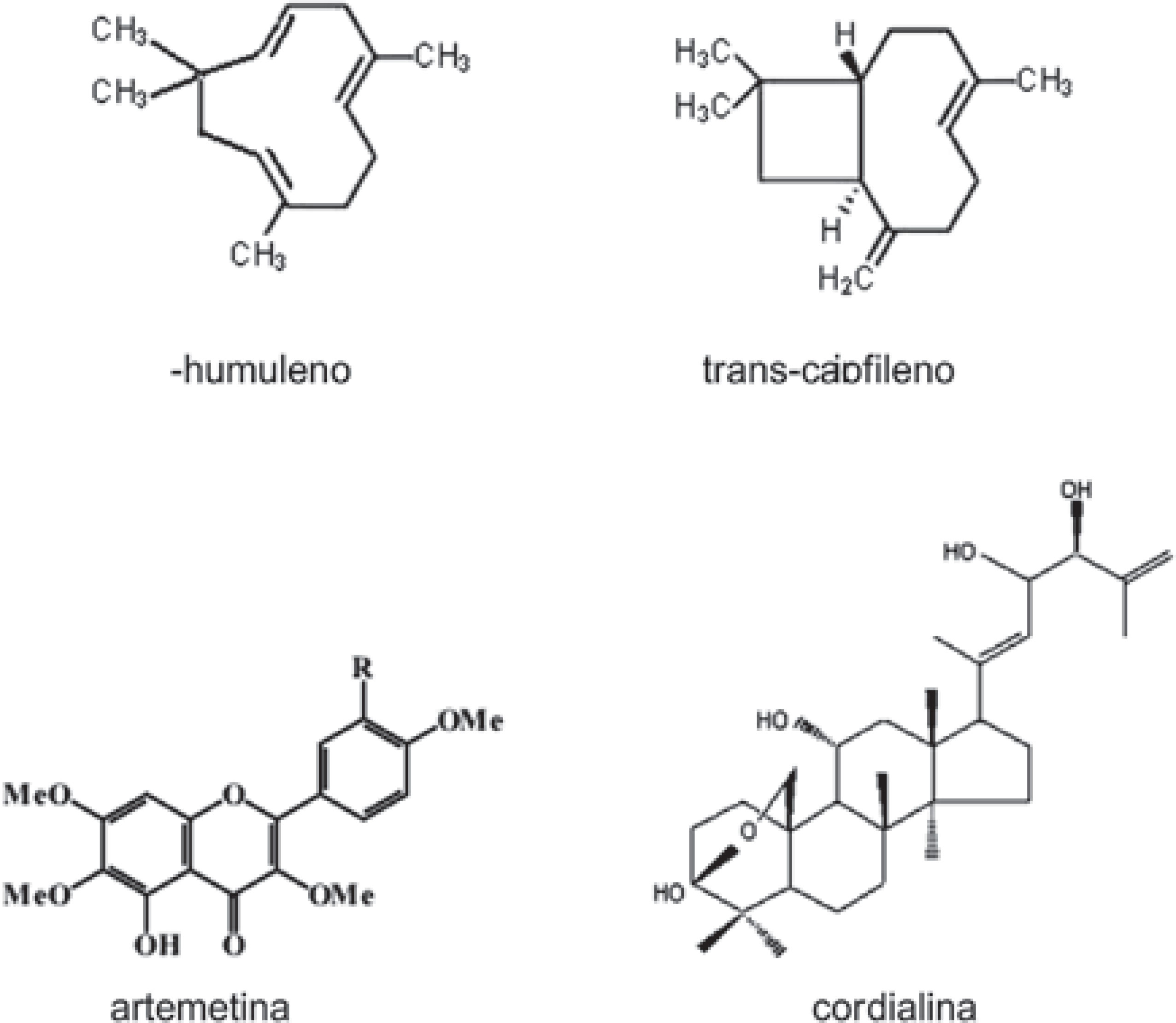
Ácidos e ésteres
O ácido rosmarínico foi encontrado no extrato hidroalcoólico das folhas da espécie descrita (Hage-Melim, 2009). O ácido caféico e ácidos graxos são encontrados no óleo das sementes (Seigler et al., 1970). Dos ácidos graxos 43% são de C-20, incomum entre tais óleos (Miller et al., 1968). O mesmo óleo contém o ácido gama-linolênico, com valores de 0,63 a 2,54% (Arrebola et al., 2004).
Notável também neste óleo é a presença de um lipídeo cianogenético, que é um diéster graxo de hidroximetilacrolein-cianidrina em que as duas hidroxilas são esterificadas com ácidos graxos predominantemente C-20 (Seigler et al., 1970).
Usos medicinais
Usos apoiados em dados clínicos
Conhecida como erva-baleeira, esta espécie é utilizada na medicina tradicional como antiinflamatório, analgésico e antiúlcera (Ventrella et al., 2008).
Usos descritos em farmacopéias e sistemas tradicionais de medicina que têm apoio experimental
A Cordia verbenacea é administrada internamente na forma de chá para artrite, reumatismo e problemas de coluna (Silva Jr. et al., 1995). Lorenzi e Matos (2002) descrevem seu emprego em doenças osteoarticulares (artrite, gota, dores musculares e da coluna).
O Formulário Nacional Fitoterápico da Farmacopéia Brasileira (ANVISA, 2011) descreve o uso tópico das folhas de Cordia verbenacea como antiinflamatório em forma de infuso, como compressa ou em forma de pomada.
Usos descritos na medicina popular não apoiados em evidência experimental ou clínica
Diversos autores citam o uso tradicional em prostatites, nevralgias e contusões, como tônico e cicatrizante, inclusive em ferimentos provocados por peixes, talvez esta a origem do nome comum; o chá de suas folhas é empregado na cicatrizaçâo de feridas externas e úlceras (Lorenzi e Matos, 2002; Panizza, 1998; Ventrella et al., 2008). Akisue et al., (1983) mencionam o chá das folhas como hemostático e no tratamento de tumores.
Atividade antiinflamatória
Duas maneiras de administração são descritas - tópica e oral.
Foram investigados o efeito antiinflamatório e toxicidade dos extratos em vários modelos experimentais em ratos Wistar. No modelo do edema induzido por carregenina foi administrado por via oral o extrato hidroalcoólico a 70% das folhas de Cordia verbenacea nas dosagens de 0,59 a 2,98 mg/kg, o qual inibiu significamente o edema. Em ensaios sobre o granuloma induzido por chamuscos de algodão onde foram utilizadas as dosagens diárias de 1,24mg/kg do extrato liofilizado a partir do primeiro dia de implantação até o sexto dia. O extrato inibiu a formação de granulomas nos animais tratados. Em testes de medição de aumento da permeabilidade vascular osanimais receberam o extrato (1,24mg/kg) na dose de 0,5ml (25mg/ kg), tendo como resultado redução da permeabilidade vascular e resposta para histamina. Foi observada baixa toxicidade do extrato (Sertié et al., 1988).
Na suposição que o principal componente antiinflamatório das folhas de C. verbenacea fosse o flavonóide artemetina Sertié e colaboradores (1990) avaliaram o efeito antiinflamatório e a toxicidade subaguda da artemetina. No ensaio do edema induzido por carragenina em ratos Wistar foram administradas as doses de 30,4; 45,6; 68,4; 102,6 e 153,9mg/kg-1 de artemetina, via oral, onde os níveis de dosagem maiores inibiram o edema num grau comparável com o controle (fenilbutazona de cálcio a 50mg/kg). Um efeito semelhante foi observado no ensaio do granuloma induzido por chamuscos de algodão a uma dose diária de artemetina de 67,07mg/kg-1. Os resultados dos experimentos com artemetina na dose de 153,9mg.kg-1 e DL50 67,07mg/kg-1 não demonstraram sinais farmacotóxicos.
Sertié e equipe (1991) avaliaram a inibição da inflamação pelo extrato etanólico a 70% das folhas de C. verbenacea em ratos. Em ensaio de edema induzido por nistatina nas patas os animais receberam a dose de 1,24mg/kg do extrato por via oral. Os resultados apontaram uma significante redução em relação ao grupo controle. A ausência de inflamação gástrica distingue o extrato da maioria dos antiinflamatórios sintéticos em uso. Passando à administração tópica foi examinado o efeito do extrato sobre edema induzido por óleo de croton em orelha de camundongos. O efeito de 0,09mg/orelha superou aquele do controle naproxeno um inibidor de ciclooxigenase. Outras observações da inibição de edema de pata com o extrato hidroalcoólico em ratos, tanto oral e tópico, confirmaram estes resultados (Sertié et al., 2005).
Resultados de alta discrepância são registrados por Bayeux et al. (2002) que avaliaram a atividade antiedematogênica do extrato bruto da parte aérea de C. curassavica, espécie que os autores afirmam ser sinonímia de C. verbenacea, e de uma fração enriquecida de artemetina. No modelo de edema de pata induzido por carragenina em camundongos o extrato diclorometânico nas doses de 300 a 1000mg/kg, via oral, mostrou atividade antiedematogênica reduzindo os edemas 42, 57 e 45%, enquanto a fração enriquecida por artemetina não mostrou atividade. Assim a presença de um outro componente com atividade antiinflamatória na planta ficou evidenciada.
Além da artemetina, ativa segundo as observações do grupo de Sertié, Ticli et al. (2005) demonstraram a ação antiinflamatória do fenilpropanóide e do ácido rosmarínico, e os pesquisadores do grupo de Calixto mostrou a importância do óleo essencial e especialmente o trans-cariofileno e humuleno. Trabalhos subseqüentes concentraram atenção nestes sesquiterpenos (Fernandes et al. 2007; Medeiros et al, 2007; Passos et al. 2007).
Passos e colaboradores (2007) avaliaram a atividade antiinflamatória e as propriedades antialérgicas do óleo essencial das folhas e de alguns constituintes ativos presentes no óleo. O tratamento sistêmico com o óleo essencial (300-600mg/kg, via oral em ratos e camundongos) reduziu o edema de pata e outros efeitos associados com a inflamação induzida por carragenina e, em camundongos inibiu a atividade de mieloperoxidase, bradiquinina, substância P - um neuropeptídeo associado com estresse psicológico, a histamina e o fator de ativação de plaquetas. Estudos com os componentes sesquiterpênicos, α-humuleno e trans-cariofileno (50mg/kg, via oral) demonstraram que, na inflamação induzida na pata por carragenina, o α-humuleno ocasionava uma redução da produção do fator de necrose de tumor TNFa, da interleucina IL1β, da prostaglandina PGE2, do óxido nítrico sintase iNOS, da ciclooxigenase COX-2. Otranscariofileno também exercia efeitos semelhantes embora não inibisse interleucina IL-1p, e os dois sesquiterpenos se equivaleram a dexametasona usada como controle (Fernandes et al., 2007). Os sesquiterpenos não inibiam a migração de neutrófilos para a cavidade pleural, induzido por ovalbumina, um efeito positivo com a dexametasona.
Extendendo os estudos destes dois sesquiterpenos na inflamação induzida por lipopolissacarídeo - LPS em pata do rato, foram observados a redução da migração de neutrófilos e da ativação de NFkB. Entretanto somente -humuleno reduzia as citocinas pro-inflamatórias TNF e IL-1 β, o edema na pata e o aumento da expressão de receptores B1 induzidos por LPS e nenhum dos dois interferiram com as quinases das classes proteína mitógeno ativada - MAP, extracelular ativada - ERK, p38, e cJun Nterminal - JNK (Medeiros et al., 2007).
Continuando o estudo dos sesquiterpenos, Rogério et al. (2009) avaliaram a atividade antiinflamatória em alergias respiratórias e o efeito de mediador da via de redução da inflamação. Nos experimentos foram utilizados camundongos BALB-C, os quais receberam doses diárias de α-humuleno e trans-cariofileno na dosagem de 50mg.kg-1 (de cada dos terpenos), via oral ou α-humuleno (Img.ml-1 via aerosol) como dose preventiva por 22 dias. O α-humuleno se revelou como o produto eficaz neste modelo de alergia respiratória murina exibindo uma ação antiinflamatória marcada, nas vias respiratórias e reduzindo o recrutamento de eosinófilos. Observou-se a redução de mediadores da inflamação, da expressão de moléculas de adesão e da ativação de fatores de transcrição [INFγ-, IL-5, CCL11, (LT)B4 e NF-κB].
Atividade antiúlcerogênica
Sertié et al. (1991) mostraram que o extrato etanólico 70% das folhas de Cordia verbenacea, liofilizado ao nível de 1,24mg/kg via oral em ratos, possuía um importante efeito de proteção à mucosa gástrica, reduzindo em 34% o número de lesões gástricas produzidas por estresse. Roldão e colaboradores (2008) mostraram que o extrato também protegia o estômago de camundongos contra lesões induzidas por etanol e etanol-ácido clorídrico. O grau de proteção alcançado era o dobro do registrado por Sertié e equipe quando as doses utilizadas foram de 200 a 800 vezes maiores (250 a 1000mg/kg). Os autores atribuem o efeito como possivelmente associado à ação antioxidante do extrato.
Atividade analgésica
Em ensaio com o objetivo de avaliar a atividade analgésica do extrato etanólico a 70% das folhas de C. verbenacea, liofilizado, ratos foram tratados com a dosagem de 1,24 ou 2,48mg/kg (peso corpo, via oral). Um discreto efeito analgésico foi observado com a dose de a 2,48mg/kg (Sertié et al., 2005). Roldão et al. (2008) não acharam efeitos analgésicos significantes em camundongos na dosagem de 250mg/kg via oral nos modelos de placa quente (56oC), ácido acético (0,6% a 10mg/kg i.p.) e teste de retirada da cauda de água a 51°C.
Atividade antiofídica
Seguindo um uso tradicional de C. verbenacea contra veneno de cobra, foi examinado o efeito do extrato hidroalcoólico da folhas contra o veneno de jararacussu, Bothrops jararacussu. O extrato inibiu a ação hemorrágica do veneno bruto. O ácido rosmarínico, isolado do extrato metanólico das folhas também inibiu a hemorragia como também a citotoxicidade e a miotoxicidade do componente fosfolipásico do veneno BthTX-I, e em menor grau da outra fosfolipase BthTX-II, mas não teve ação sobre o efeito edematogênica destas fosfolipases. Simulações da interação de ácido rosmarínico com as fosfolipases mostraram o encaixe da molécula do ácido nelas (Hage-Melim, 2009; Ticli et al. 2005).
Atividade antimicrobiana
Carvalho Jr. e equipe (2004) avaliaram a atividade antimicrobiana do óleo essencial das partes aéreas e folhas da espécie Cordia verbenacea frente a bactérias Gram-positivas e Gram-negativas pelo método de difusão em ágar. Foram observadas atividades positivas contra bactérias Gram-positivas (duas espécies de Staphylococcus, uma delas S. aureus -ATCC 5051; duas de Bacillus) e contra fungos (oito espécies de Candida, uma delas C. albicans, várias cepas, e uma de Cryptococcus), mas contra apenas um gênero de Gram-negativas (Protium mirabilis e P. vulgaris), enquanto os demais gram-negativos (duas espécies de Enterobacter, Escherichia coli, Klebisiella pneumoniae, Pseudomonas aeruginosa, e duas espécies de Salmonella) foram resistentes.
Atividade esquistossomicida
A atividade de uma fração etanólica de C. verbenacea (parte não especificada da planta) contra Schistosoma mansoni foi avaliada in vitro (vermes acasalados em meio de cultura) e in vivo (camundongos). Os resultados indicam atividade sobre os vermes adultos in vitro e possivelmente alguma ação in vivo (Frezza et al., 2010).
Farmacocinética
Visto que a atividade antiinflamatória de C. verbenacea foi associada principalmente com α-humuleno, Chaves et al. (2008) realizaram um estudo quantitativo avaliando a velocidade de absorção e excreção após administração oral, endovenosa e tópica. A absorção do humuleno é rápida alcançando a concentração máxima no plasma após 15min por via oral (150mg/ kg) e após 30min quando administrado como óleo essencial total da planta (1g/kg oral). O acúmulo nos órgãos como o fígado foi observado e demonstrou-se que ultrapassa a barreira sangue-cérebro. A aplicação tópica de fórmulas como o creme ou o spray também resultou em rápida absorção. Após 4h a redução da concentração de humuleno é significante sendo em grande parte oxidado a vários epóxidos pelos citocromos. A biodisponibilidade porvia oral é de 18%.
Toxicologia
In vivo
Na série de trabalhos sobre a farmacologia de Cordia verbenacea em animais de laboratório não foram observadas níveis significantes de toxicidade aguda nos extratos ou nas substâncias isoladas nem porvia oral nem tópica (Sertié et al., 1988, 1990, 1991 e 2005; Bayeux et al., 2002; Basile et al., 1989; Carvalho et al., 2004; Oliveira et al., 1998; Passos et al., 2007; Roldão et al., 2008). Sertié et al. (2005) mostraram que o extrato hidroalcoólico liofilizado administrado por via oral a ratos fêmeas ou machos antes do acasalamento ou nas fêmeas durante gravidez não afetou o ciclo das fêmeas nem o desenvolvimento normal dos fetos, nem a estrutura óssea, maturação sexual ou fertilidade deles.
Nos estudos de fase I (Calixto e Vergnanini 20002001) foram comprovadas que as concentrações de 0,5% até 2,5% do óleo essencial de folhas de Cordia verbenacea por aplicação tópica são seguras e não apresentaram qualquer reação alérgica ou irritativa nos voluntários sadios que participaram do estudo.
Ensaios Clínicos
Em estudos clínicos de fase I realizados por (Calixto et al. 2000 e 2001), fase II e fase III (Refsio et al., 2005) que demonstraram ação antiinflamatória e excelente tolerabilidade da Cordia verbenacea na forma de creme contendo 0,5% de óleo essencial padronizado em 2,3-2,9% de α-humuleno, conforme citação na Enciclopédia Médica descrita nas referências bibliográficas.
Nos estudos de fase II para avaliar o uso da Cordia verbenacea de aplicação tópica no tratamento da dor miofascial e da tendinite crônica, realizado com 81 pacientes, observou-se que mais de 60% dos casos tratados com Cordia apresentaram eficácia considerada ótima ou muito boa, enquanto o mesmo foi observado em apenas 40% dos casos tratados com diclofenaco dietilamônio (emulgel). Já nos estudos de fase III com 268 pacientes, os resultados indicaram que o creme de Cordia verbenacea foi eficaz no tratamento de tendinite e dor miofascial quando aplicado no local da lesão a cada 8 horas. A avaliação comparativa do creme de Cordia verbenacea 0,5% com diclofenaco dietilamônio 1%, sob forma de emulgel, demonstrou que Cordia apresentava eficácia semelhante ao do diclofenaco para os casos de tendinite crônica, dor miofascial e mesmo quando consideradas as afecções associadas (Refsio et al., 2005).
Em estudo clínico fase III, aleatório, duplo-cego e comparativo, com os mesmos produtos nas mesmas condições (aplicação tópica de 8/8 horas durante dez dias, em pacientes portadores de contusões e lesões traumáticas). Os pacientes foram divididos em 2 grupos de 55 e 59 pacientes recebendo respectivamente o creme de Cordia e diclofenaco-dietilamôneo (emulgel). A eficácia do tratamento com o creme de Cordia verbenacea (0,5%) em traumas foi demonstrada, pois 72,7% dos pacientes apresentaram uma melhora acentuada após os 10 dias de tratamento e 18,2% tiveram melhora moderada, apenas 7,3% tiveram melhora discreta e, em apenas 1,8% dos casos o medicamento foi ineficaz, pois o quadro permaneceu inalterado. O tratamento com o diclofenaco dietilamônio (emulgel 1%), também demonstrou a eficácia do mesmo, porém, em menor proporção quando comparado a Cordia verbenacea (0,5%), sendo que 62,7% dos casos a melhora foi acentuada, 18,6% a melhora foi moderada, 10,2% o quadro clínico apresentou uma discreta melhora e em 8,5% o quadro permaneceu inalterado. O estudo detectou apenas um caso de evento adverso (prurido no local de aplicação), possivelmente relacionado ao medicamento. Ambos os tratamentos apresentaram excelente segurança, não havendo diferença estatística significante de tolerabilidade entre os dois medicamentos (Brandão et al, 2006).
Efeitos adversos
Em geral não foram encontrados relatos de efeitos adversos com exceção do caso isolado acima citado.
Precauções
Gerais
O tratamento deve ser suspenso em caso de alergia (ANVISA, 2011).
Genotoxicidade
Não foram encontrados relatos de efeitos adversos.
Carcinogenese, mutagenese
Não foram encontrados relatos de efeitos.
Efeitos sobre a fertilidade
Conforme relatado acima, o extrato etanólico a 70%, administrado por 45 dias consecutivos, via oral, em dosagem de até 7,44mg/kg não apresentou qualquer sinal de toxicidade para o feto (Sertié et al., 2005).
Formas de dosagem e Posologia
Entre aplicações para o alívio de reumatismo, artrite reumatóide, gota, dores musculares e da coluna, prostatites, nevralgias e contusões, as seguintes formas de apresentação são recomendadas:
Infusão: o Formulário (ANVISA, 2011) recomenda preparar a infusão com 3g de folhas secas em 150mL de água fervente. Panizza (1998) indica a utilização das folhas frescas ou secas à sombra e recomenda uma xícara de chá 1-3 vezes ao dia.
Tintura: para aplicação tópica Panizza (1998) recomenda 3 colheres de folhas em uma xícara de álcool por 5 dias em maceração. Depois de coada a tintura é aplicada de 4 em 4 horas no local afetado. O uso interno da tintura é indicada para uso em adultos na dose de 10ml, 3 vezes ao dia, diluída em 1/2 copo d’água e para as crianças 5 ml, 3 vezes ao dia, diluído em 1/2 copo d’água (Panizza, 1998; Secretaria Municipal de Saúde, Memento terapêutico, RJ, 2002).
Em compressas pode também ser usada empregando folhas previamente aquecidas por exposição a vapor d’água em um pano e aplicada durante a noite (Panizza, 1998).
O Formulário (ANVISA, 2011) descreve uma pomada feita com 10mL da tintura feita com álcool a 70% e 100g de base de lanolina e vaselina. Baseado em dados clínicos acima esta pomada teria que ter um teor de humuleno entre 2,3 e 2,9%.
Referências bibliográficas
Akisue, M.K.; Oliveira, F.; Moraes, M.S.; Akisue, G.; Mancini, B. 1983. Caracterização farmacognóstica da droga e da tintura de Cordia verbenaceae Al. DC Boraginaceae. Revista de Ciências Farmacêuticas, v. 5, p. 69-82.
Ameira, O.A.; Pinto, J.E.B.P.; Cardoso, M.G.; Arrigoni-Blank, M.F. 2009. Estabelecimento de cultura de células em suspensão e identificação de flavonóides em Cordia verbenacea DC. Revista Brasileira Plantas Medicinais, Botucatu, v. 11(1), p. 7-11.
ANVISA. 2011. Formulário de Fitoterápicos, Farmacopéia Brasileira, 1a. Ed., p. 28 e 110, Brasília - DF.
Arrebola, M.R.B.; Peterlin, M.F.; Bastos, D.H.M.; Rodrigues, R.F.de O.; Carvalho, P.de O. 2004. Estudo dos componentes lipídicos das sementes de três espécies do gênero Cordia (Boraginaceae). Revista Brasileira de Farmacognosia, v. 14(1), p. 57-65.
Basile, A.C.; Sertie, J.A.A.; Oshiro, T; Caly, K.D.V.; Panizza, S. 1989. Topical anti-inflammatory activity and toxicity of Cordia verbenacea. Fitoterapia, v. 60, p. 260-263.
Bayeux, M.C.; Fernandes, A.T.; Foflio, M.A. eCarvalho, J.E. 2002. Evaluation of the antiedematogenic activity of artemetin isolated from Cordia curassavica DC. Brazilian Journal of Medical and Biological Research, v. 35, p. 1229-1232.
Barroso, I. C. E.; Oliveira, F. 2009. Caracterização farmacognóstica dos frutos de Cordia sellowiana Cham. e de Cordia myxa L. (Boraginaceae Jussieu). Revista Brasileira de Farmacognosia, v. 19(2A), p. 458-470.
Brandão, D.C.; Brandão, G.C.; Miranda, J.B.; Faria, P.A.; Jesus-Garcia, R. 2006. Estudo fase III, duplocego, aleatório, comparativo para avaliar a eficácia e tolerabilidade da Cordia verbenacea e do diclofenaco dietilamônio, em pacientes portadores de contusões, entorses, traumas e lesões musculares, com início inferior a 24h. Revista Brasileira de Medicina, v. 63(8), p. 408-415.
Calixto J.B.; Vergnanini, A. 2000 - 2001. Estudos pré-clínicos em roedores e cães e clínicos de fase I - Arquivo Central do Laboratório Aché.
Carvalho Jr., P.M.; Rodrigues, R.F.O.; Sawaya, A.C.H.F.; Marques, M.O.M & Shimizu, M.T. 2004. Chemical composition and antimicrobial activity of the essential oil of Cordia verbenacea DC. Journal of Ethnopharmacology, v. 95, p. 297-301.
Carvalho, S.S. 2010. Análise fotoacústica da cinética de penetração do fármaco Cordia verbenacea DC. (Acheflan) na pele humana (massagem versus fonoforese). Dissertação de Mestrado, Programa de Pós-Graduação em Bioengenharia do Instituto de Pesquisa e Desenvolvimento da Universidade Vale do Paraíba.
Chaves, J.S.; Leal, P.C.; Pianowisky, L.; Calixto, J.B. 2008. Pharmacokinetics and Tissue Distribution of the Sesquiterpene α-humulene in mice. Planta Médica, v. 74, p. 1678-1683.
Costa, J. F. O.; David, J.P.L.; David, J.M.; Giulietti, A.M.; Queiroz, L.P; Santos, R.R.; Soares, M.B.P. 2008. Immunomodulatory activity of extracts from Cordia superba Cham. and Cordia rufescens A. DC. (Boraginaceae), plant species native from Brazilian semi-arid. Revista Brasileira de Farmacognosia, v. 18(1), p. 11-15.
Enciclopédia Médica citada por Refsio, C. 2005. Revista Brasileira de Medicina, v. 62, p. 40-45. http://www.enciclopediamedica.cl/movil/index. php?sec=6&list=1&item=5444), acesso em 04/01/2012.
Fernandes, E. S.; Passos, G. F. ; Medeiros, R. ; Cunha, F. M. ; Ferreira, J. ; Campos, M.M. ; Pianowski, L. F. ; Calixto, J.B. 2007. Anti-inflammatory effects of compounds α-humulene and (-)-trans-caryophyllene isolated from the essential oil of Cordia verbenacea. European Journal of Pharmacology, v. 569, p. 228-236.
Frezza, T.F.; Oliveira, A.S.S.; Simões, L.F.; Rehder, V.L.G.; Allegretti, S.M. 2010. Ação da fração etanólica de Cordia verbenacea na sobrevida de Schistosoma mansoni. Instituto de Biologia, Departamento de Biologia Animal/Parasitologia, UNICAMP, Revista Saúde, v. 4 (Esp.1), p. 124.
Hage-Melim, L.I.S. 2009. Estudo das interações entre fosfolipases A2 e o inibidor vegetal ácido rosmarínico de Cordia verbenacea (Boraginaceae) por cocristalização e modelagem molecular. Tese de doutorado em Toxicologia. Faculdade de Ciências Farmacêuticas de Ribeirão Preto/USP.
Lameira, O.A.; Pinto, J.E.B.P.; Arrigoni-Blank, M.F.; Cardoso, M.G. 1997. Efeito de compostos fenólicos, carvão ativado e do meio físico no desenvolvimento de segmento nodal de Cordia verbenacea L. Ciência Rural, Santa Maria, v. 27(2), p. 189-192.
Lorenzi, H. e Matos, F.J.A. 2002. Plantas Medicinais no Brasil, 2a edição, Plantarum, Odessa SP
Medeiros, R.; Passos, G.F.; Vitor C.E.; Koepp, J.; Mazzuco, T.L.; Pianowski, L.F.; Campos, M.M.; Calixto, J.B. 2007. Effect of two active compounds obtained from the essential oil of Cordia verbenacea on the acute inflammatory responses elicited by LPS in the rat paw. British Journal of Pharmacology, v. 151(5), p. 618-27.
Memento terapêutico. 2002. Programa de Fitoterapia, Secretaria Municipal de Saúde RJ, p. 16.
Miller, R.W.; Earle, F.R.; Wolff, I.A.; Barclay, A.S. 1968. Search for new seed oils. XV. Oils of Boraginaceae. Lipids, v. 3(1), p. 43-45.
Oliveira, A.A.M.; Abdalla, D.S.P.; Sertié, J.A.A. 1998. Hematological evaluation of the ethanol extract of Cordia verbenacea leaves. Fitoterapia, v. 65, p. 387-390.
Panizz, S. 1998. Plantas que Curam (Cheiro de Mato), 3a. Ed., IBRASA, São Paulo, 280pp.
Passos, G.F.; Fernandes, E.S.; Da Cunha, F.M.; Ferreira, J.; Pianowski, L.F.; Campos, M.M.; Calixto, J.B. 2007. Anti-inflammatory and anti-allergic properties of the essential oil and active compounds from Cordia verbenacea. Journal of Ethnopharmacology, v. 110(2), p. 323-333.
Rapisarda, A.; lauk, L; Ragusa, S. 1997. Micromorphological Study on Leaves of Some Cordia (Boraginaceae) species used in tradicional medicine. Economic Botany, v. 51(4), p. 385-391.
Refsio, C.; Brandão, D.C.; Brandão, G.C.; Korukian, M.; Garcia, R.J.; Bonfigliori, R.; Nery, C.A.S.; Gamba, R. 2005. Avaliação clínica da eficácia e segurança do uso de extrato padronizado da Cordia verbenacea em pacientes portadores de tendinite e dor miofascial I Clinical assessment of efficacy and safety from Cordia verbenacea standartized extract in tendinitis and chronical miofacial pain patients. Revista Brasileira de Medicina, v. 62(1/2), p. 40-46.
Roldão, E.F.; Witaicenis, A.; Seito, L.N.; Hiruma-Lima, C.A.; Di Stasi, L.C. 2008. Evaluation ofthe antiulcerogenic and analgesic activities of Cordia verbenacea DC. (Boraginaceae). Journal of Ethnopharmacology, v. 119, p. 94-98.
Rogério, A.P.; Andrade, E.L.; Leite, D.F.P.; Figueiredo, C.; Calixto, J.B. 2009. Themed section: mediators and receptors in the resolution of inflammation. Preventive and therapeutic anti-inflammatory properties ofthe sesquiterpene α-humuleno in experimental airways allergic inflammation. British Journal of Pharmacology, v. 158, p. 1074-1087.
Queiroz, E.F.; Faro, R.R.A.; Melo, C.A. 2009. A biodiversidade brasileira como fonte de novas drogas: passado, presente e futuro. RDF - Revista de Fitoterapia, v. 9(1), p. 31-35.
Santos, R.P.; Nunes, E.P.; Nascimento, R.F.; Santiago, G.M.P.; Menezes, G.H.A.; Silveira, E.R.; Pessoa, O.D.L. 2006. Chemical Composition and Larvicidal Activity of the Essential Oils of Cordia leucomalloides and Cordia curassavica from the Northeast of Brazil. Journal Brazilian Chemistry Society, v. 17(5), p. 1027-1030.
Seigler, D.S.; Mikolajczak, K.L.; Smith Jr., C.R.; Wolff, I.A. 1970. Structure and Reactions of a cyanogenetic lipid from Cordia verbenacea DC. Seed oil. Chemistry and Physics of Lipids, v. 4, p. 147-161.
Sertié, J.A.A; Basile, A.C.; Panizza, S.; Matida, A.K.; Zelnik, R. 1988. Pharmacological Assay of Cordia verbenacea' Part 1. Anti-Inflammatory Activity and Toxicity of the Crude Extract of the Leaves. Planta Medica, v. 54, p. 7-10.
Sertié, J.A.A.; Basile, A.C.; Panizza, S.; Matida, A.K.; Zelnik, R. 1990. Antiinflamatory activity and sub-acute toxicity of artemetin. Planta Medica, v. 56(11), p. 36-40.
Sertié, J.A.A.; Basile, A.C.; Panizza, S.; Oshiro, T.T.; Azzolini, C.P.; Penna, S.C. 1991. Pharmacological assay of Cordia verbenacea III: oral and topical antiinflammatory activity and gastrotoxicity of a crude leaf extract. Journal of Ethnopharmacology, v. 31, p. 239-247.
Sertié, J.A.A.; Woisky, R.G.; Wiezel, G.; Rodrigues, M. 2005. Pharmacological assay of Cordia verbenacea V: oral and topical anti-inflammatory activity, analgesic effect and fetus toxicity of a crude leaf extract. Phytomedicine, v.12(5), p. 338-344.
Silva Jr., A. A.; Vizzoto, V.J.; Giorgi, E. 1995. Plantas medicinais, caracterização e cultivo. Boletim Técnico, 68. Florianópolis, EPAGRI, 71p.
Souza, G.C.; Haas, A.P.S.; Poser, G.L.; Schapoval, E.E.S.; Elisabetsky, E. 2004. Ethnopharmacological studies of antimicrobial remedies in the south of Brazil. Journal ofEthnopharmacology, v. 90, p. 135-143.
Souza, M.E; Nery, P.S.; Manganotti, S.A.; Matos, C.C.; Martins, E.R. 2009. Conteúdo de óleo essencial de Cordia verbenacea em diferentes horários de coleta. Revista Brasileira de Agroecologia, v. 4(2), p. 26722675. Resumos VI CBA e II CLAA.
Ticli, F.K. ; Hage, L.I.; Cambraia, R.S.; Pereira, P.S.; Magro, A.J.; Fontes, M.R.; Stabeli, R.G.; Giglio, J.R.; França, S.C.; Soares, A.M.; Sampaio, S.V. 2005. Rosmarinic acid, a new snake venom phospholipase A2 inhibitor from Cordia verbenacea (Boraginaeae): anriserum action potentiation and molecular interaction. Toxicon, v. 46(3), p. 318-327.
Vaz, A. P. A.; Scaranari, C.; Batista, L.A.R.; Figueira, G.M.; Sartoratto, A.; Magalhães, P. M. 2006. Biomassa e composição química de genótipos melhorados de espécies medicinais cultivadas em quatro municípios paulistas. Pesquisa Agropecuária Brasileira, v. 41(5), p. 869-872.
Velde, V.V.; Lavie, D.; Zelnik, R.; Matida, A.K. e Panizza, S. 1982. Cordialin A and B, two new triterpenes from Cordia verbenacea DC J., Chemistry Society, Perkin Trans., v. 1,p. 2697-2700.
Ventrella, M.C.; Marinho, C.R. 2008. Morphology and histochemistry of glandular trichomes of Cordia verbenacea DC. (Boraginaceae) leaves. Revista Brasileira Botânica, v. 31(3), p. 457-467.