Resumo
A Síndrome do Ovário Policístico (SOP) consiste em distúrbio comum entre mulheres em idade reprodutiva. Portadoras de SOP em geral são mais susceptíveis ao desenvolvimento de diabetes, doenças cardiovasculares e câncer no endométrio, resultante do quadro de inflamação, hiperandrogenismo e resistência insulínica. A farmacoterapia em uso para controle da SOP tem sido acompanhada por efeitos colaterais, ressaltando a relevância de pesquisas para novos tratamentos. Uma vez que metabólitos secundários têm demonstrado potencial na melhora do quadro sintomático da SOP, esse trabalho teve como objetivo realizar uma revisão sistemática da literatura abordando recentes achados nessa temática. As bases de dados utilizadas foram BVS (Biblioteca Virtual de Saúde), PubMed e Science Direct, com os critérios de inclusão: artigos experimentais no idioma inglês, período de 2020 a 2023 e compostos isolados de espécies vegetais. Como resultado, foram encontrados 14 compostos, predominantemente fenólicos, com estudos pré-clínicos e/ou clínicos. Na análise in silico 12 compostos não violaram as regras de Lipinski e Veber. Quanto à predição da toxicidade, a maioria dos compostos foi classificada nas classes IV e V, considerados com reduzida toxicidade se ingeridos. Os dados obtidos apontam para o futuro da farmacoterapia da SOP englobando compostos oriundos de fonte natural.
Saúde da Mulher; Síndrome do ovário policístico; Metabólito Secundário Vegetal; Pesquisa pré-clínica e clínica; Predição in silico; Potencial Tóxico
Abstract
The Polycystic Ovary Syndrome (PCOS) is a common disorder in women of reproductive age. PCOS carriers are usually more susceptible to developing diabetes, cardiovascular diseases, and endometrial cancer, resulting from inflammation, hyperandrogenism, and insulin resistance. Pharmacotherapy currently in use to control PCOS has been accompanied by side effects, highlighting the relevance of research into new treatments. Since secondary metabolites have shown potential in improving the symptomatic condition of PCOS, this study aimed to conduct a systematic literature review addressing recent findings on this topic. The databases used were BVS (Virtual Health Library), PubMed and Science Direct, with the inclusion criteria being experimental articles in English, from the period 2020 to 2023, and isolated compounds from plant species. As research resulted, 14 compounds were found, predominantly phenolic, with preclinical and/or clinical studies. In the in silico analysis, 12 compounds did not violate Lipinski's and Veber's rules. Regarding toxicity prediction, most compounds were classified in classes IV and V, considered to have reduced toxicity if ingested. The data obtained point to the future of PCOS pharmacotherapy encompassing compounds derived from natural sources.
Women's Health; Polycystic Ovary Syndrome; Plant Secondary Metabolite; Preclinical and Clinical Research; In silico Prediction; Toxic Potential
Introdução
A Síndrome do Ovário Policístico (SOP) é um distúrbio com etiologia multifatorial que abrange aspectos relacionados ao metabolismo glicêmico e lipídico e aos distúrbios hormonais com a desregulação do eixo hipotálamo-hipófise na produção de FSH, LH, testosterona, estrogênio, dessensibilização insulínica e inflamação crônica. A apresentação clínica é variável, podendo incluir infertilidade, hirsutismo, obesidade abdominal, acne entre outros sintomas. Cabe ressaltar que as pacientes estão mais propensas a desenvolver problemas cardiovasculares, obesidade, quadros de depressão e ansiedade1,2.
Devido à ampla heterogeneidade de sinais e sintomas da SOP, foram estabelecidos diferentes fenótipos para o diagnóstico com base nos critérios estabelecidos no Consenso de Rotterdam, juntamente a Sociedade Europeia de Reprodução Humana e Embriologia (ESHRE) e Sociedade Americana de Reprodução Médica (ASRM), considerando as manifestações clínicas e laboratoriais de forma individualizada e, também, a prevalência de riscos associados como resistência insulínica e diabetes. Os fenótipos apresentam diferente intensidade na expressão de sintomas, tendo sido classificados em clássicos A e B, onde o primeiro é mais grave com a presença de hiperandrogenismo, oligo-ovulação, morfologia ovariana policística e aumento dos riscos de resistência insulínica e síndromes metabólicas, já o fenótipo B se caracteriza pela presença de oligo-ovulação, aumento androgênico, mas sem a presença de ovários policísticos. Por sua vez, os fenótipos menos complexos são o C, onde há a presença da morfologia policística e hiperandrogenismo com ovulação normal, e o D em que ocorre normoandrogênia, oligo-ovulação e morfologia policística2,3.
Atualmente, o tratamento da SOP tem uma abordagem multifacetada, tratando sintomas específicos dependendo do fenótipo expresso por cada paciente, tendo o objetivo de reduzir sintomas pontuais como a oligo-ovulação, o hiperandrogenismo e a resistência insulínica de forma isolada. Além disso, mudanças no estilo de vida são relevantes para diminuir complicações decorrentes da desregulação hormonal, contribuindo para benefícios em nível endócrino normalizando hormônios e períodos menstruais, além de impactar na melhoria dos perfis de glicose e lipídeos. Não há medicamento específico para indicação de SOP aprovado pelos órgãos reguladores, a farmacoterapia atual, conforme Protocolo Clínico e Diretrizes Terapêuticas do Ministério da Saúde, é adaptada a cada indivíduo e sua respectiva expressão fenotípica, muitos indicados de forma off-label3.
Sendo assim, as pesquisas voltadas para a síndrome têm envolvido estudos genômicos, possibilitando uma ampliação nas investigações acerca das vias metabólicas e fisiopatológicas envolvidas como as hipotálamo-hipofisárias, de ação gonadotrófica, ação e secreção de insulina, distúrbios do tecido adiposo, homeostase, metabolismo lipídico e inflamação crônica4.
Considerando que a prospecção de novas moléculas para o tratamento da SOP mostra-se importante para a ampliação do escopo de medicamentos, tendo como fonte promissora aquelas oriundas de espécies vegetais, o objetivo desse trabalho foi compilar pesquisas recentes referentes a tais compostos potencialmente eficazes na SOP. A revisão abrange estudos pré-clínicos e clínicos, com os principais mecanismos de ação envolvidos. Ainda, para as moléculas encontradas foi realizada abordagem in silico com a avaliação dos parâmetros físico-químicos e predição do potencial tóxico.
Materiais e Métodos
Estratégia de busca nas bases de dados
O trabalho foi desenvolvido através de uma revisão sistemática da literatura utilizando as seguintes bases de dados: BVS (Biblioteca Virtual em Saúde), PubMed (U.S National Library of Medicine) e Science Direct. A busca do material para elaboração deste estudo considerou publicações em inglês, com delimitação de tempo no intervalo de 2020 a 2023. Como descritores foram utilizados os termos “polycystic ovary syndrome” e “compounds” com o operador booleano AND. Os critérios de inclusão na pesquisa foram: artigos disponíveis na íntegra, com pesquisa experimental sobre a eficácia, em fase pré-clínica e clínica, de compostos isolados oriundos de produtos naturais de espécies vegetais voltados para o tratamento da SOP. Os critérios de exclusão foram: artigos de revisão, relato de caso e artigos em outros idiomas além do inglês, e artigos indisponíveis gratuitamente nas bases de dados.
Predição in silico
A predição in silico dos compostos encontrados nos artigos selecionados incluiu o estudo de Drug-likeness levando em consideração as regras de Lipinski e Verber, com parâmetros calculados no Swiss ADME web tool (http://www.swissadme.ch/)5. Para a regra dos 5 de Lipinski foram avaliados o Peso Molecular (≤500), LogP (<5), doadores (≤5) e receptores (≤10) de ligações de hidrogênio)6. Já para a regra de Veber foi considerado o número de ligações rotacionáveis (≤10) e área de superfície polar topológica (≤140) (TPSA)7. A avaliação dos compostos nas regras citadas teve o intuito de fornecer informações sobre a farmacocinética dos compostos, referente à biodisponibilidade oral.
A avaliação da segurança dos compostos foi predita através da utilização do servidor online ProTox 3.0 (https://tox.charite.de/protox3/)8. Dentre os dados gerados pelo ProTox foram utilizadas as informações sobre dose letal 50 (DL50) em mg/kg por via oral e a categoria de toxicidade. ProTox considera seis classes de toxicidade, com base nos valores de referência de DL50: Classe I (DL50 ≤ 5) fatal se ingerido, Classe II (5<DL50 ≤ 50) fatal se ingerido, Classe III (50<DL50 ≤ 300) tóxico se ingerido, Classe IV (300<DL50 ≤ 2000) perigoso se ingerido, Classe V (2000<DL50 ≤ 5000) pode ser perigoso se ingerido e Classe VI (DL50 > 5000) não tóxico. A predição da interação toxicológica com alvos moleculares também foi realizada para os seguintes alvos: enzima aromatase, receptor de andrógeno e receptor de estrógeno. O resultado é apresentado como ativo ou inativo, sendo que ativo indica a ocorrência de uma interação tóxica, enquanto inativo significa que o composto não interage de forma tóxica. Além disso, a probabilidade (P) de ocorrência de cada resultado foi registrada.
O desenho das estruturas químicas que serão apresentadas no item Propriedade Farmacológica foi realizado no software ChemDraw® Ultra 12.0.
Resultados e discussões
A SOP é um dos distúrbios endócrino/metabólico que mais afeta mulheres em idade fértil, tendo sido reportado que 69% das pacientes apresentam quadro de infertilidade, 51% de amenorreia, e 41% de obesidade9. As intervenções terapêuticas atuais como os contraceptivos orais, supressores de hormônios andrógenos, sensibilizadores insulínicos e estimuladores da ovulação expõe a paciente a diversos efeitos adversos, tais como náusea, vômito e diarreia. Desse modo, a prospecção de novas moléculas oriundas de produtos naturais amplia o escopo para tratamentos potencialmente eficazes e seguros10,11.
Estudos recentes avaliando produtos naturais, utilizando extrato e frações de espécies vegetais, no tratamento da SOP têm apresentado promissores resultados. Como exemplo, a avaliação pré-clínica do extrato de Panax ginseng C. A. Meyer, contendo como composto majoritário o esteroide glicosilado Ginsenosídeo. Foi descrito que o uso do extrato resultou na regulação de níveis séricos de estradiol, da atividade da aromatase nos ovários e diminuição da incidência de ovários multicísticos recuperando o ciclo estral, além de apresentar atividade antioxidante e anti-inflamatória. Todos esses achados podem ser benéficos para a fisiopatologia da SOP12.
Outro exemplo inclui as fórmulas da medicina tradicional chinesa, que têm sido escolha comum para tratamentos complementares e alternativos, como, Cangfu Daotan Decoction, Zigui Decoction, Heqi San, Bushen Huatan Decoction e Siwu Decoction. Embora haja uma abundância de estudos na literatura que investigam os mecanismos por trás dessas fórmulas, a pesquisa sobre os compostos individuais é escassa, já que geralmente são compostas por extratos de várias espécies de vegetais13.
Além disso, em relação à biodiversidade brasileira a literatura tem enfatizado a sua relevância em pesquisas etnobotânicas e etnofarmacológicas para valorizar conhecimento tradicional voltado ao cuidado da saúde da mulher. Plantas medicinais utilizadas por comunidades de diferentes regiões e biomas brasileiros, se avaliadas e comprovadas a eficácia e segurança, poderão ser convertidas em medicamentos fitoterápicos disponibilizados pelo Sistema Único de Saúde (SUS) para garantir e promover a saúde da mulher no Brasil14.
Embora muitos estudos se concentrem na avaliação de extratos e frações de produtos naturais, há uma crescente percepção de que o uso de compostos isolados pode ser mais relevante para a obtenção de tratamentos com maior eficácia. Isso se deve ao fato de que os compostos isolados possibilitam uma compreensão mais clara de suas atividades farmacológicas e de seus mecanismos de ação, permitindo um ajuste mais preciso das doses e uma melhor otimização das formulações. Além disso, os compostos isolados geralmente passam por uma caracterização mais detalhada, o que contribui para a identificação de potenciais efeitos colaterais e interações medicamentosas11.
Para isso, as moléculas oriundas do metabolismo secundário de espécies vegetais são uma alternativa válida aos tratamentos já conhecidos. Uma das principais vantagens são os múltiplos alvos terapêuticos, o que pode ser especialmente benéfico no tratamento de condições complexas como a SOP, que envolvem tanto fatores endócrinos como metabólicos. Essas moléculas podem oferecer abordagens terapêuticas mais abrangentes e eficazes, reduzindo a necessidade de combinação de múltiplos medicamentos15.
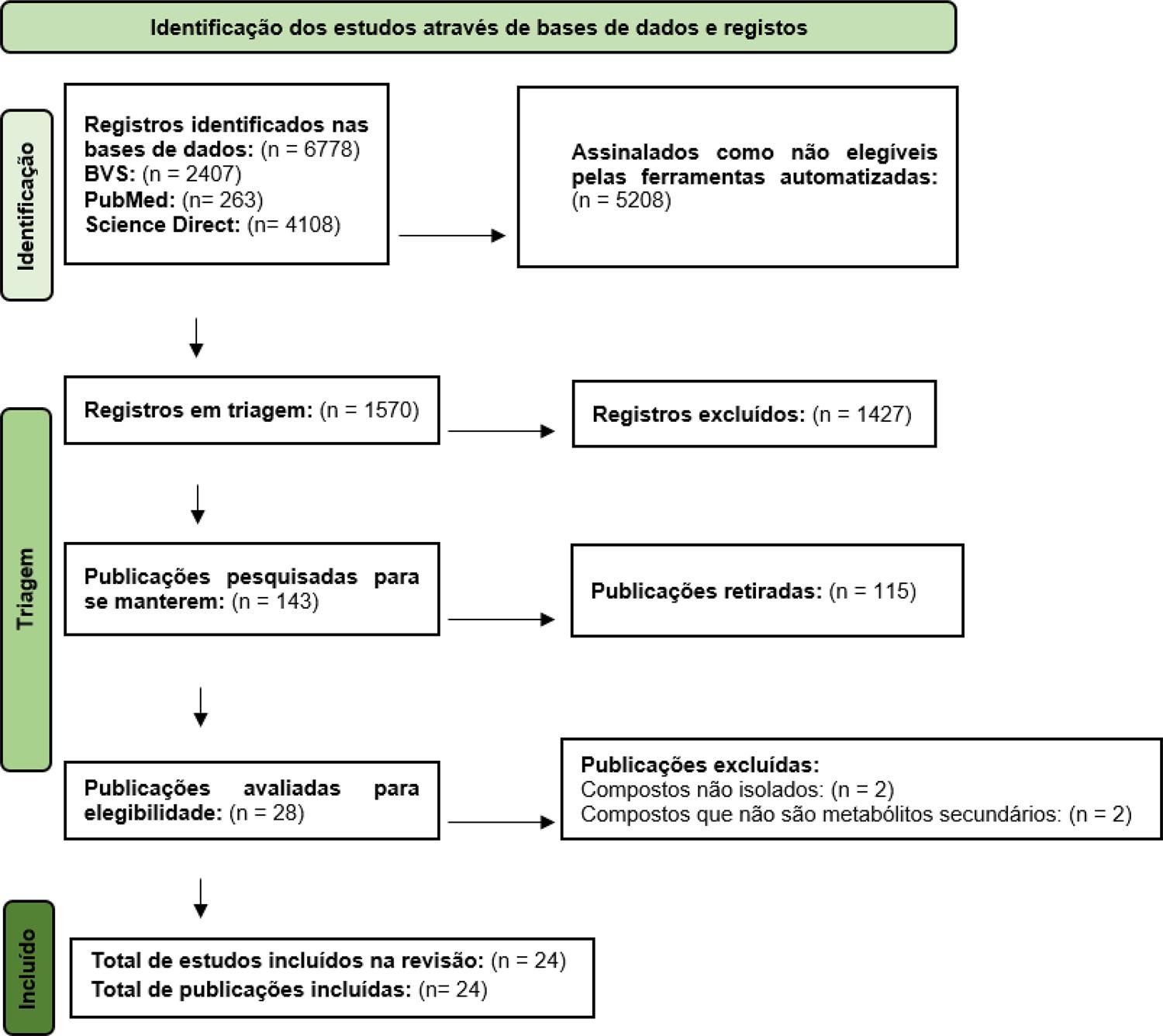
Neste contexto, essa revisão teve como foco a investigação por pesquisas científicas recentes de compostos isolados de espécies vegetais avaliados para tratamento da SOP. A busca resultou em 6778 artigos nas bases de dados BVS, PubMed e Science Direct, dos quais foram selecionados 24 seguindo os critérios de inclusão e exclusão definidos (FIGURA 1), publicados entre os anos de 2020 até 2023, no idioma inglês. Após seguir os critérios, foram encontrados quatorze compostos com estudos em fase pré-clínica, sendo que dois desses também avaliados em fase clínica. A maioria desses compostos (71,4%) pertence à classe dos compostos fenólicos majoritariamente da classe dos flavonoides. A Curcumina foi o metabólito secundário mais investigado contando com 25% das pesquisas, com estudos de fase pré-clínica e clínica. Cabe ressaltar que também foram encontrados compostos das classes dos alcaloides (7,1%), terpenos (7,1%) e os compostos (14,3%) que não se enquadram nas três grandes classes mencionadas, foram incluídos no grupo denominado demais compostos.
Os compostos avaliados demonstraram desempenhar atividade farmacológica especialmente através do mecanismo de ação que envolve vias do metabolismo da glicose, lipídeos, além de atuar na modulação de citocinas inflamatórias e enzimas associadas ao estresse oxidativo.
Na avaliação de Drug-likeness in silico, os parâmetros que fazem parte das regras de Lipinski e Veber foram utilizados para avaliar os quatorze compostos encontrados, a fim de contribuir com geração de dados referentes à biodisponibilidade por via oral. Na análise utilizando Swiss ADME web tool foi constado que doze não violam a regra Lipinski e Veber, podendo ser bom candidato a fármaco para administração por via oral. Na predição da DL50 no software ProTox, foi observado que 78,56% dos compostos pertencem a classe IV ou V, inferindo a partir dessa análise que a maioria dos compostos apresenta um menor risco de toxicidade em administração por via oral. A predição de toxicidade através da ligação aos alvos aromatase, receptor estrógeno e receptor estrógeno também foi avaliada, com 42,8% dos compostos demostrando atividade, ou seja, com potencial tóxico, em pelo menos um dos alvos escolhidos.
Na sequência os quatorze compostos serão apresentados em ordem alfabética, organizados no item Propriedade Farmacológica e subitens Alcaloides, Compostos Fenólicos, Terpenos e Demais compostos. Além da avaliação farmacológica, as informações apresentadas incluem a estrutura química de cada composto. No item Predição in silico os resultados são apresentados na forma de tabelas, juntamente com a discussão dos principais achados gerados pela análise dos compostos nos softwares Swiss ADME web tool e ProTox.
Propriedade Farmacológica
Alcaloides
Berberina
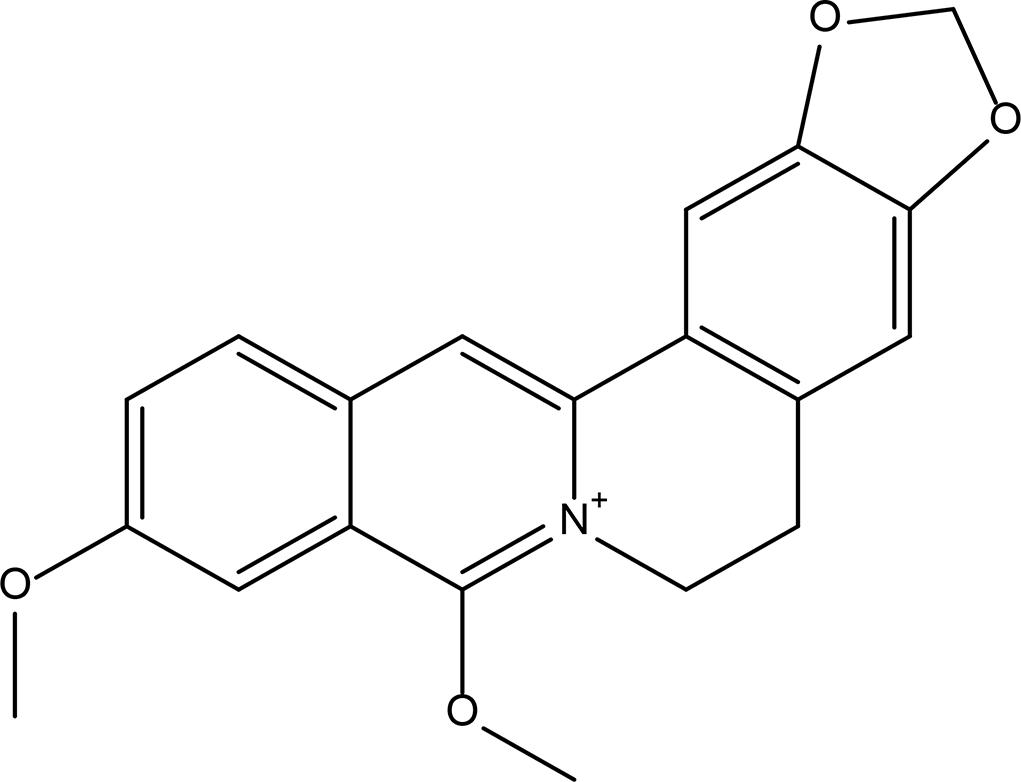
A Berberina (FIGURA 2) é um alcaloide isoquinolínico derivado comumente de espécies vegetais chinesas e amplamente usado para distúrbios metabólicos e infertilidade16,17.
Em estudo pré-clínico foi avaliado o potencial da Berberina em influenciar na expressão de GLUT4 (Transportador de Glicose), em ratas com SOP induzida por Letrozol, randomizadas em quatro grupos (n = 12 para cada grupo): Grupo 1: controle de veículo, Grupo 2, 3 e 4: tratados com Berberina (Dose: 400, 200 e 100 mg/kg, administração via intragástrica). Para isso, foi analisado o efeito do composto nas vias PI3K/AKT e MAPK que medeia o sinal do receptor de insulina. Após 28 dias de tratamento, os resultados obtidos demonstraram que a Berberina na concentração 400 mg/kg, melhorou as lesões patológicas da SOP no ovário como o tecido ovariano pálido, espessamento e os folículos císticos, também foi observada a diminuição do número de camadas de células granulosas levando a uma normalização morfológica e fisiológica. O mecanismo de ação relacionado foi do aumento da expressão da GLUT4 pela restauração da ativação da via PI3K/AKT e supressão da via MAPK, resultando na diminuição da resistência insulínica18.
Compostos fenólicos
Ácido Gálico
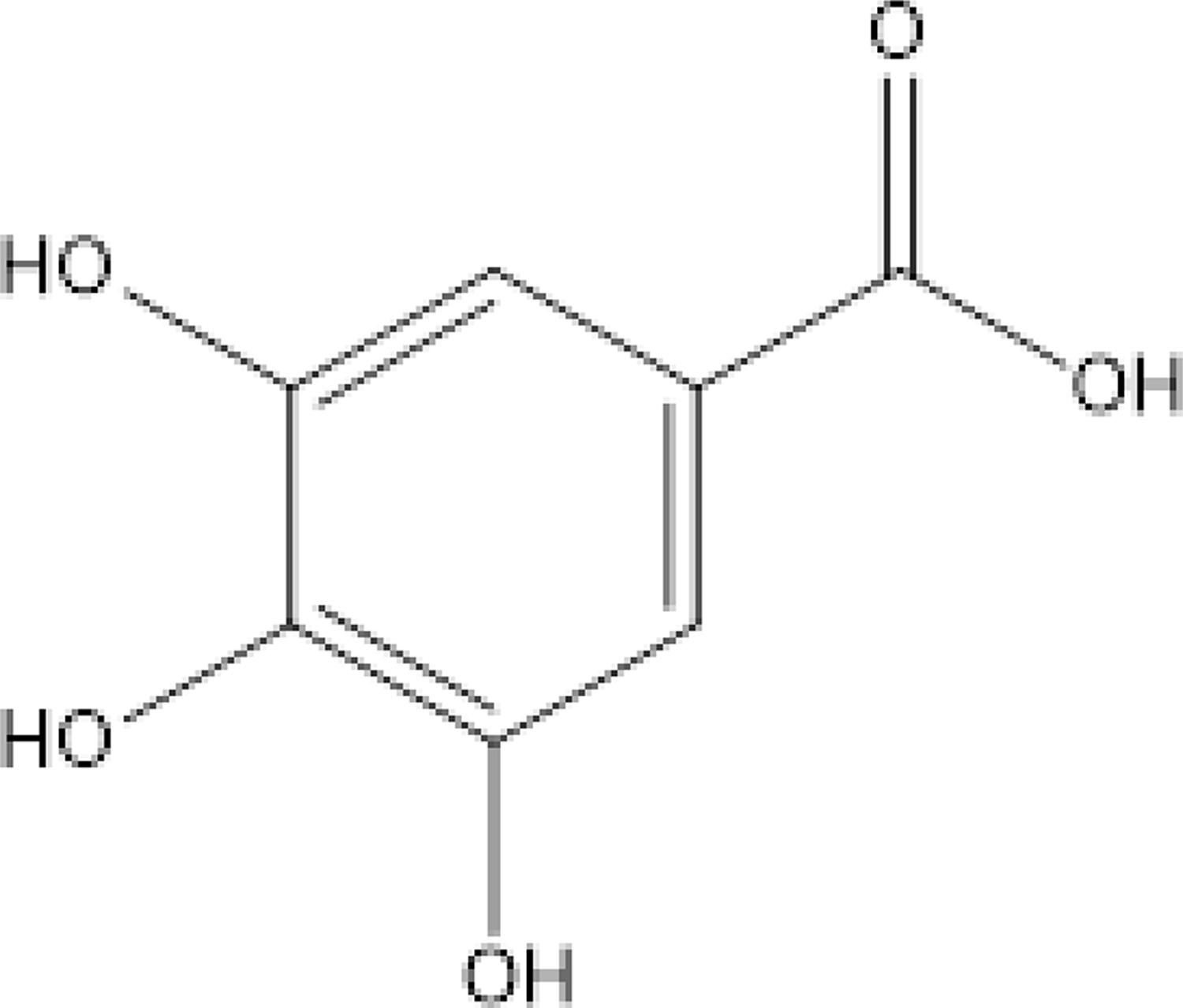
O Ácido Gálico (FIGURA 3) é um composto de coloração branca a levemente amarelado, derivado do ácido fenólico e encontrado em espécies vegetais do gênero Quercus L. e Punica L.19. Quanto às propriedades farmacológicas várias pesquisas têm descrito seu potencial como anti-inflamatório, anticâncer, antimicrobiano e antioxidante20.
Shah e colaboradores21 avaliaram o efeito do Ácido Gálico em dezoito fêmeas de camundongos induzidas a SOP após tratamento com Letrozol. Os animais foram divididos em três grupos: Grupo 1: controle, Grupo 2: Letrozol (Dose: 6 mg/kg), Grupo 3: Ácido Gálico (Dose: 75 mg/kg) por 60 dias e com administração por gavagem. Como resposta ao teste pré-clínico foi observado que os animais tratados com Ácido Gálico apresentaram redução dos níveis de testosterona, LH e da razão LH/FSH. O mecanismo é associado à diminuição do estresse oxidativo e de fatores inflamatórios, diminuição dos níveis das enzimas oxidantes malondialdeído (MDA), catalase (CAT) e superóxido dismutase (SOD), o que levou ao aumento na capacidade antioxidante celular. Observou-se também a diminuição de citocinas inflamatórias como TNF-α e IL-6 e do fator angiogênico VEGF, que são secretados em maior quantidade em mulheres com SOP. Além disso, os genes KITL e PTGS2, que são associados à foliculogênese, tiveram aumento no grupo tratado com Ácido Gálico, com normalização do desenvolvimento folicular e cistos ovarianos de menor expressão da aromatase e níveis mais altos de expressão de mRNA de genes relacionados à síntese de esteroides, incluindo Cyp19a1, reduzindo as anormalidades endócrinas e metabólicas. Também foi verificada a queda dos níveis de adiponectina, auxiliando a regular o metabolismo lipídico e a resistência insulínica.
Biochanin A
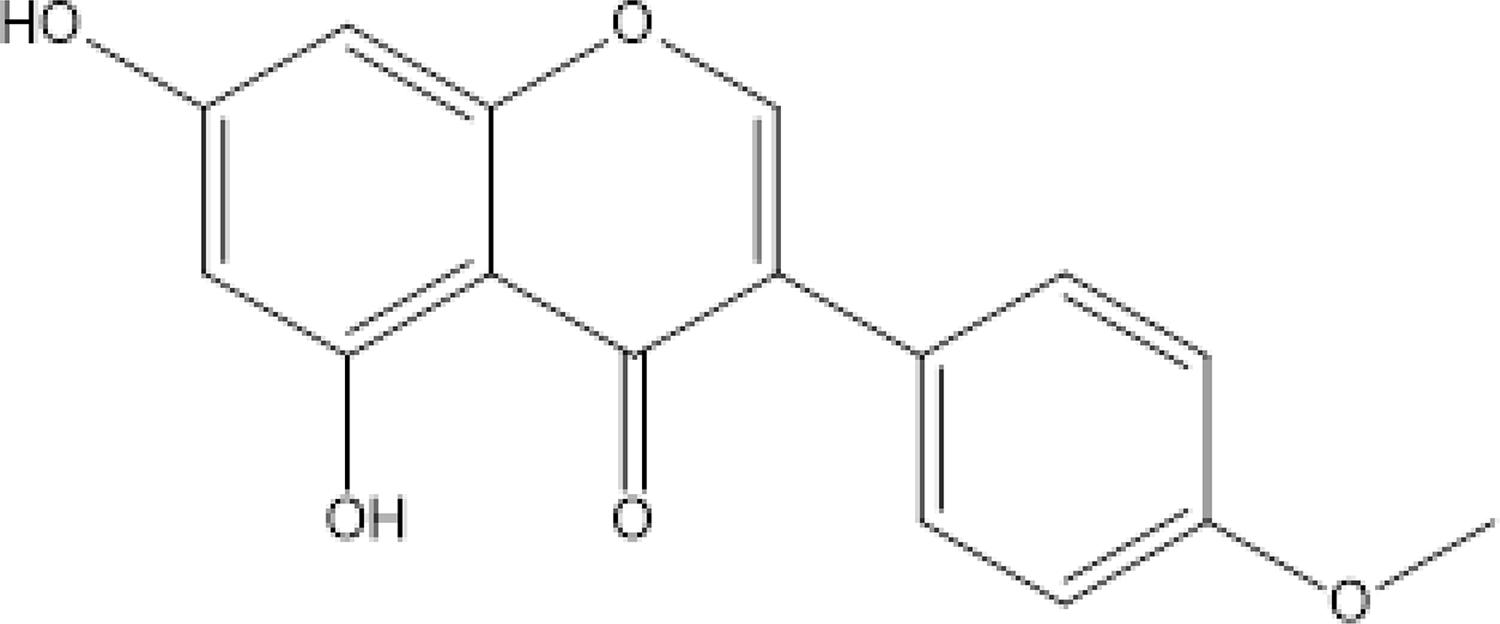
Biochanin A (49-metoxi genisteína; FIGURA 4) é um fitoestrógeno presente em Trifolium pratense L. (Fabaceae), que tem demonstrado diversas atividades biológicas, como em doenças cardiovascular, câncer, osteoporoses e sintomas menstruais22. Além disso, é utilizado em suplementos com indicação para desequilíbrios hormonais, tendo como alvo terapêutico a modulação seletiva de receptores de estrogênio23.
Em pesquisa realizada por Kotipalli e colaboradores24 foi avaliado o efeito do Biochanin A nos alvos TGFβ, GDF9 e BMP15 de ovários de fêmeas de camundongos induzidas a SOP com DHEA (dehidroepiandrosterona). O estudo foi conduzido com seis grupos (n= 6 para cada grupo): Grupo 1: controle veículo (óleo de gergelim), Grupo 2: controle com animais induzidas a SOP sem tratamento, Grupo 3, 4 e 5: tratados com Biochanin A nas doses 20, 40 e 50 mg/kg/dia, e Grupo 6: tratados com Metformina (Dose: 50 mg/kg/dia). Os animais tratados com a Biochanin A na concentração de 40 mg/kg apresentaram redução do peso corporal. Em relação aos parâmetros bioquímicos, para o perfil lipídico foi observada a redução dos níveis de colesterol total e triglicerídeos de forma dose dependente, porém não ocorreu alteração nos níveis das transaminases (TGO e TGP). No estudo também foi observada a regulação hormonal de LH, LH/FSH, testosterona, adiponectina e insulina com redução a resistência à insulina. O efeito anti-inflamatório do composto foi demonstrado pela diminuição das citocinas pró-inflamatórias, TNF-α, IL-6 e IL-1β. A administração de Biochanin A no tecido ovariano resultou em folículos saudáveis e um aumento no número de corpos lúteos no ambiente ovariano, houve também uma regulação positiva dose dependente de GDF9, TGFβR1 e BMPR2 no núcleo, células da granulosa e células da teca de ovários. Os resultados demonstraram a eficiência de Biochanin A na patologia da SOP.
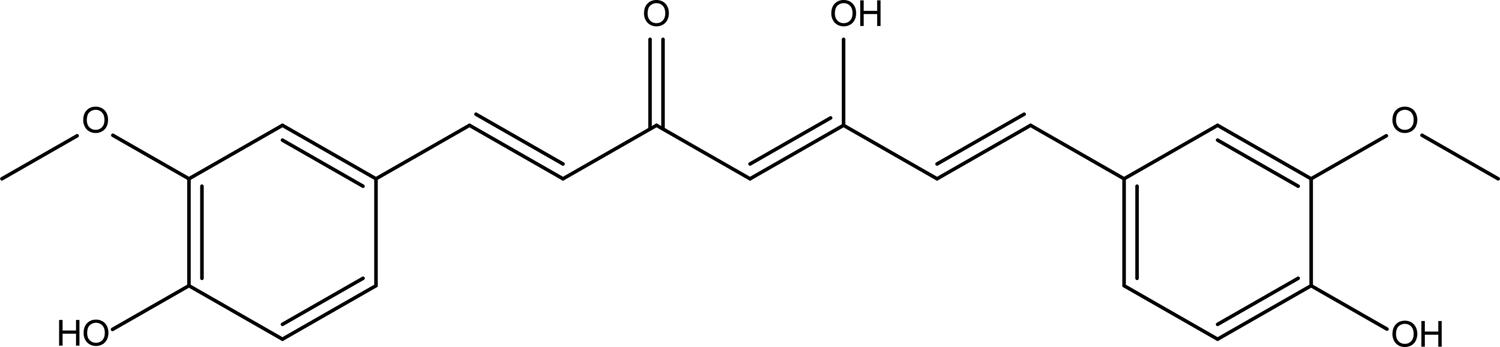
Curcumina
A Curcumina (FIGURA 5) é um composto polifenólico derivado das raízes de Curcuma longa L. (Zingiberaceae) com alto potencial antioxidante25, anti-inflamatório26 e hipoglicêmico27. Estudos pré-clínicos e clínicos, que serão apresentados na sequência, demonstram promissora ação da Curcumina no tratamento da SOP.
Com relação às pesquisas pré-clínicas, tem sido abordado possíveis hipóteses sobre os mecanismos e vias envolvidas na atividade antioxidante e anti-inflamatória. Em estudo desenvolvido por Abuelezz e colaboradores28, a Curcumina foi avaliada em seis grupos (n= 10 para cada grupo): Grupo 1: controle negativo (CMC a 0,5% por via oral), Grupo 2 (grupo SOP): letrozol (concentração: 1 mg/kg/dia por 23 dias), Grupo 3: letrozol por 23 dias seguido de citrato de clomifeno em CMC 0,5% (concentração: 1 mg/kg) por via oral durante 15 dias, Grupos 4, 5 e 6: nanocurcumina (Dose: 50 mg/kg, 100 mg/kg e 200 mg/kg) por 15 dias, em ratas induzidas a SOP por letrozol. Os resultados apontam para o restabelecimento da capacidade de funcionamento da via PI3K/AKT/mTOR que restaurou os níveis hormonais, além de melhorar captação de glicose e diminuir resistência insulínica.
Abhari e colaboradores29avaliaram nanopartículas de óxido de ferro supermagnético carregado com Curcumina (Dose: 5,4 mg/100g por 20 dias) no tratamento de fêmeas de camundongos com SOP induzida por DHEA. O estudo foi realizado em quarenta fêmeas de ratos divididas em quatro grupos: Grupo 1: controle, Grupo 2: veículo (óleo de gergelim), Grupo 3: DHEA (6 mg/100 g) e Grupo 4: DHEA mais nanopartículas de Curcumina. A pesquisa demonstrou a diminuição do volume ovariano, minimização dos danos às células granulosas e do número de folículos. O resultado observado se deu, principalmente, pela diminuição de fatores apoptóticos como BAX e níveis de expressão da proteína Caspase3 (CASP3) e aumento dos níveis de células B expressão de linfoma 2 (Bcl2). De forma geral, foi observada propriedade protetora das nanopartículas de Curcumina nas lesões ovarianas e apoptose induzida por DHEA.
Em estudo in vitro com Curcumina foi utilizado o oocisto de sessenta fêmeas divididas em cinco grupos: Grupo 1: oócitos controle, Grupo 2: oócitos do grupo com SOP, Grupo 3: oócitos do grupo com SOP tratado com 6 µM de Curcumina, Grupo 4: oócitos do grupo com SOP tratado com 12 µM de Curcumina e Grupo 5: ovócitos experimentais do grupo SOP tratado com 24 µM de Curcumina. As fêmeas de camundongos foram induzidas a SOP por valerato de estradiol. No estudo foi avaliada a capacidade antioxidante total no tecido ovariano e soro sanguíneo, sendo observado que no grupo controle com SOP os valores foram menores que no grupo tratado com a substância em questão. Além disso, verificou-se que a SOP causa efeitos destrutivos as células oócitárias, diminuindo a probabilidade de desenvolvimento de embriões, o que pode levar a dificuldades na fertilização. Estratégias de diminuição de EROs, com o uso da Curcumina, pode melhorar a qualidade dos oócitos e com diminuição dos danos oxidativos nas células envolvidas30.
Jamilian e colaboradores31 avaliaram Curcumina (Dose: 500 mg/dia) em ensaio clínico randomizado duplo cego em mulheres com SOP (n= 30), comparando os resultados em mulheres com SOP recebendo o placebo (n= 30), por 12 semanas. A intervenção teve como objetivos avaliar os parâmetros relacionados a peso corporal, glicemia e lipídeos séricos. No primeiro parâmetro houve uma redução significante diminuindo a massa gorda, estresse adipocitário e resistência insulínica. Efeitos positivos foram observados nos lipídeos séricos com diminuição da dislipidemia, bem como, na diminuição da glicemia. Foi observado que a melhora desses fatores está associada ao aumento da expressão do gene PPAR-y que são receptores ativados por proliferadores de peroxissoma tipo gama que atuam na melhoria da homeostase da glicose, sensibilidade à insulina e controle da expressão gênica e desempenham papéis-chave no metabolismo lipídico e glicídico.
Outro ensaio clínico randomizado duplo cego em portadoras de SOP que receberam Curcumina (Dose: 500 mg três vezes ao dia; n= 34) ou placebo (n= 33) (maltodextrina) em cápsula, constatou a diminuição dos níveis de glicemia de jejum e hormônios andrógenos, sendo que o nível de estradiol não apresentou aumento estatisticamente significativo quando comparado com o grupo controle. Assim, foi demonstrado que após 12 semanas, a suplementação com esse composto fenólico pode ser benéfica e segura em pacientes com SOP32.
Ghanbarzadeh-Ghashti e colaboradores33 avaliaram a atuação da Curcumina, nos parâmetros metabólicos glicêmicos e lipídico, nos níveis de andrógenos (resultados primários), características menstruais e hirsutismo (resultados secundários) em mulheres com SOP. Foi realizado estudo clínico randomizado controlado em dois grupos, um tratado com Curcumina (Dose: comprimidos de 500 mg/dia, n= 27) e outro placebo (comprimidos com mesma cor, cheiro, forma e peso quando comparado ao comprimido de Curcumina, n= 27), por 12 semanas. Como desfechos foram obtidos resultados mostrando a diminuição dos níveis de glicemia em jejum, insulina em jejum e avaliação do modelo homeostático para resistência à insulina no grupo de intervenção. No entanto, para os demais índices como triglicerídeos, colesterol, LDL-C, HDL-C, insulina, testosterona e globulina de ligação ao hormônio sexual não houve diferenças. O grupo tratado com Curcumina mostrou melhora nas características menstruais (amenorreia, oligomenorreia e irregularidades menstruais), porém o mesmo não foi observado para os índices metabólicos, hormonais e o hirsutismo.
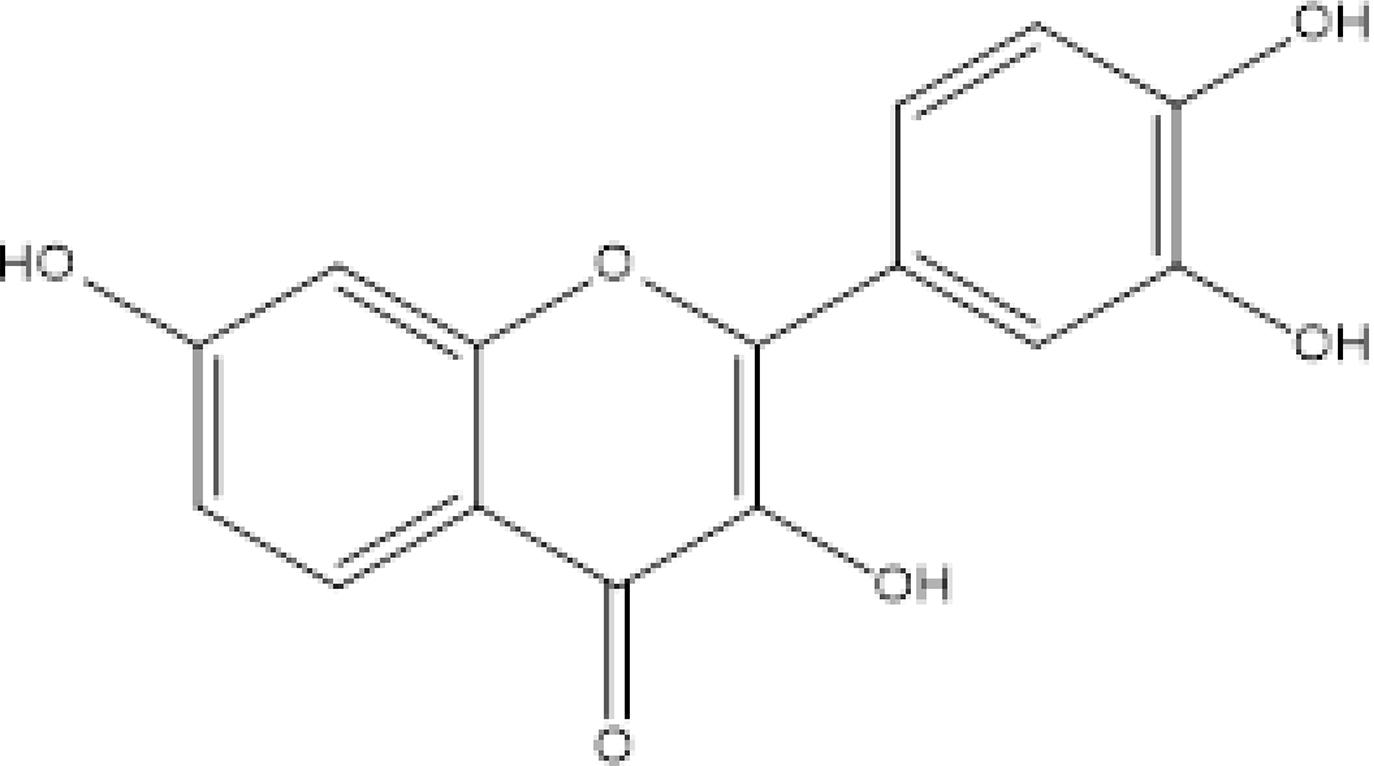
Fisetina
Para o flavonoide Fisetina (3,7,3′,4′-tetrahidroxiflavona, FIGURA 6) tem sido relatada atividade como anti-inflamatório, antioxidante, antiobesidade, antiplaquetária, antihiperlipidêmico e antidiabético34-36.
O estudo pré-clínico com o composto foi realizado com ratas divididas em quatro grupos: Grupo 1: controle, Grupo 2: ratas induzidas a SOP por Letrozol, Grupo 3: ratas induzidas a SOP por Letrozol tratadas com Fisetina (Dose: 10 mg/kg/dia por 30 dias) e Grupo 4: ratas induzidas a SOP por Letrozol tratadas com Metformina (Dose: 300 mg/kg por 30 dias). Como resultado verificou-se que Fisetina não causou significante redução do peso corporal, mas normalizou os níveis de glicose e o perfil lipídico, reduziu os níveis séricos de testosterona, além do aumento de estradiol e progesterona. Como mecanismo de ação foi possível verificar que a expressão de AMPK e SIRT1 foi aumentada e a de CYP17A1 foi diminuída, houve também o aumento da atividade enzimática de antioxidantes, incluindo CAT, SOD e GPx. O efeito da Fisetina pode estar relacionado na expressão de mRNA e CYP17A1, além da indução de SIRT1 e AMPK37.
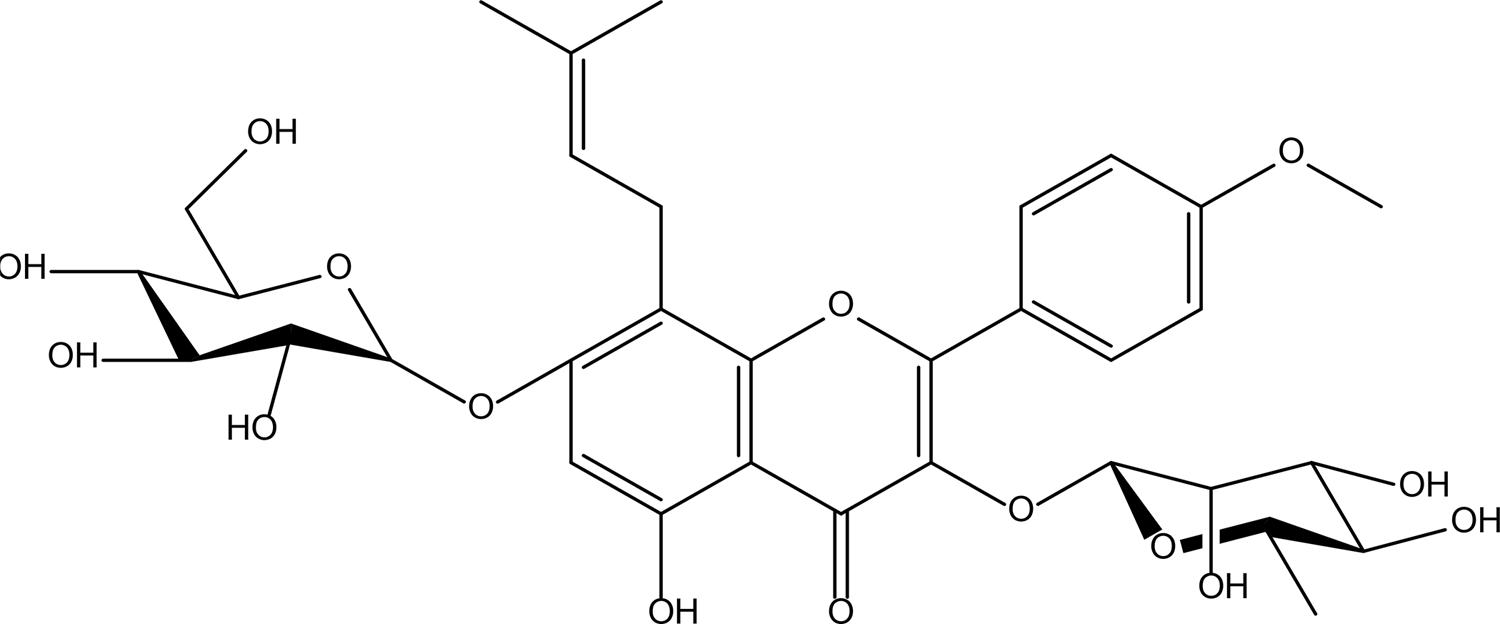
Icariina
Icariina (FIGURA 7), flavonoide glicosídeo derivado do kaempferol, é o principal composto ativo de ervas do gênero Epimedium L., que é utilizada na medicina tradicional chinesa para tratar a SOP e outras doenças ginecológicas38,39. Tem sido descrito com propriedade anti-inflamatória que pode melhorar a função ovariana40.
Em ensaio pré-clínico com a Icariina, Zuo e colaboradores41avaliaram o efeito do composto em ratas induzidas a SOP com Letrozol. Os animais foram divididos em quatro grupos (n= 9 para cada grupo): Grupo 1: controle, Grupo 2: carboxicelulose de cálcio a 0,5% (Dose: 10 ml/kg/dia), Grupo 3: tratados com Icariina (Dose: 40 mg/kg/dia) e Grupo 4: tratados com Icariina (Dose: 80 mg/kg/dia), com administração por gavagem. Foram obtidos os seguintes resultados com resposta dose-dependente: supressão de testosterona sérica, LH, razão LH/FSH e cistos foliculares. FSH sérico, estradiol e progesterona aumentaram, além do ciclo estral restaurado, melhorando a função ovariana. Houve ainda a redução nos níveis de IL-6 e TNF-α e da expressão de proteínas apoptóticas como Bax e Bad e a razão Bax/Bcl2, reduzindo apoptose nas células dos ovários e diminuindo a inflamação. Nos metabolismos de glicose e lipídeos foram observados controle dos níveis triglicerídeos, insulina em jejum e HOMA-IR que estavam elevados com a indução a SOP.
Macelignana
O monômero pertencente à classe das lignanas, Macelignana (FIGURA 8), obtido da noz-moscada, exibe estrutura química semelhante ao estrogênio natural, e acredita-se que se comporte como modulador seletivo de receptores de estrogênio. Pesquisas tem descrito que esse composto apresenta atividade anti-inflamatória e antioxidante, podendo ser uma molécula promissora se aplicada no tratamento da SOP42,43.
Esse composto foi avaliado por Shi e colaboradores44em fêmeas de camundongos induzidas a SOP com DHEA, divididas em cinco grupos (n= 8 para cada grupo): Grupo 1: controle, Grupo 2: DHEA (6 mg/100g), Grupo 3: Pílula Nuangong Qiwei (Dose: 1,3 mg/g/dia), Grupo 4: Diane-35 (Dose: 0,0052 mg/dia) e Grupo 5: Macelignana (Dose: 0,03 mg/dia). A administração foi por via intragástrica na concentração durante 21 dias. Os resultados demostraram melhoria no peso ovariano, ciclo estral, no número de folículos antrais, redução de apoptose de células granulosa, aumentando significativamente os níveis de estrogênio, redução da testosterona, progesterona, nos níveis de LH e da razão LH/FSH, alívio na depressão e ansiedade. Na atividade antioxidante, o composto causou uma melhora nos níveis de enzimas oxidativas como SOD, MDA e GSH. Foi verificada a redução dos níveis de mRNA do fator inflamatório ovariano IL-6, sugerindo que o composto melhora os níveis de transcrição de genes relacionados à inflamação e apoptose no tecido ovariano dos animais com SOP. Ocorreu aumento da expressão transcricional do gene codificador da aromatase ovariana, CYP19A1, que tem um efeito positivo na secreção de estrogênio e melhora os níveis de expressão de TGF-β3 e SMAD 2, normalizando os distúrbios hormonais.
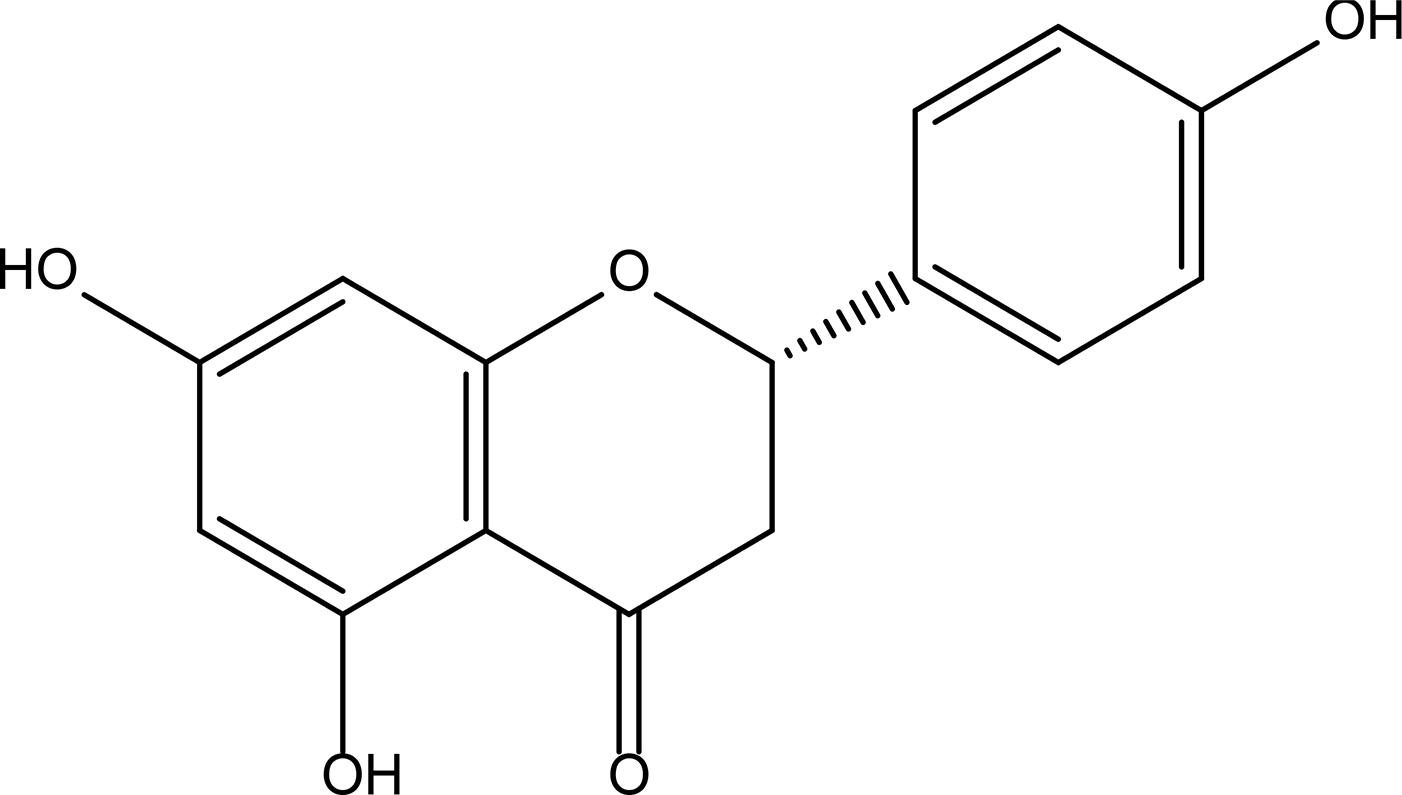
Narigenina
O flavonoide Narigenina (FIGURA 9), estruturalmente semelhante com esteroides, tem sido isolado de várias espécies vegetais, como Typha angustifolia L. (Typhaceae), Citrus aurantium L. (Rutaceae) e Amygdalus persica L. (Rosaceae), com promissora aplicação como anti-inflamatório, casos de obesidade e doenças intestinais45.
Em ensaio pré-clínico desenvolvido por Dashputre e colaboradores46, Narigenina foi avaliada na forma nanoparticulada devido à sua baixa solubilidade em água, favorecendo assim a sua biodisponibilidade oral. A avaliação foi realizada em ratas divididas em cinco grupos (n= 6 para cada grupo): Grupo 1: controle, Grupo 2: Letrozol (Dose: 1 mg/kg), Grupo 3: Narigerina (Dose: 50 mg/kg), Grupo 4: Narigerina (Dose: 100 mg/kg) e Grupo 5: Citrato de Clomifeno (Dose: 1 mg/kg). A SOP foi induzida nas ratas com Letrozol. Como resultado foi verificado que a Narigenina teve impacto protetor na concentração de hormônios sexuais, com diminuição de níveis de testosterona e LH, e na composição da microbiota intestinal. A atividade antioxidante também foi verificada, mostrando aumento dos níveis das enzimas GSH, SOD e CAT, e redução de MDA. Além disso, o tratamento evitou a modificação morfológica do ovário, provocada pela SOP. A tolerância à glicose e os níveis de insulina apresentaram melhora em ambas as doses avaliadas, além do aumento dos níveis de PGC-1α e SIRT1 que são baixas na SOP. A redução dose dependente dos níveis das enzimas esteroidogênicas 3β-hidroxiesteroide desidrogenase (3β-HSD) e 17β-hidroxiesteroide desidrogenase (17β-HSD) também foi observada, bem como, a diminuição dos níveis dos marcadores pró-inflamatórios/inflamatórios TNF-α e IL-6.
Em outro estudo pré-clínico utilizando ratas induzidas a SOP com Letrozol e célula granulosa humana, Narigenina teve efeito avaliado na saúde ovariana, nos folículos, nos corpos lúteos, nos níveis séricos de andrógenos e sensibilidade a glicose. No ensaio in vivo os animais foram divididos em cinco grupos (n= 5 a 6 para cada grupo): Grupo 1: controle (óleo de milho), Grupo 2: Letrozol (Dose: 1 mg/kg/dia), Grupo 3: Metformina (Dose: 300 mg/kg/dia); Grupo 4: Narigenina (Dose: 50 mg/kg/dia) e Grupo 5: Metformina (Dose: 300 mg/kg/dia)+ Narigenina (Dose: 50 mg/kg/dia). Já no ensaio in vitro foi utilizada apenas Narigenina (concentração: 2,5 µM) ou em associação com Metformina (concentração: 1 mM). Na análise histológica do ovário foi observada a diminuição de cistos foliculares melhorando o potencial ovulatório e o número de corpos lúteos, redução nos níveis de andrógenos. Na terapia combinada de Narigenina com Metformina foi observada a regulação dos níveis de glicose basal e pós-prandial ao normal, por efeito aditivo do composto com o fármaco. Além disso, foi observada melhora na resposta da insulina, com regulação positiva de pAKT após tratamento com Narigenina. Um aumento na expressão da CYP19A1 (aromatase) devido ao tratamento com o composto foi observado, o que possivelmente favorece a conversão de esteróides/andrógenos C19 em estrogênios para ajudar a restaurar a esteroidogênese normal. Já o nível de expressão de 3β-HSD2 foi restaurado no ovário de ratas com SOP e células ovarianas humana47.
Quercetina
A Quercetina (FIGURA 10) é um flavonoide descrito na literatura com atividade anticâncer, antidiabética, anti-inflamatória, antioxidante e hipolipemiante48.
Em 2021, Mihanfar e colaboradores49 demonstraram em ensaio pré-clínico o efeito da Quercetina em ratas induzidas a SOP com Letrozol (Dose: 1 mg/kg). Os animais foram divididos em três grupos (n= 6 para cada grupo): Grupo 1: controle, Grupo 2: animais com SOP não tratados e Grupo 3: tratados com Quercetina (Dose: 100 mg/kg por 30 dias). Em relação à avaliação do peso, corporal, ovariano e uterino, o composto causou a reversão das alterações do peso uterino causado pelo Letrozol, já para o peso corporal e ovariano não houve diferença estatisticamente significante após o tratamento. O tratamento com Quercetina normalizou o ciclo estral, além de reverter alterações histológicas ovarianas causadas pela SOP. A avaliação do perfil lipídico considerou os níveis de colesterol, TG, LDL-C e HDL-C, parâmetros que foram alterados nos animais com SOP, porém normalizados após tratamento com Quercetina. Outro parâmetro bioquímico avaliado foi o nível de glicose, que apresentou um decréscimo nos animais tratados com reversão da resistência à insulina. Alteração hormonal também foi observada nos animais com SOP, sendo que após o tratamento os níveis de testosterona, estradiol, progesterona, adiponectina, resistina, e visfatina foram regulados quando comparado com o grupo controle. Os níveis de expressão de p-AMPK e SIRT-1 foram mensurados, mostrando que Quercetina regulou alteração causada pela SOP.
Outro ensaio pré-clínico realizado para Quercetina utilizou ratas divididas em seis grupos (n= 7 para cada grupo) sendo os três últimos com ratas induzidas a SOP com DHEA: Grupo 1: controle salina, Grupo 2: Metformina (Dose: 25 mg/kg), Grupo 3: Quercetina (Dose: 25 mg/kg), Grupo 4: sem tratamento, Grupo 5: Metformina (Dose: 25 mg/kg), Grupo 6: Quercetina (Dose: 25 mg/kg), sendo a administração realizada por via oral; durante 28 dias. Os resultados mostraram redução do peso corporal e do nível de testosterona, aumento dos níveis estrogênicos e do peso ovariano, otimizando o ciclo estral, funções do eixo hipotálamo-hipófise-ovário regulando nível de LH e da razão LH/FSH, além da redução da síntese da proteína Bax e da razão Bax/Bcl-2, em comparação com Grupo 4, com SOP e não tratado50.
A redução da resistência insulínica no tratamento com Quercetina foi observada por Zheng e colaboradores51, em ratas induzidas a SOP por DHEA (Dose: 6 mg/kg). Os animais foram divididos em três grupos (n= 30 para cada grupo): Grupo 1: DHEA, Grupo 2: controle positivo com Metformina (Dose: 100 mg/kg/dia) e Grupo 3: Quercetina (Dose: 100 mg/kg/dia), a administração foi por gavagem por 28 dias. Verificou-se também que o composto atua diminuindo a expressão de citocinas inflamatórias como IL-1b, IL-6 e TNF-α, o mecanismo proposto tem relação com a expressão de genes relacionados aos receptores CNP/NPR2, que são responsáveis por regular a ovulação. Os animais tratados com Quercetina afetaram positivamente a transcrição levando a efeitos restauradores da ovulação, com regulação dos níveis de testosterona, estrogênio, LH, razão LH/FSH e Bax.
Quercitrina
O flavonoide Quercitrina (FIGURA 11) é a Quercetina na forma O-glicosilada, ambos encontrados amplamente em flores, folhas e frutos de várias espécies vegetais. Esses compostos têm sido descritos com efeito anticancerígeno, antifibrose, anti-inflamatório e antioxidante52.
Em pesquisa realizada por Li e colaboradores53, foi avaliada a associação da Quercitrina com a via PI3K-Akt na SOP-RI (Síndrome do Ovário Policístico associada à Resistência Insulínica), via relevante no metabolismo da glicose, in vivo utilizando ratas induzidas a SOP com Letrozol e in vitro com linhagem celular de fibroblasto 3T3-L1. No estudo in vivo com duração de 21 dias, os animais foram divididos em seis grupos (n= 8 para cada grupo): Grupo 1: controle, Grupo 2: com SOP, Grupo 3: Diane-35 (Dose: 0,2 mg/kg/dia acetato de cicloproterona + 3,5 μg/kg/dia etinilestradiol) em associação com metformina (Dose: 50 mg/kg/dia), Grupo 4: Quercitrina (Dose: 12,5 mg/kg/dia), Grupo 5: Quercitrina (Dose: 25 mg/kg/dia) e Grupo 6: Quercitrina (Dose: 25 mg/kg/dia). Os resultados in vivo mostraram que, nos animais tratados com Quercitrina, as camadas de células da granulosa ficaram mais finas e foram revertidos os distúrbios morfológicos melhorando a função ovariana, além da redução do peso corporal normalizando os níveis de colesterol total e triglicerídeos e inibindo a diferenciação e acúmulo lipídico em adipócitos maduros reduzindo a resistência insulínica. Os níveis hormonais também foram regulados pela substância, as ratas do grupo de intervenção demonstraram diminuição da razão LH/FSH. O efeito da Quercitrina na resistência insulínica pode ser explicado a partir da ação desse composto na atividade da via PI3K/AKT, afetando assim a função endócrina reprodutiva nos animais. Por sua vez, o estudo in vitro foi realizado com a linhagem celular 3T3-L1 induzida à maturação em tecido adiposo. No tecido adiposo maturado a Quercitrina foi testada, as células dispostas à intervenção mostraram um aumento no apoptose dos adipócitos, esse resultado indica que o composto em questão possui efeito relacionado com a diminuição da resistência à insulina, tendo em vista que este tecido desempenha um papel crucial na via de sinalização PI3K/AKT e está envolvido na fisiopatologia da SOP e da resistência insulínica. A Quercitrina, nesse contexto pode ter atuado aumentando a atividade da via supracitada.
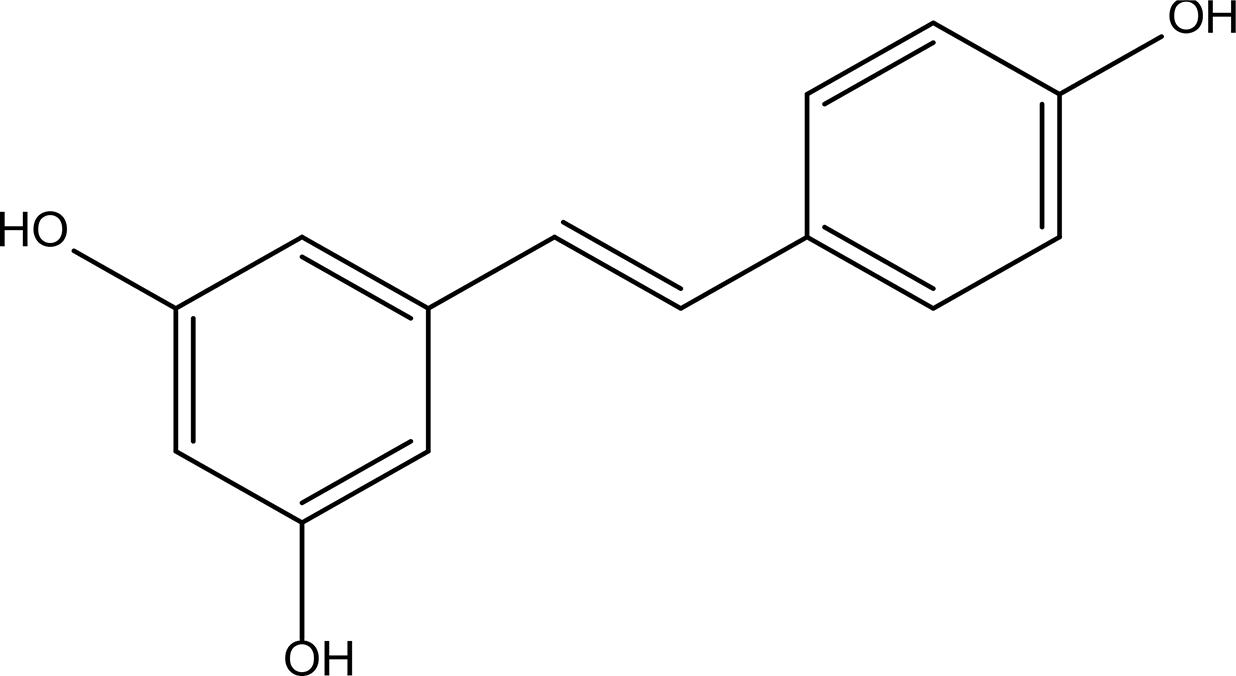
Resveratrol
O Resveratrol (FIGURA 12) é um polifenol natural de espécies vegetais, encontrado em uvas, vinho tinto e amendoim54. Pesquisas têm evidenciado vários efeitos biológicos para o Resveratrol, incluindo ação antioxidante, anti-inflamatória e antitrombótica55,56.
Pesquisa de fase clínica avaliou o composto em mulheres com SOP, em estudo randomizado duplo cego, divididas em dois grupos (n= 39 em cada grupo). Um grupo recebeu placebo, enquanto o outro grupo cápsulas de Resveratrol (Dose: 1000 mg/dia) via oral. Como resultados do consumo de Resveratrol por três meses de tratamento foram melhorias na regulação do ciclo menstrual e diminuição da queda de cabelo. No entanto, não foram verificadas alterações relevantes na perda de peso, na normalização de hormônios andrógenos como testosterona e no metabolismo de carboidratos e lipídeos57.
Na pesquisa pré-clínica realizada por Chen e colaboradores58, as ratas foram divididas em quatro grupos: Grupo 1: controle (n= 13), Grupo 2: Tributilestanho (Dose: 100 ng/kg/dia, n= 18), Grupo 3: Tributilestanho (Dose: 100 ng/kg/dia) + Resveratrol (Dose: 20 mg/kg/dia, n= 14) e Grupo 4: Resveratrol (Dose: 20 mg/kg/dia, n= 12). O Tributilestanho foi utilizado para induzir a SOP. Como resultado foi observada a diminuição de LH, AMH e estradiol, no entanto, não houve alterações na testosterona, progesterona e FSH. Entre os mecanismos que podem estar envolvido na diminuição dos fatores supracitados está o que afirma que o composto atua recuperando os danos na zona de contato (projeções transzonais) entre as células envolvidas na patogênese da SOP como as células da teca e os oócitos otimizando a comunicação celular destas, isso ocorre, pois o Resveratrol aumenta a entrada de cálcio na célula, pela ativação da calmodulina, fosforilando a CaMKIIβ, melhorando a falha ovariana, recuperando os ciclos estrais. Além disso, a ruptura das projeções transzonais e a regulação positiva de CaMKIIβ também foram observadas em amostras de pacientes com SOP.
Em 2023, Liang e colaboradores59 avaliaram Resveratrol (Dose: 1, 10 e 100 µM; por 4 h) em ensaio in vitro em célula granulosa ovariana coletada de mulheres inférteis, portadoras de SOP. O grupo que recebeu o tratamento com Resveratrol foi comparado com o grupo controle (DMSO 0,1%) e grupo modelo (500 µM de H2O2). As células foram induzidas a apoptose por H2O2, modelo comum para a produção de estresse oxidativo. O Resveratrol reduziu significativamente a ocorrência de apoptose nas concentrações de 1 e 10 µM. Em avaliação mais detalhada foi verificado o nível das proteínas TGF-β, Bax e caspase 9 sendo observada diminuição, e para Bcl-2 um aumentado, enquanto os níveis de proteína de caspase 8, caspase 3, fator de diferenciação de crescimento 9 (GDF9) e a proteína morfogenética óssea 15 (BMP15) não expressou diferença significativa, em ensaio com western blot.
Terpenos
Nerolidol
O Nerolidol (FIGURA 13) é um composto sesquiterpênico com diversas atividades farmacológicas descritas como anti-inflamatório, antinociceptiva, antioxidante, neuroprotetora, antiúlcera, anti-leishmania, anti-schistosoma, antimalárica, antimicrobiana, antibiofilme, e anticâncer60-62.
O Nerolidol foi avaliado em ratas com SOP induzida com DHEA por Türkmen e colaboradores63, em quatro grupos (n= 8 para cada grupo): Grupo 1: controle, Grupo 2: SOP, Grupo 3: SOP tratada com Nerolidol (Dose: 100 mg/kg/dia) e Grupo 4: Nerolidol (Dose: 100 mg/kg/dia), via oral durante 21 dias. A avaliação dos níveis hormonais mostrou que o composto diminuiu os níveis de testosterona e LH e aumentou o de FSH. A atividade anti-inflamatória foi demonstrada pela diminuição da expressão de IL-1β, IL-6 e TNF-α. A diminuição do apoptose celular foi relacionada à redução da expressão dos genes Bax e P53. Morfologicamente, o grupo tratado com Nerolidol apresentou diminuição da congestão vascular dos folículos atrésicos. Além disso, foi constatada melhora dos sintomas histopatológicos, como edema, sangramento e folículos degenerativos desencadeados pela SOP. Os resultados do estudo sugerem que o Nerolidol pode ser benéfico em doenças metabólicas como a SOP, onde a inflamação, o estresse oxidativo e a apoptose de células uterinas são a base.
Demais compostos
Salidrosídeo
O composto Salidrosídeo (FIGURA 14) é um fenilpropanoide glicosídico extraído das raízes da espécie Rhodiola rosea L. (Crassulaceae), conhecido pelas propriedades antioxidantes, com estudos mostrando sua ação na redução da lesão causada pelo estresse oxidativo no sistema cardiovascular, doenças endócrinas e neurodegenerativas64-66.
Ji e colaboradores67 avaliaram o Salidrosídeo em ensaio in vitro utilizando linhagem celular KGN (granulosa) tratadas com 500 nM de dihidrotestosterona (DHT), em modelo que vem sendo empregado em estudos envolvendo a SOP. Os ensaios foram realizados com n= 3 ou n= 9, a depender do parâmetro avaliado. Como resultado a viabilidade celular, verificada em 24 e 48 h de tratamento, mostrou que a máxima concentração segura do composto é de 100 µM, não tendo sido verificado efeitos adversos. Assim, a concentração de 100 µM foi empregada para avaliação do efeito no estresse oxidativo, juntamente com uma concentração mais baixa de 30 µM. No tratamento com Salidrosídeo ocorreu melhora da atividade de enzimas superoxido dismutase (SOD) e glutationa peroxidase (GPx), que havia sido diminuída no tratamento com DHT para a indução da SOP, com regulação da atividade antioxidante e eliminação de radicais livres. Ainda, o aumento dos níveis de malondialdeído (MDA) foi revertido após tratamento com Salidrosídeo, indicando que esse composto pode amenizar o estresse oxidativo em células KGN induzidas a SOP. A ativação da expressão de nuclear factor erythroid 2-related factor 2 (Nrf2) que regula genes antioxidantes também foi verificado, sendo o primeiro estudo a demonstrar que Salidrosídeo pode amenizar a apoptose e estresse oxidativo por esta via, mediada por AMPK.
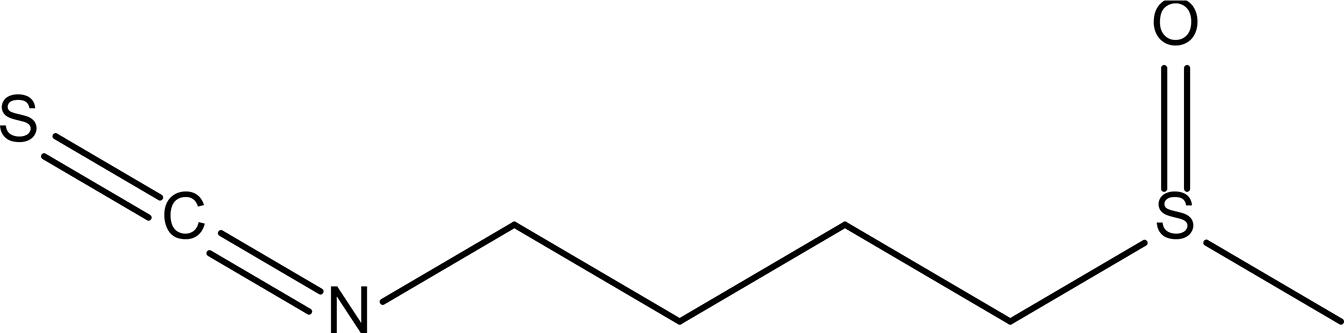
Sulforafano
O Sulforafano (FIGURA 15) é um isotiocianato natural encontrado em vegetais do gênero Brassica L. (Brassicaceae), com propriedade imunorreguladora, antitumoral e antioxidante68.
Em 2021, Taheri e colaboradores69 investigaram o potencial efeito protetor de Sulforafano (Dose: 10 µM; 24 h) contra a produção de ERO e apoptose de células da granulosa pela ativação de genes e proteínas de AMPK/AKT/NRF2. O estudo foi realizado in vitro em células da granulosa coletadas de doze pacientes com SOP, diagnosticadas de acordo com o critério de Rotterdam. Como grupo controle, foram selecionadas nove mulheres sem problemas de fertilidade para a coleta e isolamento das células. O resultado obtido mostrou que o composto pode induzir a expressão de AMPK/AKT/NRF2, tanto em nível genético quanto proteico, verificado em análise por qRT-PCR e western blotting, respectivamente, reduzindo níveis intracelulares de ERO e de apoptose celular das células coletadas de pacientes com SOP quando comparada com o grupo controle. Os resultados obtidos apontam para o potencial uso de Sulforafano no tratamento complementar para pacientes com SOP por meio de administração oral ou durante a maturação in vitro de complexos cumulus-oócito em tecnologia de reprodução assistida.
Porém, estudos in vivo devem ser realizados para definir a concentração a ser utilizada, bem como a segurança do uso.
Predição in silico
Propriedades físico-químicas
Os estudos in silico configuram-se como uma importante ferramenta no processo de desenvolvimento de novos fármacos. Neste trabalho, a análise das propriedades físico-químicas dos metabólitos secundários foi realizada através do servidor on-line SwissADME, com cálculo de descritores físico-químicos que são parâmetros para avaliação da fase farmacocinética5. Foram preditos Peso Molecular (PM), LogP, número aceptores e doadores de ligação de hidrogênio que fazem parte da avaliação da regra de Lipinski, que tem como base perfis físico-químicos de fármacos aprovados nos estudos de fase clínica II. A área superficial topológica (TPSA) e número de ligações rotacionáveis foram considerados para avaliar a regra de Veber. A não violação dos parâmetros para estas regras indica que o composto poderá apresentar biodisponibilidade adequada quando administrado por via oral, com potencial de atravessar barreiras biológicas via intestinal e hematoencefálica6;7.
Os resultados obtidos estão disponíveis na TABELA 1, juntamente com os valores de referência. A partir dos valores tabelados foi possível verificar que apenas dois compostos (Icariina e Quercitrina) violam as regras de Lipinski e Veber, correspondendo a 14,3% dos compostos avaliados. Estes compartilham como característica em comum serem compostos fenólicos, classe que quando glicosilada apresenta peso molecular elevado, dificultando a adequação da molécula nos parâmetros de Drug-likeness avaliado. Para os demais compostos avaliados (85,7%) os resultados favoráveis para as regras avaliadas, apontam para adequada biodisponibilidade para administração por oral.
Quanto aos compostos que violaram as regras, cabe mencionar novas considerações, em artigo publicado por Lipinski70 em 2016, para compostos de origem vegetal quando submetidos sua avaliação na regra dos cinco. Neste artigo, Lipinski considera que a complexidade de uma molécula de origem vegetal traz consigo uma maior eficiência em atingir objetivos biológicos devido a fatores como evolução natural, a flexibilidade conformacional e as ligações intramoleculares. Sendo que algumas estruturas químicas oriundas de produtos naturais geralmente são exceções à regra dos cinco de Lipinski, visto que, apesar de violarem a regra, estas ainda são favoráveis a absorção oral, devido as suas especificidades de auto-modulação e propriedades biofísicas relacionadas à penetração em membranas e alvos devido a diversidade estrutural e seletividade biológica. Além disso, considerando que metabólitos secundários são majoritariamente estruturas cíclicas, o que facilita à permeabilidade nas membranas celulares. A consideração destas características é relevante na prospecção de produtos naturais de origem vegetal como fonte de fármacos, para que mesmo em casos que violem as regras avaliadas, não tenham seus estudos descontinuados, mas tal resultado sirva apenas como um ponto de atenção na aplicação da administração por via oral.
Predição da toxicidade
Avaliar a segurança dos compostos no desenvolvimento de pesquisa por novos fármacos é etapa crucial tanto quanto comprovação da atividade farmacológica, uma vez que mesmo que o composto provenha de fonte natural este pode produzir efeitos tóxicos e até mesmo letais para o paciente. Neste sentido, foi realizada a predição de dose letal 50 (DL50) para administração por via oral dos compostos, seguida da classificação de toxicidade, utilizando o software ProTox. Os resultados obtidos estão disponíveis na Tabela 2. Dentre os compostos avaliados, seis (42,8%) apresentaram valores de DL50 na faixa 2260-5000 mg/kg classificando-os na classe V, cinco (35,7%) apresentaram valores de DL50 na faixa 1000-2000 mg/kg classificando-os na classe IV e três (21,4%) apresentaram valores de DL50 na faixa 159-200 mg/kg sendo classificados na classe III. Os dados podem inferir que a maioria dos compostos das classes IV e V possuem baixa toxicidade, sendo apenas os compostos Berberina, Fisetina e Quercetina, classificados na classe III, o que indica maior probabilidade de toxicidade se ingerido.
Em relação ao alcaloide Berberina, apesar do uso em produtos farmacêuticos há uma escassez acerca de pesquisas que avaliem a sua toxicidade. Estudos in vivo (ratos) afirmam que, apesar de ter uma ampla faixa de segurança, em uso repetitivo e cumulativo foi observado possível o aumento da sua concentração no plasma com potencial tóxico. Uma das consequências dessa toxicidade seria a hipoglicemia causada pela inibição da via gliconeogênica71.
Já para a Quercetina e a Fisetina, quando avaliada a toxicidade em ensaio in vivo por via oral, mostraram efeito fotocarcinogênicos com aumento da chance de efeitos adversos mutagênicos pela indução da radiação ultravioleta em ratos. No entanto, não há evidências de risco quanto ao uso em humanos72.
Além disso, os principais fármacos utilizados no tratamento da SOP, Espironolactona, Inositol e Metformina, também foram avaliados, tendo sido classificados nas classes IV, VI e IV, respectivamente, indicando que a maioria dos compostos em fase de estudos pré-clínicos e clínicos, apresenta a mesma classificação de segurança ou são mais seguros que os medicamentos disponíveis no mercado.
No ProTox também é possível realizar a predição da ação tóxica de compostos em alvos biológicos específicos. A análise é baseada no conjunto de dados do Tox21 (Toxicology in the 21st Century), que é uma biblioteca contendo dados relacionados ao potencial de toxicidade de cerca de dez mil compostos. É possível obter predições de respostas tóxicas de compostos visualizando se estes têm a capacidade de interrupção de vias biológicas8;73.
Nesse contexto, com base na fisiopatologia e principais alvos da SOP, foram considerados na análise os receptores nucleares, andrógeno e estrogênio, e a enzima aromatase. A predição destes parâmetros é relevante para analisar se a toxicidade ocorre no alvo ou fora do alvo farmacológico. Os resultados obtidos pelo ProTox para cada interação toxicológica nos alvos moleculares são dados como ativo, quando o composto interage de forma tóxica, ou inativo, quando o composto não interage de forma tóxica, e a respectiva probabilidade de ocorrer cada resultado. Os escores de probabilidade são uma estimativa de confiabilidade do resultado, em que se os resultados maiores que 0,7 há uma maior probabilidade de ocorrer a interação tóxica8.
A TABELA 2 apresenta os resultados encontrados para avaliação dos compostos quanto aos efeitos tóxicos nos alvos mencionados: aromatase, receptor andrógeno e receptor de estrogênio. Foi verificado que para a enzima aromatase 6,6% dos compostos são ativos no alvo, sendo a maioria inativo, com apenas a Biochanina A predita com atividade tóxica.
Para os receptores andrógenos o Resveratrol foi ativo (correspondendo a 6,6%), os demais não tiveram atividade tóxica no alvo. Por sua vez, o receptor estrógeno foi o que teve maior número de compostos com atividade tóxica, com 40%: Biochanina A, Curcumina, Fisetina, Narigenina, Quercetina e Resveratrol. Nesse cenário, ressalta-se que, apesar da Curcumina e Fisetina serem ativos a probabilidade de interação tóxica é menor que 0,7, o que é positivo tendo em vista o menor do risco de toxicidade.
Na comparação feita com os resultados para os metabólitos secundários avaliados com os principais medicamentos para tratar a SOP, a Metformina e o Inositol, que tem alvos farmacológicos voltados para a resistência insulínica, e não em receptores das células ovarianas, demonstraram ser inativos nos alvos avaliados, não apresentando ação tóxica nos alvos relacionados à SOP. Apenas a Espironolactona demonstrou atividade de interação tóxica com a aromatase e receptor andrógeno, indicando a importância da busca de novos fármacos que não tenham esse potencial tóxico.
Conclusão
A revisão sistemática realizada evidenciou o significativo potencial terapêutico dos metabólitos secundários no tratamento da SOP, sendo que os mais frequentes nos estudos analisados pertencem à classe dos compostos fenólicos, especialmente flavonoides. A avaliação desses compostos, em ensaios de fase pré-clínica (20 artigos) e clínica (4 artigos), apresentou em geral desfechos positivos, como a regulação de hormônios como testosterona, FSH e LH, a redução da resistência insulínica, da inflamação crônica, do estresse oxidativo e de parâmetros lipídicos. Nos resultados das análises in silico, apenas a Icariina e a Quercitrina violaram as regras de Lipinski e Veber, demostrando que a maior parte dos metabólitos avaliados pode apresentar adequada biodisponibilidade oral. Com relação à predição da toxicidade, apenas Berberina, Fisetina e Quercetina foram incluídas na classe III, com baixas concentrações para atingir DL50, no entanto, não há evidência da toxicidade em estudos em humanos. Quanto aos alvos farmacológicos, a maior probabilidade de atividade tóxica foi verificada para o receptor de estrógeno, sendo que a ocorrência da atividade tóxica para a aromatase e receptor androgênico foi baixa. Assim, a busca por fármacos para a SOP tendo como fonte compostos oriundos de espécies vegetais pode ser uma alternativa em pesquisas que visam propor um tratamento frente à complexa sintomatologia causada pela doença.
Referências
- 1 Vilar L. Endocrinologia Clínica. 7 th ed. 2021. 6ª ed. Rio de Janeiro: Guanabara Koogan, 2021. ISBN: 978-85-277-3032-7.
- 2 Mitra S, Saharia, GK, Jena SK. Cardio-metabolic risk in Rotterdam clinical phenotypes of PCOS. Ann Endocrinol. 2024; 85(1): 44-7. ISSN: 0003-4266. [ https://doi.org/10.1016/j.ando.2023.06.001 ].
» https://doi.org/10.1016/j.ando.2023.06.001 - 3 Escobar-Moreale HF. Polycystic ovary syndrome: definition, aetiology, diagnosis and treatment. Nat Rev Endocrinol. 2018; 14(5): 270-84. ISSN: 1759-5037. [ https://doi.org/10.1038/nrendo.2018.24 ].
» https://doi.org/10.1038/nrendo.2018.24 - 4 Azziz R. Polycystic ovary syndrome. Obst Gynec. 2018; 132(1): 321-36. ISSN: 0029-7844. [ https://doi.org/10.1097/AOG.0000000000002698 ].
» https://doi.org/10.1097/AOG.0000000000002698 - 5 Daina A, Michielin O, Zoete V. SwissADME: a free web tool to evaluate pharmacokinetics, drug-likeness and medicinal chemistry friendliness of small molecules. Sci Rep. 2017; 7(42717):. ISSN: 2045-2322. [ https://doi.org/10.1038/srep42717 ].
» https://doi.org/10.1038/srep42717 - 6 Lipinski CA, Lombardo F, Dominy BW, Feeney PJ. Experimental and computational approaches to estimate solubility and permeability in drug discovery and development settings. Adv Drug Deli Rev. 1997; 23(1-3): 3-25. ISSN: 0169-409X. [ https://doi.org/10.1016/S0169-409X (96)00423-1].
» https://doi.org/10.1016/S0169-409X (96)00423-1 - 7 Veber DF, Johnson SR, Cheng HY, Smith BR, Ward KW, Kopple KD. Molecular properties that influence the oral bioavailability of drug candidates. J Med Chem. 2002; 45(12): 2615-23. ISSN: 0022-2623. [ https://doi.org/10.1021/jm020017n ]
» https://doi.org/10.1021/jm020017n - 8 Banerjee P , Kemmler E , Dunkel M , Preissner R . ProTox 3.0: a webserver for the prediction of toxicity of chemicals. Nucl Acid Res. 2024; 52 (W1): W513-20. ISSN: 1362-4962. [ https://doi.org/10.1093/nar/gkae303 ].
» https://doi.org/10.1093/nar/gkae303 - 9 PCASRM: Practice Committee of the American Society for Reproductive Medicine. Role of metformin for ovulation induction in infertile patients with polycystic ovary syndrome (PCOS): a guideline. Fertil Steril. 2017; 108(3): 426-41. ISSN: 0015-0282. [ https://doi.org/10.1016/j.fertnstert.2017.06.026 ].
» https://doi.org/10.1016/j.fertnstert.2017.06.026 - 10 Cena H , Chiovato L , Nappi RE . Obesity, polycystic ovary syndrome, and infertility: a new avenue for GLP-1 receptor agonists. J Clin Endocrin Metab. 2020; 105(8): e2695-e2709. ISSN: 1945-7197. [ https://doi.org/10.1210/clinem/dgaa285 ].
» https://doi.org/10.1210/clinem/dgaa285 - 11 Jung W , Choi H , Kim J , Kim J , Kim W , Nurkolis F , et al . Effects of natural products on polycystic ovary syndrome: From traditional medicine to modern drug discovery. Heliyon. 2023; 9(10): e20889. ISSN: 2405-8440. [ https://doi.org/10.1016/j.heliyon.2023.e20889 ].
» https://doi.org/10.1016/j.heliyon.2023.e20889 - 12 Choi JH, Jang M, Kim EJ, Lee MJ, Park KS, Kim SH, et al. Korean Red Ginseng alleviates dehydroepiandrosterone-induced polycystic ovarian syndrome in rats via its anti-inflammatory and antioxidant activities. J Ginseng Res. 2020; 44(6): 790-8. ISSN: e2093-4947. [ https://doi.org/10.1016/j.jgr.2019.08.007 ].
» https://doi.org/10.1016/j.jgr.2019.08.007 - 13 Zhang Y, Guo X, Ma S, Ma H, Li H, Wang Y, et al. The treatment with complementary and alternative traditional Chinese medicine for menstrual disorders with polycystic ovary syndrome. Evid Based Complement Alternat Med. 2021; 2021(6678398): 1-19. ISSN: 1741-4288. [ https://doi.org/10.1155/2021/6678398 ].
» https://doi.org/10.1155/2021/6678398 - 14 Moreno NT, Santos L, Udulutsch RG. Etnobotânica aliada à saúde da mulher no SUS: um estudo com a Comunidade Tradicional Caiçara do Sertão do Ubatumirim/Ubatuba/SP. Rev Fitos. 2024; 18(1): e1533. e-ISSN: 2446-4775. [ https://doi.org/10.32712/2446-4775.2024.1533 ].
» https://doi.org/10.32712/2446-4775.2024.1533 - 15 Iervolino M, Lepore E, Forte G, Laganà AS, Buzzaccarini G, Unfer V. Natural molecules in the management of polycystic ovary syndrome (PCOS): an analytical review. Nutrients. 2021; 13(5): 1-12. ISSN: 2072-6643. [ https://doi.org/10.3390/nu13051677 ].
» https://doi.org/10.3390/nu13051677 - 16 Wu J , Li J , Li W , Sun B , Xie J , Cheng W , et al . Achyranthis bidentatae radix enhanced articular distribution and anti-inflammatory effect of berberine in Sanmiao Wan using an acute gouty arthritis rat model. J Ethnopharmacol. 2018; 221: 100-8. ISSN: 0378-8741. [ https://doi.org/10.1016/j.jep.2018.04.025 ].
» https://doi.org/10.1016/j.jep.2018.04.025 - 17 Jin F, Xie T, Huang X, Zhao X. Berberine inhibits angiogenesis in glioblastoma xenografts by targeting the VEGFR2/ERK pathway. Pharm Biol. 2018; 56(1): 665-71. ISSN: 1388-0209. [ https://doi.org/10.1080/13880209.2018.1548627 ].
» https://doi.org/10.1080/13880209.2018.1548627 - 18 Zhang N, Liu X, Zhuang L, Liu X, Zhao H, Shan Y, et al. Berberine decreases insulin resistance in a PCOS rats by improving GLUT4: dual regulation of the PI3K/AKT and MAPK pathways. Regul Tox and Pharm. 2020; 110(104544): 1-6. ISSN: 0273-2300. [ https://doi.org/10.1016/j.yrtph.2019.104544 ].
» https://doi.org/10.1016/j.yrtph.2019.104544 - 19 Fernandes FHA, Salgado HRN. Gallic Acid: Review of the Methods of Determination and Quantification. Crit Rev Anal Chem. 2016; 46(3): 257-65. ISSN: 1547-6510. [ https://doi.org/10.1080/10408347.2015.1095064 ].
» https://doi.org/10.1080/10408347.2015.1095064 - 20 Choubey S, Varughese LR, Kumar V, Beniwal V. Medicinal importance of gallic acid and its ester derivatives: a patent review. Pharm Pat Anal. 2015; 4(4): 305-15. ISSN: 2046-8954. [ https://doi.org/10.4155/ppa.15.14 ].
» https://doi.org/10.4155/ppa.15.14 - 21 Shah MZH, Soni M, Shrivastava VK, Mir MA, Muzamil S. Gallic acid reverses ovarian disturbances in mice with letrozole-induced PCOS via modulating Adipo R1 expression. Tox Rep. 2022; 9(2022): 1938-49. ISSN: 2214-7500. [ https://doi.org/10.1016/j.toxrep.2022.10.009 ].
» https://doi.org/10.1016/j.toxrep.2022.10.009 - 22 Patisaul HB, Jefferson W. The pros and cons of phytoestrogens. Front Neuroendocrinol. 2010; 31(4): 400-19. ISSN: 0091-3022. [ https://doi.org/10.1016/j.yfrne.2010.03.003 ].
» https://doi.org/10.1016/j.yfrne.2010.03.003 - 23 Kim IS . Current perspectives on the beneficial effects of soybean isoflavones and their metabolites for humans. Antioxidants. 2021; 10(7): 1064. ISSN: 2076-3921. [ https://doi.org/10.3390/antiox10071064 ].
» https://doi.org/10.3390/antiox10071064 - 24 Kotipalli RSS, Patnaik SS, Kumar JM, Ramakrishna S, Muralidharan K. Biochanin-A attenuates DHEA-induced polycystic ovary syndrome via upregulation of GDF9 and BMP15 signaling in vivo. Life Sci. 2023; 326(121795): 1-12. ISSN: 0024-3205. [ https://doi.org/10.1016/j.lfs.2023.121795 ].
» https://doi.org/10.1016/j.lfs.2023.121795 - 25 Choi SH, Shapiro H, Robinson GE, Irvine J, Neuman J, Rosen B, et al. Psychological side-effects of clomiphene citrate and human menopausal gonadotrophin. J Psychosom. Obstet Gynaecol. 2005; 26(2): 93-100. ISSN: 1743-8942. [ https://doi.org/10.1080/01443610400022983 ].
» https://doi.org/10.1080/01443610400022983 - 26 Arun N, Nalini N. Efficacy of turmeric on blood sugar and polyol pathway in diabetic albino rats. Plant Foods Hum Nutr. 2002; 57(1): 41-52. ISSN: 0921-9668. [ https://doi.org/10.1023/a:1013106527829 ].
» https://doi.org/10.1023/a:1013106527829 - 27 Pari L, Murugan P. Effect of tetrahydrocurcumin on blood glucose, plasma insulin and hepatic key enzymes in streptozotocin induced diabetic rats. J Basic Clin Physiol Pharmacol. 2005; 16(4): 257-74. ISSN: 2191-0286. [ https://doi.org/10.1515/jbcpp.2005.16.4.257 ].
» https://doi.org/10.1515/jbcpp.2005.16.4.257 - 28 Abuelezz NZ , Shabana ME , Abdel-Mageed HM , Rashed L , Morcos GN . Nanocurcumin alleviates insulin resistance and pancreatic deficits in polycystic ovary syndrome rats: Insights on PI3K/AkT/mTOR and TNF-a modulations. Life Sci. 2020; 256(118003): 1-11. ISSN: 0024-3205. [ https://doi.org/10.1016/j.lfs.2020.118003 ].
» https://doi.org/10.1016/j.lfs.2020.118003 - 29 Abhari SMF, Khanbabaei R, Roodbari, NH, Parivar K, Yaghmaei P. Curcumin-loaded super-paramagnetic iron oxide nanoparticle affects on apoptotic factors expression and histological changes in a prepubertal mouse model of polycystic ovary syndrome-induced by dehydroepiandrosterone-A molecular and stereological study. Life Sci. 2020; 249(117515): 1-9. ISSN: 0024-3205. [ https://doi.org/10.1016/j.lfs.2020.117515 ].
» https://doi.org/10.1016/j.lfs.2020.117515 - 30 Bari YN, Babapour V, Ahmadi A, Kheybari MZ, Akbari G. The effect of curcumin on embryonic in vitro development in experimental polycystic ovary syndrome: An experimental study. Int J Reprod Biomed. 2021; 19(11): 997-1004. ISSN: 1680-6433. [ https://doi.org/10.18502/ijrm.v19i11.9915 ].
» https://doi.org/10.18502/ijrm.v19i11.9915 - 31 Jamilian M, Foroozanfard F, Kavossian E, Aghadavod E, Shafabakhsh R, Hoseini A, et al. Effects of curcumin on body weight, glycemic control and serum lipids in women with polycystic ovary syndrome: A randomized, double-blind, placebo-controlled trial. Clin nutr ESPEN. 2020; 36(2020): 128-33. ISSN: 2405-4577. [ https://doi.org/10.1016/j.clnesp.2020.01.005 ].
» https://doi.org/10.1016/j.clnesp.2020.01.005 - 32 Heshmati J, Moini A, Sepidarkish M, Morvaridzadeh M, Salehi M, Palmowski A, et al. Effects of curcumin supplementation on blood glucose, insulin resistance and androgens in patients with polycystic ovary syndrome: A randomized double-blind placebo-controlled clinical trial. Phytomed. 2021; 80(153395): 1-7. ISSN: 0944-7113. [ https://doi.org/10.1016/j.phymed.2020.153395 ].
» https://doi.org/10.1016/j.phymed.2020.153395 - 33 Ghanbarzadeh-Ghashti N, Ghanbari-Homaie S, Shaseb E, Abbasalizadeh S, Mirghafourvand M. The effect of Curcumin on metabolic parameters and androgen level in women with polycystic ovary syndrome: a randomized controlled trial. BMC Endoc Disor. 2023; 23(40): 1-10. ISSN: 1472-6823. [ https://doi.org/10.1186/s12902-023-01295-5 ].
» https://doi.org/10.1186/s12902-023-01295-5 - 34 Shi YS, Li CB, Li XY, Wu J, Li Y, Fu X, et al. Fisetin attenuates metabolic dysfunction in mice challenged with a high-fructose diet. J Agric Food Chem. 2018; 66(31): 8291-8. ISSN: 1520-5118. [ https://doi.org/10.1021/acs.jafc.8b02140 ].
» https://doi.org/10.1021/acs.jafc.8b02140 - 35 Prasath GS, Pillai SI, Subramanian SP. Fisetin improves glucose homeostasis through the inhibition of gluconeogenic enzymes in hepatic tissues of streptozotocin induced diabetic rats. Eur J Pharmacol. 2014; 740: 248-54. ISSN: 0014-2999. [ https://doi.org/10.1016/j.ejphar.2014.06.065 ].
» https://doi.org/10.1016/j.ejphar.2014.06.065 - 36 Kim SC, Kim YH, Son SW, Moon EY, Pyo S, Um SH, Fisetin induces Sirt1 expression while inhibiting early adipogenesis in 3T3-L1 cells. Biochem Biophys Res Commun. 2015; 467(4): 638-44. ISSN: 1090-2104. [ https://doi.org/10.1016/j.bbrc.2015.10.094 ].
» https://doi.org/10.1016/j.bbrc.2015.10.094 - 37 Mihanfar A, Nouri M, Roshangar L, Khadem-Ansari MH. Ameliorative effects of fisetin in letrozole-induced rat model of polycystic ovary syndrome. J Steroid Biochem Mol Biol. 2021; 213(105954): 1-10. ISSN: 0960-0760. [ https://doi.org/10.1016/j.jsbmb.2021.105954 ].
» https://doi.org/10.1016/j.jsbmb.2021.105954 - 38 Indran IR, Zhang SJ, Zhang ZW, Sun F, Gong Y, Wang X, et al. Selective estrogen receptor modulator effects of Epimedium extracts on breast cancer and uterine growth in nude mice. Planta Med. 2014; 80(1): 22-8. ISSN: 0032-0943. [ https://doi.org/10.1055/s-0033-1360112 ].
» https://doi.org/10.1055/s-0033-1360112 - 39 Tang Y, Li Y, Xin D, Chen L, Xiong Z, Yu X. Icariin alleviates osteoarthritis by regulating autophagy of chondrocytes by mediating PI3K/AKT/mTOR signaling. Bioengineered. 2021; 12(1): 2984-99. ISSN: 2165-5987. [ https://doi.org/10.1080/21655979.2021.1943602 ].
» https://doi.org/10.1080/21655979.2021.1943602 - 40 He C, Wang, Z, Shi, J. Pharmacological effects of Icariin. Adv Pharmacol. 2020; 87(2020): 179-203. ISSN: 2633-4682. [ https://doi.org/10.1016/bs.apha.2019.10.004 ].
» https://doi.org/10.1016/bs.apha.2019.10.004 - 41 Zuo L , Hai Y , Zhang R , Zuo B , Tian J , Li P , et al . Therapeutic potential of icariin in rats with letrozole and high-fat diet-induced polycystic ovary syndrome. Europ J Pharm. 2023; 953(175825): 1-14. ISSN: 0014-2999. [ https://doi.org/10.1016/j.ejphar.2023.175825 ].
» https://doi.org/10.1016/j.ejphar.2023.175825 - 42 Cui CA, Jin DQ, Hwang YK, Lee IS, Hwang JK, Ha I et al. Macelignan attenuates LPS-induced inflammation and reduces LPS-induced spatial learning impairments in rats. Neurosci Lett. 2008; 448(1): 110-4. ISSN: 0304-3940. [ https://doi.org/10.1016/j.neulet.2008.10.035 ].
» https://doi.org/10.1016/j.neulet.2008.10.035 - 43 Jin DQ, Lim CS, Hwang JK, Ha I, Han JS. Antioxidant and anti-inflammatory activities of macelignan in murine hippocampal cell line and primary culture of rat microglial cells. Biochem. Biophys. Res Commun. 2005; 331(4): 1264-9. ISSN: 0006-291X. [ https://doi.org/10.1016/j.bbrc.2005.04.036 ].
» https://doi.org/10.1016/j.bbrc.2005.04.036 - 44 Shi XJ, Du Y, Chen L, Chen, YY, Luo M, Cheng Y. Treatment of polycystic ovary syndrome and its associated psychiatric symptoms with the Mongolian medicine Nuangong Qiwei Pill and macelignan. J Ethnopharmacol 2023; 317(116812): 1-12. ISSN: 0378-8741. [https://doi.org/10.1016/j.jep.2023.116812].
» https://doi.org/10.1016/j.jep.2023.116812 - 45 Wu YX , Yang XY , Han BS , Hu YY , An T , Lv BH , et al . Naringenin regulates gut microbiota and SIRT1/PGC-1? signaling pathway in rats with letrozole-induced polycystic ovary syndrome. Biomed Pharmacother. 2022; 153(113286). ISSN: 0753-3322. [ https://doi.org/10.1016/j.biopha.2022.113286 ].
» https://doi.org/10.1016/j.biopha.2022.113286 - 46 Dashputre NL, Laddha UD, Patil SB, Kadam JD, Kshirsagar SJ. An insight to development and in-vitro, ex-vivo, in-vivo study of naringenin nanoparticles against letrozole induced polycystic ovarian syndrome in female wistar rats. J Drug Del Sci Tech. 2023; 90(105129): 1-19. ISSN: 1773-2247. [ https://doi.org/10.1016/j.jddst.2023.105129 ].
» https://doi.org/10.1016/j.jddst.2023.105129 - 47 Rashid R , Tripathi R , Singh A , Sarkar S , Kawale A , Bader GN , et al . Naringenin improves ovarian health by reducing the serum androgen and eliminating follicular cysts in letrozole-induced polycystic ovary syndrome in the Sprague Dawley rats. Phytoth Res. 2023; 37(9): 4018-4041. ISSN: 1099-1573. [ https://doi.org/10.1002/ptr.7860 ].
» https://doi.org/10.1002/ptr.7860 - 48 David AVA, Arulmoli R, Parasuraman S. Overviews of biological importance of quercetin: a bioactive flavonoid. Phcog Rev. 2016; 10(20): 84-9. ISSN: 0973-7847. [ https://doi.org/10.4103/0973-7847.194044 ].
» https://doi.org/10.4103/0973-7847.194044 - 49 Mihanfar A, Nouri M, Roshangar L, Khadem-Ansari MH. Therapeutic potential of quercetin in an animal model of PCOS: Possible involvement of AMPK/SIRT-1 axis. Europ J Pharm. 2021; 900(174062): 1-9. ISSN: 0014-2999. [ https://doi.org/10.1016/j.ejphar.2021.174062 ].
» https://doi.org/10.1016/j.ejphar.2021.174062 - 50 Mahmoud AA, Elfiky AM, Abo-Zeid FS. The anti-androgenic effect of quercetin on hyperandrogenism and ovarian dysfunction induced in a dehydroepiandrosterone rat model of polycystic ovary syndrome. Steroids. 2022; 177(108936): 1-12. ISSN: 0039-128X. [ https://doi.org/10.1016/j.steroids.2021.108936 ].
» https://doi.org/10.1016/j.steroids.2021.108936 - 51 Zheng S, Chen Y, Ma M, Li M. Mechanism of quercetin on the improvement of ovulation disorder and regulation of ovarian CNP/NPR2 in PCOS model rats. J Form Med Assoc. 2022; 121(6): 1081-92. ISSN: 0929-6646. [ https://doi.org/10.1016/j.jfma.2021.08.015 ].
» https://doi.org/10.1016/j.jfma.2021.08.015 - 52 Tang J, Diao P, Shu X, Li L, Xiong L. Quercetin and Quercitrin Attenuates the Inflammatory Response and Oxidative Stress in LPS-Induced RAW264.7 Cells: In Vitro Assessment and a Theoretical Model. Biomed Res Int. 2019; 28(7039802): 1-8. ISSN: 2314-6141. [ https://doi.org/10.1155/2019/7039802 ].
» https://doi.org/10.1155/2019/7039802 - 53 Li M, Gao S, Kang M, Zhang X, Lan P, Wu X et al. Quercitrin alleviates lipid metabolism disorder in polycystic ovary syndrome-insulin resistance by upregulating PM20D1 in the PI3K/Akt pathway. Phytomed. 2023; 117(154908): 1-14. ISSN: 0944-7113. [ https://doi.org/10.7150/10.1016/j.phymed.2023.154908 ].
» https://doi.org/10.7150/10.1016/j.phymed.2023.154908 - 54 Ortega I, Duleba AJ. Ovarian actions of resveratrol. Ann N Y Acad Sci. 2015; 1348(1): 86-96. ISSN: 1749-6632. [ https://doi.org/10.1111/nyas.12875 ].
» https://doi.org/10.1111/nyas.12875 - 55 Rege SD, Kumar S, Wilson DN, Tamura L, Geetha T, Mathews ST, et al. Resveratrol protects the brain of obese mice from oxidative damage. Oxid Med Cell Longev. 2013; 2013(429092): 1-7. ISSN: 1942-0994. [ https://doi.org/10.1155/2013/419092 ].
» https://doi.org/10.1155/2013/419092 - 56 Rauf A, Imran M, Suleria HAR, Ahmad B, Peters DG, Mubarak MS. A comprehensive review of the health perspectives of resveratrol. Food Funct. 2017; 13;8(12): 4284-305. ISSN: 2042-650X. [ https://doi.org/10.1039/c7fo01300k ].
» https://doi.org/10.1039/c7fo01300k - 57 Mansour A, Samadi M, Sanginabadi M, Gerami H, Karimi S, Hosseini S, et al. Effect of resveratrol on menstrual cyclicity, hyperandrogenism and metabolic profile in women with PCOS. Clin Nutri. 2021; 40(6): 4106-12. ISSN: 0261-5614. [ https://doi.org/10.1016/j.clnu.2021.02.004 ].
» https://doi.org/10.1016/j.clnu.2021.02.004 - 58 Chen M, He C, Zhu K, Chen Z, Meng Z, Jiang X, et al. Resveratrol ameliorates polycystic ovary syndrome via transzonal projections within oocyte-granulosa cell communication. Theran. 2022; 12(2): 782-95. ISSN: 1838-7640. [ https://doi.org/10.7150/thno.67167 ].
» https://doi.org/10.7150/thno.67167 - 59 Liang Y, Xu ML, Gao X, Wang Y, Zhang LN, Li YC, et al. Resveratrol improves ovarian state by inhibiting apoptosis of granulosa cells. Gynecol Endocr. 2023; 39(1): 1-6. ISSN: 1473-0766. [ https://doi.org/10.1080/09513590.2023.2181652 ].
» https://doi.org/10.1080/09513590.2023.2181652 - 60 Chan WK , Tan LTH , Chan KG , Lee LH , Goh BH . Nerolidol: a sesquiterpene alcohol with multi-faceted pharmacological and biological activities. Molecules. 2016; 21(5): 1-40. ISSN: 1420-3049. [ https://doi.org/10.3390/molecules21050529 ].
» https://doi.org/10.3390/molecules21050529 - 61 Fonsêca DV, Salgado PR, Carvalho FL, Salvadori MGS, Penha ARS, Leite FC, Almeida RN. Nerolidol exhibits antinociceptive and anti-inflammatory activity: involvement of the GABAergic system and proinflammatory cytokines. Fundam Clin Pharmacol. 2015; 30(1): 14-22. ISSN: 0767-3981. [ https://doi.org/10.1111/fcp.12166 ].
» https://doi.org/10.1111/fcp.12166 - 62 Carvalho RB, Almeida AAC, Campelo NB, Lellis DROD, Nunes LCC. Nerolidol and its pharmacological application in treating neurodegenerative diseases: A review. Recent Pat Biotechnol. 2018; 12(3), 158-68. ISSN: 1872-2083. [ https://doi.org/10.2174/1872208312666171206123805 ].
» https://doi.org/10.2174/1872208312666171206123805 - 63 Türkmen NB, Yüce H, Aydin M, Taslidere A, Dogan A, Özek DA, et al. Nerolidol attenuates dehydroepiandrosterone-induced polycystic ovary syndrome in rats by regulating oxidative stress and decreasing apoptosis. Life Sci. 2023; 315(121380): 1-15. ISSN: 0024-3205. [ https://doi.org/10.1016/j.lfs.2023.121380 ].
» https://doi.org/10.1016/j.lfs.2023.121380 - 64 Tang C, Zhao CC, Yi H, Geng ZJ, Wu XY, Zhang Y, et al. Traditional Tibetan medicine in cancer therapy by targeting apoptosis pathways. Front Pharmacol. 2020; 11(976): 1-19. ISSN: 1663-9812. [ https://doi.org/10.3389/fphar.2020.00976 ].
» https://doi.org/10.3389/fphar.2020.00976 - 65 Nabavi SF, Braidy N, Orhan IE, Badiee A, Daglia M, Nabavi SM. Rhodiola rosea L. and alzheimer's disease: from farm to pharmacy. Phytother Res. 2016; 30(4): 532-9. ISSN: 1099-1573. [ https://doi.org/10.1002/ptr.5569 ].
» https://doi.org/10.1002/ptr.5569 - 66 Zheng T, Bian F, Chen L, Wang Q, Jin S. Beneficial effects of Rhodiola and salidroside in diabetes: potential role of AMP-activated protein kinase. Mol Diagn Ther. 2019; 23(4): 489-98. ISSN: 1177-1062. [ https://doi.org/10.1007/s40291-019-00402-4 ].
» https://doi.org/10.1007/s40291-019-00402-4 - 67 Ji R , Jia FY , Chen X , Wang ZH , Jin WY , Yang J . Salidroside alleviates oxidative stress and apoptosis via AMPK/Nrf2 pathway in DHT-induced human granulosa cell line KGN. Arch Biochem Bioph. 2022; 715(109094): 1-13. ISSN: 0003-9861. [ https://doi.org/10.1016/j.abb.2021.109094 ].
» https://doi.org/10.1016/j.abb.2021.109094 - 68 Kubo E, Chhunchha B, Singh P, Sasaki H, Singh DP. Sulforaphane reactivates cellular antioxidant defense by inducing Nrf2/ARE/Prdx6 activity during aging and oxidative stress. Sci Rep. 2017; 7(14130): 1-17. ISSN: 2045-2322. [ http://dx.doi.org/10.1038/s41598-017-14520-8 ].
» http://dx.doi.org/10.1038/s41598-017-14520-8 - 69 Taheri M, Roudbari NH, Amidi F, Parivar K. The protective effect of sulforaphane against oxidative stress in granulosa cells of patients with polycystic ovary syndrome (PCOS) through activation of AMPK/AKT/NRF2 signaling pathway. Reprod Biol. 2021; 21(4): 1-8. ISSN: 1642-431X. [ https://doi.org/10.1016/j.repbio.2021.100563 ].
» https://doi.org/10.1016/j.repbio.2021.100563 - 70 Lipinski CA. Rule of five in 2015 and beyond: Target and ligand structural limitations, ligand chemistry structure and drug discovery project decisions. Adv Drug Deli Rev. 2016; 101: 34-41. ISSN: 0169-409X. [ http://dx.doi.org/10.1016/j.addr.2016.04.029 ].
» http://dx.doi.org/10.1016/j.addr.2016.04.029 - 71 Moreira ES , Ames-Sibin AP , Bonetti CI , Leal LE , Peralta RM , Sá-Nakanishi AB , et al . The short-term effects of berberine in the liver: narrow margins between benefits and toxicity. Tox Letters. 2022; 368: 56-65. ISSN: 0378-4274. [ https://doi.org/10.1016/j.toxlet.2022.08.005 ].
» https://doi.org/10.1016/j.toxlet.2022.08.005 - 72 Pihl C, Granborg JR., Pinto FE, Bjerring P, Andersen F, Janfelt C, et al. Oral administration of quercetin and fisetin potentiates photocarcinogenesis in UVR-exposed hairless mice. Phytomed Plus. 2024; 4(2): 1-8. ISSN: 2667-0313. [ https://doi.org/10.1016/j.phyplu.2024.100547 ].
» https://doi.org/10.1016/j.phyplu.2024.100547 - 73 Huang R, Xia M, Nguyen DT, Zhao T, Sakamuru S, Zhao J, et al. Tox21Challenge to build predictive models of nuclear receptor and stress response pathways as mediated by exposure to environmental chemicals and drugs. Front Environ Sci. 2016; 3(85): 1-9. ISSN: 2296-665X. [ https://doi.org/10.3389/fenvs.2015.00085 ].
» https://doi.org/10.3389/fenvs.2015.00085
-
Fonte de financiamento:
Nenhuma.
Datas de Publicação
- Publicação nesta coleção
12 Mar 2025 - Data do Fascículo
Fev 2025
Histórico
- Recebido
26 Maio 2024 - Aceito
18 Nov 2024
 Síndrome do ovário policístico: revisão sistemática de recentes pesquisas referentes à investigação de metabólitos secundários para o tratamento
Síndrome do ovário policístico: revisão sistemática de recentes pesquisas referentes à investigação de metabólitos secundários para o tratamento