Resumo
Enterococcus faecium apresenta resistência às principais classes de antimicrobianos, sendo essencial a descoberta de novas opções terapêuticas. Um dos mecanismos que promove resistência à ação de antimicrobianos é o biofilme. O objetivo deste estudo foi avaliar a eficácia da Cordia salicifolia Cham (Boraginaceae), uma planta medicinal popular no Brasil, sobre o biofilme de E. faecium. Foram avaliados isolados de E. faecium (n=12) obtidos de pacientes hospitalizados. O perfil de sensibilidade a antimicrobianos foi determinado. A atividade antibacteriana dos extratos aquoso e etanólico, obtidos das folhas e talos da planta, foi avaliada pela determinação da concentração inibitória mínima e a atividade sobre o biofilme foi avaliada pelo método de quantificação de biomassa por cristal violeta, após 24 horas de incubação na presença dos extratos. A maioria dos isolados foi classificada como forte produtora de biofilme (83,3%) e apresentou resistência à vancomicina (91,6%), ampicilina (91,6%), gentamicina (83,3%) e estreptomicina (50%). Não foi observada inibição do crescimento ou do biofilme pelos extratos de C. salicifolia, apesar do uso de concentração igual a dose tóxica para macrófagos. Concluindo, os extratos, aquoso e etanólico de C. salicifolia não apresentam atividade antibacteriana e nem anti-biofilme sobre isolados clínicos de E. faecium.
Palavras-chave Biofilme; Cordia salicifolia; Enterococcus faecium; Plantas medicinais; Vancomicina
Abstract
Enterococcus faecium is resistant to the main classes of antimicrobials, making it essential to discover new therapeutic options. One of the mechanisms that promotes resistance to the action of antimicrobials is biofilm. The objective of this study was to evaluate the effectiveness of Cordia salicifolia Cham (Boraginaceae), a popular medicinal plant in Brazil, on E. faecium biofilm. Isolates of E. faecium (n=12) obtained from hospitalized patients were evaluated. The antimicrobial sensitivity profile was determined. The antibacterial activity of the aqueous and ethanolic extracts, obtained from the leaves and stems of the plant, was evaluated by determining the minimum inhibitory concentration and the activity on the biofilm was evaluated by the biomass quantification method by crystal violet, after 24 hours of incubation in the presence of the extracts. The majority of isolates were classified as strong biofilm producers (83.3%) and showed resistance to vancomycin (91.6%), ampicillin (91.6%), gentamicin (83.3%) and streptomycin (50%). No growth or biofilm inhibition was observed by C. salicifolia extracts, despite the use of a concentration equal to the toxic dose for macrophages. In conclusion, aqueous and ethanolic extracts of C. salicifolia do not present antibacterial or anti-biofilm activity against clinical isolates of E. faecium.
Keywords Biofilm; Cordia salicifolia; Enterococcus faecium; Medicinal plants; Vancomycin
Introdução
O gênero Enterococcus é composto por bactérias com morfologia de cocos e comportamento tintorial Gram-positivo[1]. Entre as espécies desse gênero se destacam Enterococcus faecium, patógeno oportunista que habita comumente o intestino de seres humanos e de outros animais, sendo também encontrado na natureza[1]. Esse microrganismo é um importante agente nosocomial, responsável por 40% das infecções hospitalares causadas por esse gênero[2]. E. faecium tem a capacidade de adaptar-se rapidamente ao ambiente hospitalar e adquirir genes que conferem resistência a diversas classes de antimicrobianos utilizados no tratamento de bactérias Gram-positivas, inclusive aos glicopeptídeos, como vancomicina e teicoplanina[3]. Os fenótipos de E. faecium resistentes à vancomicina (VREfm) são considerados pela Organização Mundial da Saúde (OMS) como um dos agentes prioritários para o qual é imperativo encontrar novas e eficazes estratégias terapêuticas devido à multirresistência desse microrganismo[4,5].
Um dos elementos que também contribuem para a resistência de E. faecium é a capacidade de produção de biofilme, o qual é uma comunidade de microrganismos sésseis ligados a uma superfície biótica ou abiótica e unidos por uma matriz de substâncias poliméricas extracelulares, formando uma estrutura estável e altamente resistente ao sistema imunológico do hospedeiro, bem como aos antimicrobianos, dificultando sua erradicação[6,7].
O aumento de linhagens bacterianas cada vez mais resistentes aos antimicrobianos utilizados na clínica faz com que seja necessário o uso de novos medicamentos. Dentre essas novas possibilidades de agentes antimicrobianos, as substâncias naturais vêm recebendo grande atenção de pesquisadores por facilitarem a adesão dos pacientes ao tratamento[8]. No Brasil, e em outros países da América Latina, já existem programas que monitoram o uso das substâncias naturais pela população, identificando as mais utilizadas e realizando triagem de potenciais atividades antimicrobianas[9]. Essas substâncias naturais podem ser eficazes inclusive contra bactérias multirresistentes, além de apresentarem sinergismos com antimicrobianos[10].
Diversas dessas substâncias naturais já tiveram seu efeito antimicrobiano reportado, como o extrato etanólico da Mikania glomerata, conhecida popularmente como guaco, comercializada com indicação de uso como expectorante e antigripal, e que apresentou atividade antimicrobiana contra E. faecium, Bacillus subtilis e Staphylococcus aureus[9]. Essas substâncias naturais podem atuar também no biofilme, através da ruptura da membrana externa, capacidade de ligação ao complexo adesina-parede celular, interações com DNA e ligação à proteínas[8,11,12], resultando em uma diminuição da resistência aos antimicrobianos[13].
Vários estudos foram realizados com diferentes espécies do gênero Cordia, como a C. exaltata com capacidade antimicrobiana contra Pseudomonas aeruginosa, Escherichia coli e S. aureus[14]. C. dichotoma apresentou atividade antimicrobiana contra Klebsiella pneumoniae[15]. Além da C. verbenacea com atividade antimicrobiana contra bactérias Gram-positivas[16]. No entanto, até a presente data, não há nenhum estudo sobre o potencial antimicrobiano de uma das espécies mais conhecidas e utilizadas desse gênero no Brasil, principalmente nas regiões sul e sudeste, a Cordia salicifolia Cham; 1753 [17], pertencente à família Boraginaceae, popularmente conhecida como cafezinho do mato, Bugre e Porangaba. Essa planta tem sido utilizada principalmente na forma de chás para fins antimicrobianos, anti-inflamatórios, diuréticos e analgésicos[18].
Pelo exposto, o objetivo deste estudo experimental foi avaliar a eficácia dos extratos aquoso e etanólico de C. salicifolia em inibir o crescimento e a capacidade de produção de biofilme de E. faecium.
Material e Métodos
Material Vegetal
O material vegetal de C. salicifolia, composto por folhas e talo, foi obtido comercialmente na empresa Chá & Cia Ervas Medicinais (FIGURA 1), mediante certificação de análise e identificação botânica (número 801/18 R, fornecedor 000466-01, lote do fornecedor 1017).
Extratos aquoso e etanólico de Cordia salicifolia Cham
Os extratos, aquoso e etanólico da C. salicifolia foram obtidos no Laboratório de Farmacologia, da Universidade Federal do Triângulo Mineiro (UFTM). Para a preparação do extrato aquoso, foi utilizado o método de infusão, utilizando-se 10 g de folhas e talos infusionados com 1000 mL de água destilada aquecida, durante 10 minutos, em seguida filtrados e os resíduos sólidos descartados. Por fim, a infusão filtrada foi liofilizada e o extrato seco armazenado. Para a preparação do extrato etanólico, para cada 100 g de folhas e talos foram usados 1000 mL de álcool etílico (99,7%) para cobri-los e depois macerá-los por 15 dias, sendo homogeneizados periodicamente. Em seguida, ele foi filtrado e submetido à evaporação[19].
Isolados de Enterococcus faecium
Este estudo foi realizado no Laboratório de Pesquisa em Microbiologia, do Instituto de Ciências Biológicas e Naturais da UFTM, no período de março a novembro de 2024. Os isolados bacterianos encontravam-se armazenados em caldo Brain Heart Infusion (BHI), com 30% de glicerol, em freezer - 80 °C. Foram selecionados 12 isolados de E. faecium obtidos de diferentes espécimes clínicos de pacientes internados no Hospital de Clínicas da UFTM, entre os anos de 2007 e 2017 (TABELA 1), selecionados por critérios de variabilidade de espécime, gênero, idade e ano de identificação. Foi realizada a confirmação da identificação em espécie através de provas bioquímicas específicas para cocos Gram-positivos, entre as quais se destacam a prova da produção de catalase, prova de tolerância ao Cloreto de sódio 6,5%, teste de PYR, teste de motilidade, fermentação do manitol e fermentação da arabinose, além de provas complementares como a coloração de Gram[20]. Os isolados selecionados neste estudo tiveram o genoma completo sequenciado em parceria realizada previamente.
Avaliação da concentração inibitória mínima de antimicrobianos
O perfil de sensibilidade dos isolados foi analisado pelo método de diluição em caldo seguindo protocolos do Clinical Laboratory Standards Institute (CLSI), a fim de determinar a concentração inibitória mínima (CIM) dos antimicrobianos vancomicinas, ampicilina, gentamicina e estreptomicina[21].
Foram preparadas soluções estoque dos antimicrobianos a serem testados, e realizadas diluições seriadas dessas soluções em caldo Mueller Hinton, em placas de 96 poços de poliestireno. As concentrações dos antimicrobianos vancomicina e ampicilina variaram de 0,5 a 256 µg/mL, gentamicina de 1 a 512 µg/mL e estreptomicina de 1,95 a 1000 µg/mL. Foram preparadas suspensões dos isolados de E. faecium, após descongelamento e cultivo em placas de Petri contendo ágar Mueller Hinton, à 37°C, durante 24 horas. Posteriormente, foi preparada uma suspensão das colônias em caldo Mueller Hinton com turvação equivalente a 0,5 MacFarland (1,5 x 108 UFC/mL), utilizando espectrofotômetro (Pró-análise), no qual deveria apresentar densidade óptica entre 0,08 - 0,13, à 600 nm (OD600). Em cada poço da placa com antimicrobianos foram inoculados 20 µL da suspensão bacteriana, dispondo 11 poços por isolado, sendo um isolado por linha. Em seguida, as placas foram incubadas em estufa (LimaTec) à 37°C, por 24 horas.
Em cada placa havia uma coluna de poços para controle de crescimento contendo caldo Mueller Hinton e suspensão bacteriana, uma coluna de poços para controle de esterilidade contendo apenas caldo Mueller Hinton, uma linha para controle do antimicrobiano contendo a suspensão de um isolado de linhagem de referência ATCC 29212 sensível a ele, além de uma linha de um isolado de linhagem de referência ATCC 51299 resistente a ele, todos estabelecidos pelo CLSI[21].
O resultado foi interpretado por meio de luz transmitida, sendo a CIM a menor concentração de antimicrobiano capaz de inibir completamente o crescimento bacteriano, tornando o poço com aspecto visualmente límpido.
Avaliação da concentração inibitória mínima do extrato aquoso de Cordia salicifolia Cham
A determinação da CIM do extrato aquoso de C. salicifolia contra os isolados de E. faecium foi realizada conforme a metodologia descrita por Filho et al[22], com adaptações.
O extrato aquoso foi diluído em uma solução de caldo Mueller Hinton com 10% de dimetilsulfóxido (DMSO) até atingir a concentração de 1000 mg/mL, concentração citotóxica média para macrófagos humanos determinada no Laboratório de Farmacologia da UFTM[19].
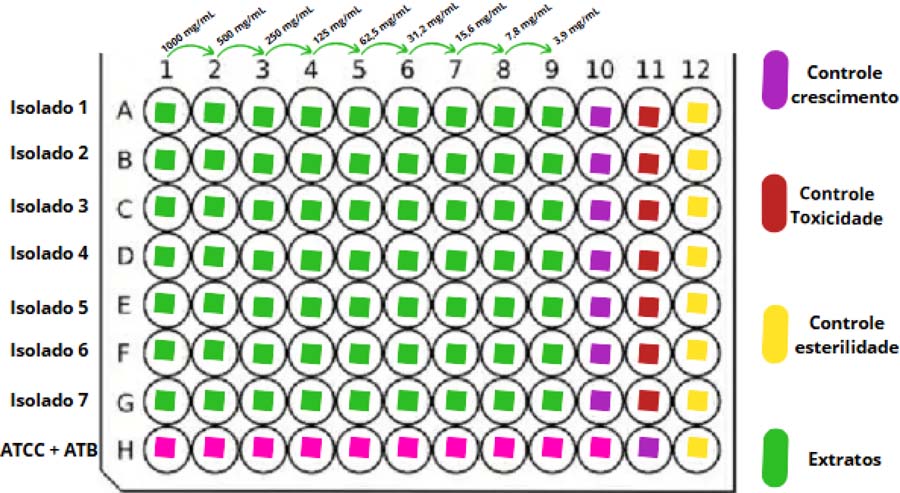
Em uma placa de 96 poços, foi adicionado 40 µL do extrato aquoso em diluições seriadas com concentrações entre 1000 e 1,95 mg/mL nos poços, sendo uma concentração em cada coluna. Em seguida, foram adicionadas 160 µL da suspensão bacteriana de cada isolado, preparadas da mesma forma do teste de CIM dos antimicrobianos, sendo um isolado por linha. Os controles foram o caldo Mueller Hinton para controle de esterilidade, a ATCC 29212 (sensível a vancomicina) inoculada com vancomicina para controle de execução correta da metodologia, suspensões bacterianas para controle de crescimento, além de controle de toxicidade do DMSO contendo a suspensão bacteriana + DMSO + água utilizada como solvente do extrato, conforme FIGURA 2. A placa foi incubada à 37°C, por 24 horas e analisada da mesma forma da placa de CIM dos antimicrobianos.
: Mapa da placa de concentração inibitória mínima do extrato aquoso de Cordia salicifolia Cham.
Avaliação da concentração inibitória mínima do extrato etanólico de Cordia salicifolia Cham
A determinação da CIM do extrato etanólico de C. salicifolia contra os isolados de E. faecium foi feita seguindo a mesma metodologia do extrato aquoso, sendo alterada apenas a diluição. O extrato etanólico foi diluído em uma solução de caldo Mueller Hinton com 20% de DMSO, devido sua menor solubilidade em água, até atingir a concentração de 0,06 mg/mL, dose citotóxica média que foi determinada no Laboratório de Farmacologia da UFTM. Foram testadas concentrações de 0,06 a 0,00012 mg/mL de extrato etanólico de C. salicifolia contra E. faecium.
Avaliação da Concentração Bactericida Mínima
Após a leitura das placas de CIM dos extratos aquoso e etanólico, foi realizada a avaliação da concentração bactericida mínima (CBM) dos extratos sobre os isolados de E. faecium. Seguindo o protocolo padrão do CLSI[21], com adaptações, foram removidos 10 µL dos poços em que não houve turvação, ou seja, aqueles em que os extratos inibiram o crescimento bacteriano, dos poços com a maior concentração de extrato, dos poços com a menor concentração de extrato e, também dos poços sem extrato. Todos foram cultivados em placas de ágar Mueller Hinton, incubados à 37°C, por 24 horas. Posteriormente, foi feita a verificação do local onde foram inseridos, identificando um possível crescimento bacteriano.
Detecção e classificação de produção de biofilme
Para cada isolado de E. faecium selecionado foi realizada uma análise do seu nível de produção de biofilme, baseando-se na metodologia de Stepanovic et al[23]; com adaptações. Foram preparadas suspensões bacterianas, com densidade óptica a 600 nm (OD600) de 0,2, a partir de cultivos dos isolados em ágar BHI, incubados à 37°C, por 24 horas.
Em seguida, foi feito o inóculo na placa de 96 poços de fundo chato. Iniciando pelos controles, adicionou-se 200 μL de caldo BHI em 6 poços, que foram os controles de esterilidade. Para o controle de formação de biofilme, adicionou-se 200 μL de suspensão bacteriana da ATCC 29212, que é uma forte produtora de biofilme, em 6 poços. Em seguida, os outros isolados foram adicionados, sendo 6 poços com 200 μL de suspensão bacteriana para cada, conforme FIGURA 3. A placa foi incubada à 37°C, por 24 horas. Todo o experimento foi realizado em duplicata.
Em seguida, os poços foram lavados com solução tamponada, removendo qualquer material que não fosse o biofilme formado. Esse biofilme foi fixado com metanol, corado com cristal violeta à 2% e homogeneizado com ácido acético 33%. Finalizou-se com a leitura das placas em aparelho leitor de placas de microtitulação (ThermoPlate) à 570 nm (OD570), no qual o valor de densidade óptica corresponde à quantidade de biomassa no poço. A absorbância final de cada isolado foi a média das absorbâncias dos 6 poços. O fluxograma da metodologia resumida pode ser visualizado na FIGURA 4.
Finalmente, foi definido um valor de cut-off para a placa, e foram realizados os cálculos para classificar os isolados, conforme proposto por Stepanovic et al[23].
Avaliação dos extratos de Cordia salicifolia Cham sobre o biofilme
Após classificar cada isolado, iniciou-se o ensaio de produção de biofilme na presença dos extratos da planta, seguindo a metodologia descrita por Pavão et al[24], com modificações. Após o preparo da suspensão bacteriana com densidade óptica a 600 nm (OD600) de 0,2, a placa de 96 poços de fundo chato foi cultivada, adicionando-se 160 μL de cada suspensão bacteriana em 12 poços, entre eles 6 poços recebem 40 μL de uma dose sub-inibitória do extrato de C. salicifolia e os outros 6 recebem uma dose com metade dessa concentração, conforme FIGURA 5. Após o cultivo, resumidamente, a placa foi lavada, fixada, corada e foi feita a leitura, tudo em duplicata, seguindo os mesmos passos da avaliação inicial de biofilme sem os extratos. Após fazer a leitura da placa e os cálculos necessários, baseando-se na média de absorbância dos seis poços de cada isolado, média de absorbância dos seis poços do controle negativo e desvio padrão do controle negativo, o cut off estabelecido por placa, cada isolado foi classificado quanto a produção de biofilme na presença dos extratos de C. salicifolia, seguindo os critérios de Stepanovic et al[23].
: Mapa da placa de biofilme do Enterococcus faecium com extrato de Cordia salicifolia Cham.
Por fim, foi feita uma análise comparativa entre a classificação de produção de biofilme de cada isolado puro e na presença de diferentes concentrações de extratos aquoso e etanólico da C. salicifolia, verificando se o extrato foi capaz de inibir, diminuir ou potencializar o biofilme bacteriano.
Resultados e Discussão
Rendimento dos extratos aquoso e etanólico
O rendimento dos extratos aquoso e etanólico é influenciado por diversos fatores ambientais, como o clima e a parte da planta utilizada[24]. Nos estudos realizados no Laboratório de Estudos Farmacológicos da UFTM, o extrato aquoso apresentou uma concentração citotóxica média para macrófagos humanos muito alta em comparação ao extrato etanólico, sendo necessário o uso de maior quantidade de extrato aquoso nos experimentos. Para que pudessem ser realizadas todas as análises, o extrato aquoso precisaria ter um melhor rendimento. Portanto, devido à quantidade insuficiente, não foi feita a análise da eficácia do extrato aquoso de C. salicifolia contra o biofilme do E. faecium, apenas a determinação de sua CIM e CBM.
Avaliação da Concentração Inibitória Mínima de Antimicrobianos
Entre os 12 isolados de E. faecium analisados, 11 (91,6%) foram resistentes à vancomicina, 11 (91,6%) foram resistentes também à ampicilina, 10 (83,3%) à gentamicina e 6 (50%) à estreptomicina, sendo essa resistência à gentamicina e estreptomicina uma resistência de alto nível (FIGURA 6). Essa multirresistência aos antimicrobianos mais utilizados na clínica médica, principalmente à vancomicina, está em conformidade com a ampla revisão bibliográfica realizada por Jabbari et al.[25].
: Perfil de resistência dos isolados de Enterococcus faecium aos antimicrobianos vancomicina, ampicilina, gentamicina e estreptomicina.
A revisão de Jabbari et al.[25] também destaca que o fenótipo VRE foi responsável por algumas das infecções hospitalares fatais causadas por Enterococcus. Jabbari et al.[25] ainda destacaram um levantamento feito pela OMS em diversos países, que aponta o Brasil com alta prevalência de isolados de VRE, com mais de 60% dos isolados analisados sendo VRE.
Avaliação da concentração inibitória mínima dos extratos aquoso e etanólico de Cordia salicifolia Cham
As concentrações máximas de extratos aquoso e etanólico de C. salicifolia testadas contra os isolados de E. faecium foram iguais a suas concentrações citotóxicas médias, sendo 1000 mg/mL para o extrato aquoso e 0,06 mg/mL para o extrato etanólico. Essas concentrações máximas e suas sub-doses não foram capazes de inibir o crescimento bacteriano dos 12 isolados analisados de E. faecium e das ATCCs de E. faecalis 29212 e 51299 (TABELA 2).
: Concentração inibitória mínima dos extratos aquoso e etanólico de Cordia salicifolia Cham contra os isolados de Enterococcus faecium.
Não foram encontrados na literatura outros estudos de avaliação da CIM dos extratos, aquoso ou etanólico, da C. salicifolia contra E. faecium ou outras espécies bacterianas. No entanto, em estudo realizado com outra espécie do gênero, C. verbenacea, a análise da atividade antimicrobiana do óleo essencial revelou sensibilidade quando testado com bactérias Gram-positivas como S. aureus e S. epidermidis, enquanto bactérias Gram-negativas apresentaram resistência[16].
Avaliação da Concentração Bactericida Mínima
Embora não houvesse uma CIM nas concentrações testadas, foi realizada a análise da CBM[26] para verificar se os extratos poderiam ter qualquer efeito bactericida quando avaliados em condições diferentes daquelas analisadas na microplaca de 96 poços. Foram avaliados o crescimento de E. faecium em ágar Mueller Hinton na presença da maior concentração testada dos extratos, na presença da menor concentração testada dos extratos, além do crescimento na ausência dos extratos utilizados como controle (FIGURA 7). Em todas as análises houve crescimento bacteriano, reforçando o resultado de que, nestas concentrações os extratos, aquoso e etanólico de C. salicifolia, não apresentaram atividade antimicrobiana contra esses isolados de E. faecium.
: Análise da concentração bactericida mínima dos extratos aquoso e etanólico de Cordia salicifolia Cham.
Detecção e classificação de produção de biofilme
Entre os 12 isolados analisados e classificados através da metodologia descrita[23], 10 (83,3%) foram classificados como forte produtores de biofilme e 2 (16,7%) foram moderados produtores de biofilme, não houve nenhum isolado que não produzisse ou fosse fraco produtor de biofilme.
Esses resultados convergem com os estudos de Pavão et al[24], que também analisaram a produção de biofilme por diferentes espécies bacterianas e de diferentes sítios de isolamento, sendo os isolados hospitalares os maiores produtores de biofilme.
Além de serem altamente capazes de produzir biofilme, esses isolados apresentaram alta resistência aos antimicrobianos testados, sugerindo uma relação entre a capacidade de formação de biofilme e a resistência aos antimicrobianos, como descrito por Lewis et al[27], uma bactéria com biofilme maduro pode tolerar concentrações até 1000 vezes maiores em comparação a bactérias planctônicas. Também corrobora para essa tese, o estudo de Silva et al.[28] no qual foi reportado que os isolados analisados de E. faecium e outras espécies foram majoritariamente fracos produtores de biofilme e apresentaram menor resistência aos antimicrobianos.
Avaliação dos extratos de Cordia salicifolia Cham sobre o biofilme
A concentração citotóxica média do extrato etanólico da C. salicifolia igual a 0,06 mg/mL e suas diluições não apresentaram inibição da produção de biofilme do E. faecium. Em dois isolados (276 e 882) a presença do extrato alterou a classificação, passando de moderados para fortes produtores de biofilme ao serem cultivados com o extrato etanólico. Em um dos isolados (722) analisados, a concentração de 0,03 mg/mL apresentou algum efeito de inibição sobre o biofilme, passando de forte para moderado produtor, mas na concentração de 0,06 mg/mL ele voltou a apresentar uma forte produção de biofilme (TABELA 3).
: Produção de biofilme por isolados de Enterococcus faecium na ausência e na presença de 0,03 mg/mL e 0,06 mg/mL de extrato etanólico de Cordia salicifolia Cham.
Diferentemente do presente estudo, Santos et al.[29] reportaram a eficácia dos extratos de Salvia officinalis e Glycyrrhiza glabra sobre o biofilme de E. faecium e E. faecalis. Essas plantas inibiram o biofilme quando usadas simultaneamente, tendo eficácia comparável à clorexidina, um antisséptico químico com ação antibacteriana.
No entanto, Glasenapp et al.[30] que analisaram a atividade dos extratos de duas espécies de plantas, Bruguiera cylindrica e Laguncularia racemosa, em diferentes fases da produção de biofilme de alguns microrganismos, reportaram que o extrato de B. cylindrica aumentou a capacidade de adesão do biofilme de E. coli (ATCC 25404). Além disso, os extratos de B. cylindrica e L. racemosa não alteraram a quantidade de biomassa celular do biofilme de E. coli, e ainda, promoveram um aumento das substâncias poliméricas extracelulares, que formam uma camada viscosa que torna o agregado de bactérias mais resistente, caracterizando o biofilme. Esse aumento pode ser justificado pela capacidade dessas plantas em modular a composição química da matriz do biofilme.
Conclusão
Os resultados do presente estudo indicaram que os extratos, aquoso e etanólico, obtidos de folhas e talos de C. salicifolia não apresentaram atividade antibacteriana nem anti-biofilme em isolados clínicos de E. faecium.
Agradecimentos
Agradeço aos coautores pelo apoio essencial na realização deste estudo e pelas contribuições científicas durante o processo. Também agradeço ao Diego Batista Carneiro de Oliveira e à Iara Rossi Gonçalves por todas as contribuições para a finalização e aprimoramento deste artigo de Pesquisa.
Referências
- 1 García-Solache M, Rice LB. The Enterococcus: a Model of Adaptability to Its Environment. Clin Microbiol Rev [Internet]. 2019 Mar 20; 32(2): e00058-18. [acesso em: 1 nov. 2024]. [ https://doi.org/10.1128/cmr.00058-18 ] [ https://pubmed.ncbi.nlm.nih.gov/30700430/ ].
» https://doi.org/10.1128/cmr.00058-18» https://pubmed.ncbi.nlm.nih.gov/30700430/ - 2 Gao W , Howden BP , Stinear TP . Evolution of virulence in Enterococcus faecium, a hospital-adapted opportunistic pathogen. Current Opin Microbiol. 2018 Feb; 41: 76-82. [acesso em: 1 nov. 2024] [ https://doi.org/10.1016/j.mib.2017.11.030 ] [ https://pubmed.ncbi.nlm.nih.gov/29227922/ ].
» https://doi.org/10.1016/j.mib.2017.11.030» https://pubmed.ncbi.nlm.nih.gov/29227922/ - 3 Zhou X, Willems RJL, Friedrich AW, Rossen JWA, Bathoorn E. Enterococcus faecium: from microbiological insights to practical recommendations for infection control and diagnostics. Antimicr Resist Infect Control. 2020 Aug 10; 9(1): 130. [acesso em: 7 nov. 2024] [ https://doi.org/10.1186/s13756-020-00770-1 ] [ https://pubmed.ncbi.nlm.nih.gov/32778149/ ].
» https://doi.org/10.1186/s13756-020-00770-1» https://pubmed.ncbi.nlm.nih.gov/32778149/ - 4 Gorrie C, Higgs C, Carter G, Stinear TP, Howden B. Genomics of vancomycin-resistant Enterococcus faecium. Microb Genom. 2019 Jul 1; 5(7): e000283. [acesso em: 7 nov. 2024]. [ https://doi.org/10.1099/mgen.0.000283 ] [ https://pubmed.ncbi.nlm.nih.gov/31329096/ ].
» https://doi.org/10.1099/mgen.0.000283» https://pubmed.ncbi.nlm.nih.gov/31329096/ - 5 Tacconelli E, Carrara E, Savoldi A, Harbarth S, Mendelson M, Monnet DL, et al. Discovery, research, and development of new antibiotics: the WHO priority list of antibiotic-resistant bacteria and tuberculosis. Lancet Infect Dis [Internet]. 2018 Mar; 18(3): 318-27. [acesso em: 7 nov. 2024]. [ https://doi.org/10.1016/S1473-3099 (17)30753-3] [ https://pubmed.ncbi.nlm.nih.gov/29276051/ ].
» https://doi.org/10.1016/S1473-3099 (17)30753-3» https://pubmed.ncbi.nlm.nih.gov/29276051/ - 6 Lev K, Kunz Coyne AJ, Kebriaei R, Morrisette T, Stamper K, Holger DJ, et al. Evaluation of Bacteriophage-Antibiotic Combination Therapy for Biofilm-Embedded MDR Enterococcus faecium. Antibiotics. 2022 Mar 15; 11(3): 392. [acesso em: 7 nov. 2024]. [ https://doi.org/10.3390/antibiotics11030392 ] [ https://pubmed.ncbi.nlm.nih.gov/35326855/ ].
» https://doi.org/10.3390/antibiotics11030392» https://pubmed.ncbi.nlm.nih.gov/35326855/ - 7 Srivastava S, Bhargava A. Biofilms and human health. Biotechnol Letters. 2015 Sep 19; 38(1): 1-22. [acesso em: 7 nov. 2024] [ https://doi.org/10.1007/s10529-015-1960- ] [8 https://pubmed.ncbi.nlm.nih.gov/26386834/ ].
» https://doi.org/10.1007/s10529-015-1960-» https://pubmed.ncbi.nlm.nih.gov/26386834/ - 8 Jaroš P, Timkina E, Michailidu J, Maršík D, Kulišová M, Kolouchová I, et al. Boswellic Acids as Effective Antibacterial Antibiofilm Agents. Molecules. 2022 Jun 13; 27(12): 3795. [acesso em: 7 nov. 2024] [ https://doi.org/10.3390/molecules27123795 ] [ https://pubmed.ncbi.nlm.nih.gov/35744925/ ].
» https://doi.org/10.3390/molecules27123795» https://pubmed.ncbi.nlm.nih.gov/35744925/ - 9 Duarte MCT. Atividade antimicrobiana de plantas medicinais e aromáticas utilizadas no Brasil. Construindo a história dos produtos naturais. Multiciência. 2006; 7: 46-77. [acesso em: 10 nov. 2024]. Disponível em: [ http://plone.ufpb.br/nephf/contents/documentos/artigos/fitoterapia/atividade-antimicrobiana-de-plantas ].
» http://plone.ufpb.br/nephf/contents/documentos/artigos/fitoterapia/atividade-antimicrobiana-de-plantas - 10 Álvarez-Martínez FJ, Barrajón-Catalán E, Micol V. Tackling Antibiotic Resistance with Compounds of Natural Origin: A Comprehensive Review. Biomedicines. 2020 Oct 11; 8(10): 405. [acesso em: 10 nov. 2024]. [ https://doi.org/10.3390/biomedicines8100405 ] [ https://pubmed.ncbi.nlm.nih.gov/33050619/ ].
» https://doi.org/10.3390/biomedicines8100405» https://pubmed.ncbi.nlm.nih.gov/33050619/ - 11 Cowan MM. Plant Products as Antimicrobial Agents. Clin Microbiol Rev. 1999 Oct 1; 12(4): 564-82. [acesso em: 10 nov. 2024]. [ https://doi.org/10.1128/CMR.12.4.564 ] [ https://pubmed.ncbi.nlm.nih.gov/10515903/ ].
» https://doi.org/10.1128/CMR.12.4.564» https://pubmed.ncbi.nlm.nih.gov/10515903/ - 12 Lu L, Hu W, Tian Z, Yuan D, Yi G, Zhou Y, et al. Developing natural products as potential anti-biofilm agents. Chinese Medic. 2019 Mar 20; 14(1). [acesso em: 10 nov. 2024]. [ https://doi.org/10.1186/s13020-019-0232-2 ] [ https://pubmed.ncbi.nlm.nih.gov/30936939/ ].
» https://doi.org/10.1186/s13020-019-0232-2» https://pubmed.ncbi.nlm.nih.gov/30936939/ - 13 Yong YY, Dykes GA, Choo WS. Biofilm formation by staphylococci in health-related environments and recent reports on their control using natural compounds. Critical Rev Microbiol. 2019 Feb 20; 45(2): 201-22. [acesso em: 10 nov. 2024]. [ https://doi.org/10.1080/1040841X.2019.1573802 ] [ https://pubmed.ncbi.nlm.nih.gov/30786799/ ].
» https://doi.org/10.1080/1040841X.2019.1573802» https://pubmed.ncbi.nlm.nih.gov/30786799/ - 14 Nogueira TBSS, Nogueira RBSS, Silva DA, Tavares J, Lima EO, Pereira FO, et al. First Chemical Constituents from Cordia exaltata Lam and Antimicrobial Activity of Two Neolignans. Molecules. 2013 Sep 10; 18(9): 11086-99. [acesso em: 10 nov. 2024]. [ https://doi.org/10.3390/molecules180911086 ] [ https://pubmed.ncbi.nlm.nih.gov/24025457/ ].
» https://doi.org/10.3390/molecules180911086» https://pubmed.ncbi.nlm.nih.gov/24025457/ - 15 Sharma M, Mallubhotla S. Diversity, Antimicrobial Activity, and Antibiotic Susceptibility Pattern of Endophytic Bacteria Sourced From Cordia dichotoma L. Frontiers Microbiol. 2022 May 13; 13. [acesso em: 10 nov. 2024]. [ https://doi.org/10.3389/fmicb.2022.879386 ] [ https://pubmed.ncbi.nlm.nih.gov/35633730/ ].
» https://doi.org/10.3389/fmicb.2022.879386» https://pubmed.ncbi.nlm.nih.gov/35633730/ - 16 Carvalho PM, Rodrigues RF, Christine A, Marques MM, Shimizu MT. Chemical composition and antimicrobial activity of the essential oil of Cordia verbenacea D.C. J Ethnopharmacol. 2004 Dec 1; 95(2-3): 297-301. [acesso em: 10 nov. 2024]. [ https://doi.org/10.1016/j.jep.2004.07.028 ] [ https://pubmed.ncbi.nlm.nih.gov/15507352/ ].
» https://doi.org/10.1016/j.jep.2004.07.028» https://pubmed.ncbi.nlm.nih.gov/15507352/ - 17 Flora do Brasil 2020 [Internet]. Cordia salicifolia. Jardim Botânico do Rio de Janeiro. [acesso em: 05 fev. 2025]. Disponível em: [ https://floradobrasil.jbrj.gov.br ].
» https://floradobrasil.jbrj.gov.br - 18 Matias EFF, Alves EF, Silva MKN, Carvalho VRA, Coutinho HDM, Costa JGM. The genus Cordia: botanists, ethno, chemical and pharmacological aspects. Rev Bras Farmacogn. 2015 Sep; 25(5): 542-52. [acesso em: 10 nov. 2024]. [ https://doi.org/10.1016/j.bjp.2015.05.012 ].
» https://doi.org/10.1016/j.bjp.2015.05.012 - 19 Oliveira SR. Potencial antioxidante e efeito de preparações fitoterápicas de Cordia salicifolia sobre adipocinas. Uberaba. 2020. 66f. Dissertação de Mestrado [Programa de Pós-Graduação em Ciência e Tecnologia de Materiais, área de concentração - Produtos Naturais e Sintéticos Bioativos] - Universidade Federal do Triângulo Mineiro, UFTM, Uberaba, MG. 2020. [acesso em: 10 nov. 2024]. Disponível em: [ https://bdtd.uftm.edu.br/bitstream/123456789/1273/1/DISSERT%20SIMONE%20R%20OLIVEIRA.pdf ].
» https://bdtd.uftm.edu.br/bitstream/123456789/1273/1/DISSERT%20SIMONE%20R%20OLIVEIRA.pdf - 20 Franco ATM, et al. Comparação entre teste bioquímico clássico e o método da reação em cadeia da Polimerase (PCR) para identificação de estirpes de Enterococcus faecalis isoladas da cavidade oral. Salusvita. Bauru. 2012; 31(3): 191-202. [acesso em: 7 nov. 2024]. Disponível em: [ https://secure.unisagrado.edu.br/static/biblioteca/salusvita/salusvita_v31_n3_2012_art_01.pdf ].
» https://secure.unisagrado.edu.br/static/biblioteca/salusvita/salusvita_v31_n3_2012_art_01.pdf - 21 CLSI. Performance Standards for Antimicrobial Susceptibility Testing. [Internet]. Twenty-sixth Edition. CLSI document M100-Ed31. Wayne, PA: Clinical and Laboratory Standards Institute; 2021. [acesso em: 13 nov. 2024]. Disponível em: [ https://clsi.org/standards/products/microbiology/documents/m100/ ].
» https://clsi.org/standards/products/microbiology/documents/m100/ - 22 Santos Filho LGA, Castro KNC, Pereira AML, Diniz FM. Detecção da atividade antibacteriana in vitro de compostos naturais à base de plantas: metodologia científica. [acesso em: 10 nov. 2024]. Disponível em: [ https://ainfo.cnptia.embrapa.br/digital/bitstream/item/206136/1/Comunicado-254-AINFO.pdf ].
» https://ainfo.cnptia.embrapa.br/digital/bitstream/item/206136/1/Comunicado-254-AINFO.pdf - 23 Stepanovic S, Vukovic D, Dakic I, Savic B, Švabic-Vlahovic M. A modified microtiter-plate test for quantification of staphylococcal biofilm formation. J Microbiol Meth. 2000 Apr; 40(2): 175-9. [acesso em: 10 nov. 2024]. [ https://doi.org/10.1016/S0167-7012 (00)00122-6] [ https://pubmed.ncbi.nlm.nih.gov/10699673/ ].
» https://doi.org/10.1016/S0167-7012 (00)00122-6» https://pubmed.ncbi.nlm.nih.gov/10699673/ - 24 Pavão DP e, Moraes FC, Ribeiro BLM, Costa FGR, Camara MBP. Capacidade de formação de biofilme por cepas bacterianas e ação antibiofilme do extrato de Lafoensia pacari (Lythraceae). Rev Fitos. 2021 Jun 30; 15(2): 153-65. [acesso em: 10 nov. 2024]. [ https://doi.org/10.32712/2446-4775.2021.1073 ].
» https://doi.org/10.32712/2446-4775.2021.1073 - 25 Jabbari SMS, Pormohammad A, Hashemi A, Lak P. Global prevalence of antibiotic resistance in blood-isolated Enterococcus faecalis and Enterococcus faecium: a systematic review and meta-analysis. Infec Drug Resist. 2019 Sep; 12: 2713-25. [acesso em: 10 nov. 2024]. [ https://doi.org/10.2147/IDR.S206084 ].
» https://doi.org/10.2147/IDR.S206084 - 26 Gonçalves AL, Alves Filho A, Menezes H. Estudo comparativo da atividade antimicrobiana de extratos de algumas árvores nativas. Arq Inst Biol. 2005 Jul; 72(3): 353-8. [acesso em: 10 nov. 2024]. [ https://doi.org/10.1590/1808-1657v72p3532005 ].
» https://doi.org/10.1590/1808-1657v72p3532005 - 27 Lewis K. Riddle of Biofilm Resistance. Antimicrob Agents Chemother. 2001 Apr; Volume 45. [acesso em: 13 nov. 2024]. [ https://doi.org/10.1128/aac.45.4.999-1007.2001 ].
» https://doi.org/10.1128/aac.45.4.999-1007.2001 - 28 Silva MGV, Andrade JM, Moura FML, Medeiros AKA, Cordeiro GS, Melo NSS, et al. Resistência antimicrobiana e formação de biofilme de Enterococcus spp. isolados de queijo coalho. Medicina Veterinária (UFRPE). 2024 May 23; 18(1): 91-7. [acesso em: 13 nov. 2024]. DOI: https://doi.org/10.26605/medvet-v18n1-5879
» https://doi.org/10.26605/medvet-v18n1-5879 - 29 Santos TDSA, Meccatti VM, Pereira TC, Marcucci MC, Hasna AA, Valera MC, et al. Antibacterial Effect of Combinations of Salvia officinalis and Glycyrrhiza glabra Hydroalcoholic Extracts against Enterococcus spp. Coatings. 2023; 13: 1579. [acesso em: 13 nov. 2024]. [ https://doi.org/10.3390/coatings13091579 ].
» https://doi.org/10.3390/coatings13091579 - 30 Glasenapp Y, Cattò C, Villa F, Saracchi M, Cappitelli F, Papenbrock J. Promoting Beneficial and Inhibiting Undesirable Biofilm Formation with Mangrove Extracts. Int J Mol Sci. 2019; 20: 3549. [acesso em: 13 nov. 2024]. https://doi.org/10.3390/ijms20143549 ].
» https://doi.org/10.3390/ijms20143549
-
Fonte de Financiamento:
Universidade Federal do triângulo Mineiro.
Datas de Publicação
- Publicação nesta coleção
18 Fev 2026 - Data do Fascículo
Fev 2026
Histórico
- Recebido
21 Fev 2025 - Aceito
05 Nov 2025
 Eficácia da Cordia salicifolia Cham (Boraginaceae) contra o biofilme de Enterococcus faecium
Eficácia da Cordia salicifolia Cham (Boraginaceae) contra o biofilme de Enterococcus faecium

 Fonte: autores, 2024.
Fonte: autores, 2024. Fonte: autores, 2024.
Fonte: autores, 2024.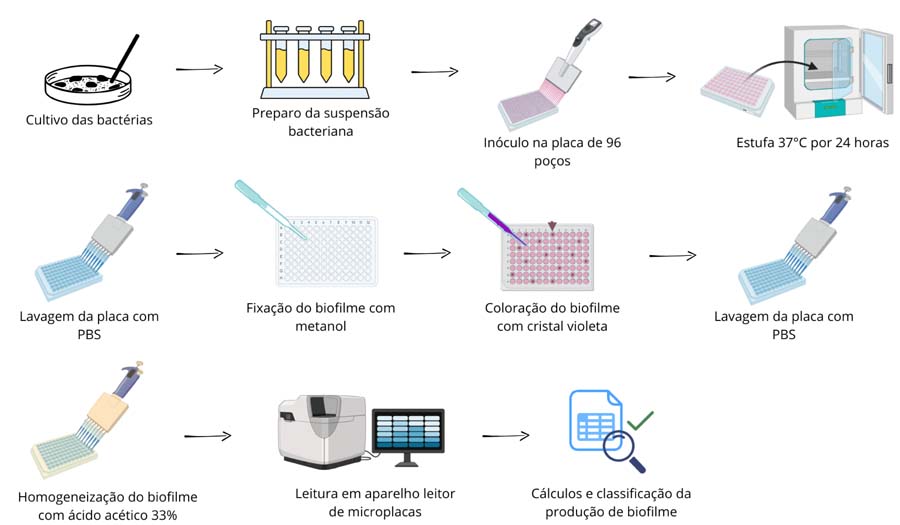 Fonte: autores, 2024.
Fonte: autores, 2024.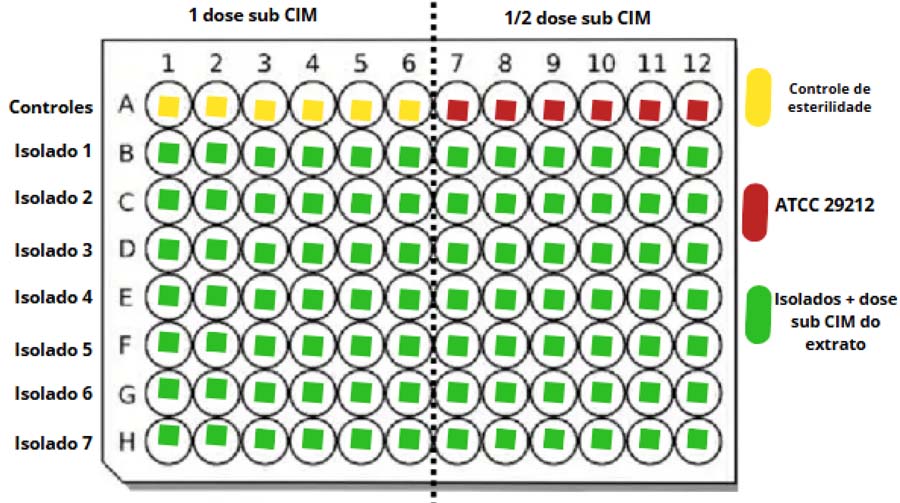 Fonte: autores, 2024.
Fonte: autores, 2024.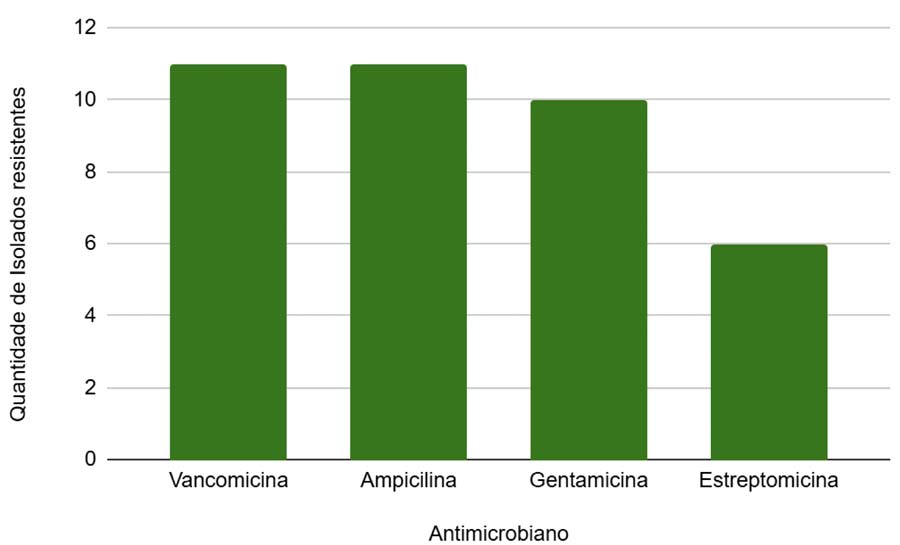 Fonte: autores, 2024.
Fonte: autores, 2024.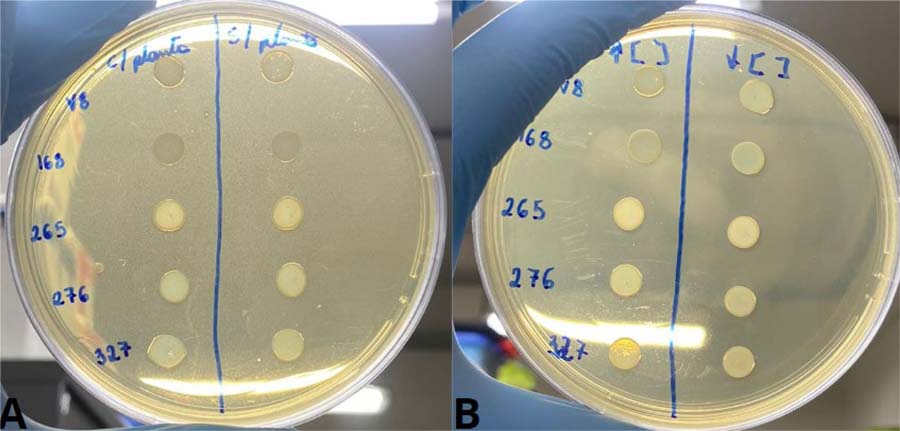 A: Avaliação do crescimento com a maior concentração do extrato e sem extrato. B: Avaliação do crescimento com a maior concentração do extrato e com a menor concentração do extrato. Fonte: autores, 2024.
A: Avaliação do crescimento com a maior concentração do extrato e sem extrato. B: Avaliação do crescimento com a maior concentração do extrato e com a menor concentração do extrato. Fonte: autores, 2024.