Resumo
Cannabis sativa é uma espécie vegetal complexa, nativa da Ásia, rica em substâncias bioativas, os canabinoides, possuindo elevado interesse medicinal. No Brasil, a importação de extratos de C. sativa para uso terapêutico e sua elaboração artesanal são regulamentados pela ANVISA. Existem nove extratos de C. sativa e 14 produtos à base de canabidiol comercializados mediante a apresentação de receituário tipo B, de numeração controlada, regulamentados pela RDC 327/2019, de forma a garantir segurança, eficácia e qualidade para os consumidores. São requisitos fundamentais apresentar padrões de qualidade que envolvam boas práticas de fabricação, determinação da pureza e potência dos canabinoides, ausência de contaminantes e pesticidas, além dos testes microbiológicos. O controle de qualidade acompanha todo o processo de fabricação, desde a matéria-prima, sendo mandatória a rastreabilidade desde o cultivo até o monitoramento pós comercialização. Para as determinações analíticas de resíduos de solventes, é empregada a cromatografia gasosa, enquanto o teor de canabinoides é avaliado por cromatografia líquida e análises inorgânicas empregam espectrometria de absorção atômica com forno de grafite e geração de hidreto. Esse artigo busca apresentar o estado atual dos ensaios de controle de qualidade conforme definidos na legislação para produtos à base de Cannabis.
controle de qualidade; regulamentação; produtos à base de Cannabis; cromatografia
Abstract
Cannabis sativa is a complex plant native to Asia, rich in bioactive compounds called cannabinoids, and has significant medicinal interest. In Brazil, ANVISA regulates the importation of Cannabis extracts for therapeutic use and their artisanal production. Currently, nine C. sativa extracts and 14 cannabidiol-based products are available with a type B prescription, following RDC 327/2019, ensuring safety, efficacy, and quality. Products must meet strict quality standards, including good manufacturing practices, cannabinoid purity and potency, absence of contaminants and pesticides, and microbiological testing. Quality control from raw material to post-marketing monitoring ensures complete traceability. Gas chromatography is used for solvent residue analysis, while cannabinoid content is assessed through liquid chromatography. Inorganic analyses employ atomic absorption spectrometry with a graphite furnace and hydride generation. This article presents the current state of quality control testing for Cannabis-based products according to existing regulations.
Keywords quality control; regulation; Cannabis-based products; chromatography
Introdução
Cannabis sativa e a relevância dos canabinoides
A Cannabis sativa L. é considerada uma das plantas mais antigas conhecida pelo homem1,2, com evidências arqueológicas de que foi cultivada na Ásia Central em 12.000 a.C3. Os relatos da utilização da planta como medicamento, em cerimônias religiosas e para fins recreativos devido ao seu potencial psicoativo são conhecidos há mais de cinco milênios4,5. Somente em 1753, o botânico sueco Carolus Linnaeus (Carl Von Linné) classificou a espécie Cannabis sativa L. (Cannabaceae)2,6. O gênero Cannabis é formado por espécies altamente variáveis, complexas e polimórficas. C. sativa é nativa da Ásia central e meridional, e possui muitos nomes e sinônimos, entre eles destacam-se: cânhamo, marijuana, marihuana, hemp, pot, gandia, grass, chanvre e maconha, como é popularmente conhecida no Brasil7,8.
A C. sativa é uma planta dioica, portanto possui espécimes femininas e masculinas, sendo atualmente cultivada em praticamente todos os países9,10. As espécimes femininas são mais ricas em compostos psicoativos comparadas às masculinas. Porém, geralmente as masculinas são mais altas e menos robustas, atingindo a média de 1-3 metros de altura. A extensão da ramificação, altura da planta, bem como a disposição dos seus constituintes dependem de diversos fatores, dentre eles: condições ambientais, origem geográfica, método de secagem, tipo de produção - “indoor” ou “outdoor” – e estágio de maturidade da planta10. Técnicas de plantio clássicas e inovadoras têm sido utilizadas para melhorar e diversificar as formas das drogas recreativas de C. sativa, resultando assim em muitas cultivares ricas em canabinoides adequadas para o uso recreativo6,11. C. sativa é considerada uma matriz complexa devido aos diversos compostos presentes em sua composição, que estão distribuídos entre várias classes químicas, tais como terpenos, açúcares, hidrocarbonetos, esteroides, flavonoides, aminoácidos, entre outros1,12.
As propriedades medicinais que alguns de seus compostos apresentam, têm sido objeto crescente de discussão. Dentre os produtos de caráter medicinal, se destacam os extratos oleosos formulados com as inflorescências desidratadas sendo infundidas em veículos oleosos, como óleo de oliva, coco, soja ou girassol13,14. Há diversos relatos clínicos dos efeitos positivos dos extratos e derivados de C. sativa, por exemplo, no tratamento do câncer, atuando na prevenção de náusea, dor decorrente da quimioterapia e no reestabelecimento do apetite, sendo usado inclusive para quadros de anorexia associados a HIV/AIDS4,5. Além disso, atividades antitumorais foram evidenciadas em modelos in vitro e in vivo, como potenciais retardantes e inibidores de crescimento de células tumorais4. Diversos relatos de efeitos analgésicos para dores neuropáticas também são encontrados, assim como estudos pré-clínicos documentando efeitos anticonvulsionantes e anti-epileptogênicos4,13. Por fim, há uma crescente quantidade de estudos em que se reporta a sua efetividade no tratamento paliativo e na contenção de sintomas de quadros clínicos como fibromialgia, epilepsia, distúrbios do sono, esclerose múltipla, refluxo gastrointestinal, síndrome do intestino irritável, hipertensão, esquizofrenia e transtorno de ansiedade generalizada4,5.
Estrutura e ação dos canabinoides
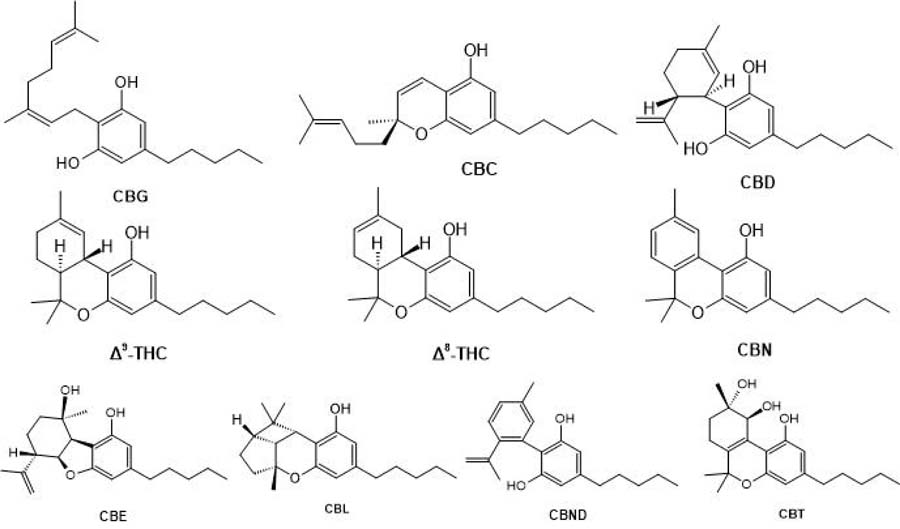
Mais de 700 constituintes naturais já foram identificados em C. sativa15, com destaque para os mais de 100 compostos terpenofenólicos, chamados canabinoides16-20. Estão concentrados nas secreções resinosas produzidas por tricomas glandulares distribuídos, principalmente, nas superfícies aéreas da planta e nas inflorescências femininas. Estes canabinoides são distribuídos em onze grupos, cada grupo representado por um canabinoide principal, a saber: (1) canabigerol (CBG), (2) canabicromeno (CBC), (3) canabidiol (CBD), (4) Δ9-trans-tetraidrocanabinol (THC), (5) Δ8-tetraidrocanabinol (Δ8-THC), (6) canabiciclol (CBL), (7) canabielsoin (CBE), (8) canabinol (CBN), (9) canabinodiol (CBND), (10) canabitriol (CBT), e (11) tipos diferentes de canabinoides10.
A FIGURA 1 apresenta a estrutura do canabinoide representante de cada grupo, do primeiro até o décimo grupo.
: Estrutura dos canabinoides canabigerol (CBG), canabicromeno (CBC), canabidiol (CBD), Δ9-trans-tetraidrocanabinol (THC), Δ8-tetraidrocanabinol (Δ8-THC), canabiciclol (CBL), canabielsoin (CBE), canabinol (CBN), canabinodiol (CBND) e canabitriol (CBT).
No material vegetal fresco de C. sativa, a maioria dos canabinoides que são produzidos pelo metabolismo da planta estão na forma de ácidos carboxílicos, tais como: o ácido tetrahidrocanabinol (Δ9-THCA) precursor do THC, o ácido canabidiólico (CBDA) precursor do CBD e o ácido canabigerólico (CBGA), precursor do CBG. Os precursores ácidos podem ser convertidos em seus análogos por descarboxilação, através da perda do grupo -COOH produzindo “canabinoides neutros” 21-23.
Os canabinoides possuem propriedades características de interação com dois subtipos de proteína-G acopladas a unidades receptoras do sistema denominado endocanabinoide (CB1 e CB2). Estes receptores se encontram localizados no cérebro, no Sistema Nervoso Central (SNC) e em órgãos periféricos de mamíferos, estando associados a respostas do sistema imunológico e a efeitos moduladores da cascata de citocinas4.
Destacam-se como canabinoides mais abundantes em C. sativa: 21,22 o CBD, como anticonvulsivante testado para uso em pacientes com epilepsia, além de atuar como anti-inflamatório, ansiolítico, antiespasmódico, analgésico e antipsicótico24; o CBG, com propriedades antiproliferativas, antiglaucoma, anti-inflamatórias, antifúngica e analgésica10,24,25; o CBN que atua como anti-inflamatório, anticonvulsivante e como sedativo1,24; o CBC como anti-inflamatório, antifúngico e analgésico24; e o THC, que é reconhecidamente a principal substância com características psicoativas da planta. Entre esses, o canabinol (CBN) merece uma atenção especial por possuir significativo efeito sedativo e apresentar participação relevante no chamado Efeito Entourage – a relação sinérgica entre todas as substâncias presentes na C. sativa que potencializa os efeitos terapêuticos dos canabinoides4.
Existe uma enormidade de isômeros encontrados em C. sativa, substâncias com a mesma fórmula molecular, mas estruturalmente diferentes, que representam desafios consideráveis nas análises empregando cromatografia líquida acoplada a detectores de arranjo de diodos (CLAE-DAD). Como exemplo, pode-se citar os canabinoides: CBC, CBD, CBL, THC, 9-cis-THC e 8-THC, todos com fórmula molecular C21H30O2 e massa molecular de 314 Daltons.
Técnicas Analíticas
A United Nations Office on Drugs and Crime (UNODC)24 editou um manual com métodos recomendados para identificação de canabis e seus diversos produtos, como técnicas cromatográficas acopladas a detectores convencionais, como a Cromatografia Gasosa com detector de ionização por chama (CG-DIC) e a CLAE-DAD, além de prever o acoplamento da cromatografia com a espectrometria de massas (CLAE-EM). Diversos métodos analíticos são utilizados para a identificação e quantificação de canabinoides em diversas matrizes, dentre as quais destacam-se plantas, óleos, produtos farmacêuticos e fluidos biológicos26.
A espectrometria de massas (EM) acoplada ou não a uma técnica de separação é, sem dúvida, a ferramenta mais amplamente utilizada. Quando associada à cromatografia líquida de alta ou ultra eficiência, garante-se um método seletivo e sensível, sendo a técnica de escolha para análise de THC, CBD e seus metabólitos em fluidos biológicos, como sangue, urina ou saliva27. A cromatografia líquida acoplada a espectrometria de massa em série (LC-EM/EM) é extremamente eficaz, pois combina os benefícios da separação da cromatografia líquida convencional ou da cromatografia líquida de ultra eficiência com a sensibilidade e seletividade do espectrômetro de massas em série28,29.
Outra técnica também utilizada para esse fim é o acoplamento da EM com a cromatografia gasosa (CG). A desvantagem dessa técnica é a necessidade de uma etapa prévia de derivatização. Por meio de reações de transformação molecular, se modifica a estrutura dos canabinoides de modo a torná-los voláteis e, só assim, passíveis de serem analisados por CG tanto para o acoplamento com a EM quanto com detector de ionização por chama30,31.
Outra técnica também acoplada a espectrometria de massas, que desponta pela agilidade, simplicidade e robustez é a análise direta em tempo real (ADTR-EM). Essa técnica não utiliza preparo de amostra e tem sido usada para triagem rápida e autenticação de produtos à base de C. sativa32.
Em relação aos métodos cromatográficos, a cromatografia líquida acoplada ao detector de Ultravioleta visível (UV-Vis) ou acoplada ao detector de arranjo de diodos (CLAE-DAD) ainda é considerada a técnica padrão para quantificação de THC, CBD e outros canabinoides em plantas, óleos e outros produtos farmacêuticos14.
Em relação às técnicas espectroscópicas aplicadas tanto no âmbito dos ensaios de triagem, quando nos de confirmação, são usadas a Espectroscopia no Infravermelho por Transformada de Fourier, onde é possível a identificação rápida de canabinoide em óleos e extratos vegetais, sendo menos sensível que as técnicas cromatográficas. Já a espectroscopia Raman, que permite uma análise rápida e não destrutiva, também é usada para caracterização de produtos à base de canabis33.
Os imunoensaios e testes rápidos também podem ser utilizados. Dentre estes, destaca-se o Elisa (Enzyme-Linked Immunosorbent Assay), utilizado para triagem de THC e metabólitos em fluidos biológicos. É um ensaio menos específico quando comparado às técnicas cromatográficas, podendo gerar casos de falso positivo. Os testes colorimétricos e kits portáteis fornecem resultados qualitativos, sendo utilizados como uma avaliação preliminar, para detecção de canabinoides, sendo mandatório a confirmação por métodos seletivos que garantam a identificação inequívoca do alvo analítico24,34.
Cabe ressaltar que, a escolha do método analítico depende do uso pretendido (triagem, confirmação, autenticação), que será uma função da matriz da amostra e da seletividade e sensibilidade requeridas.
Regulamentação mundial dos produtos à base de C. sativa
Nos últimos cinquenta anos, C. sativa passou por importantes avanços quanto a legalização e regulamentações sanitárias em escala global tanto para fins recreativos quanto medicinais14. Em termos globais, os Estados Unidos foi o primeiro país a trabalhar aspectos relacionados à regulamentação de produtos à base de C. sativa. Entre 1914 e 1933, trinta e três estados promulgaram leis restringindo a produção legal apenas para fins medicinais e industriais. Em 1937, o Marijuana Tax Act (Ato de Imposto sobre a Maconha) definiu o cânhamo como uma droga narcótica, sem distinguir entre plantas de baixo e alto teor de THC. Essas restrições limitaram a expansão da produção de cânhamo, que começou a declinar até desaparecer completamente na década de 195035. No QUADRO 1 encontram-se os principais marcos mundiais relacionados ao tema36.
É possível verificar uma mudança de paradigma relacionada ao uso de produtos à base de C. sativa entre os anos de 1975 e 1988. A partir de 1988, foi permitida a reintrodução do cultivo da planta em várias partes do mundo.
Regulamentação no Brasil
O primeiro ato referente à regulamentação de produtos à base de C. sativa no Brasil foi a Portaria SVS/MS nº 344/1998. Nesse documento, a canabis e seus derivados foram incluídos na lista de plantas prescritas37. O cultivo de cânhamo no Brasil é regulamentado pela Agência Nacional de Vigilância Sanitária38. Apesar da recente permissão para produtos à base de CBD no país, seguido após a mudança desse composto para a lista de substâncias sujeitas a controle especial, o THC ainda permanece na lista de substâncias entorpecentes e, portanto, proibidas.
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou, no dia 3 de dezembro de 2019, a Resolução de Diretoria Colegiada (RDC) 327/19, que cria uma categoria de produtos derivados de C. sativa. Seguindo as normas da ANVISA, os produtos à base de Cannabis devem ser comercializados respeitando o limite de no máximo 0,2% de THC, com exceção dos produtos indicados para os cuidados paliativos de pacientes sem alternativas terapêuticas e em vinte de três situações clínicas irreversíveis ou terminais, que poderão conter teor de THC acima de 0,2%39. A regra para o registro de medicamentos novos ou inovadores no Brasil prevê a realização de pesquisas clínicas que sejam capazes de comprovar a eficácia desses produtos, além de outros requisitos para seu enquadramento como medicamento, o que não é o caso produtos de canabis. O CBD só pode ser utilizado a partir de receita médica do tipo B e, conforme determina a legislação para o tema, somente no caso de esgotamento de outros tratamentos39. Até junho de 2023, vinte e cinco produtos à base de Cannabis foram aprovados pela ANVISA, sendo onze deles à base de extratos de C. sativa e quatorze produtos fitofármacos contendo CBD. Cabe ressaltar que apenas dois produtos contêm THC acima de 0,2 %.
Os medicamentos Dronabinol (Marinol®) e a Nabilona (Cesamet®), ainda não disponíveis no Brasil, contém análogos sintéticos do THC e são prescritos como estimuladores de apetite para pacientes com HIV/AIDS e como antiemético para náuseas e vômitos relacionados à quimioterapia40. O único medicamento disponível no Brasil é o Mevatyl®, uma solução em spray que contém 27 mg/ml de THC e 25 mg/ml de CBD, prescrito para tratar espasticidade muscular relacionada à esclerose múltipla41.
Atualmente em tramitação na Comissão de Assuntos Econômicos do Senado Federal, o Projeto de Lei (PL) n° 89/2023 aguarda pareceres das comissões pertinentes para avançar no processo legislativo. O PL tem como intuito estabelecer uma Política Nacional que assegure o fornecimento gratuito de medicamentos formulados a partir de derivados vegetais contendo CBD, em conjunto com outras substâncias canabinoides, incluindo o THC, nas unidades de saúde públicas e privadas vinculadas ao Sistema Único de Saúde (SUS). O objetivo principal do projeto é ampliar o acesso a tratamentos com canabis medicinal para pacientes que necessitam, especialmente aqueles com doenças crônicas como epilepsia, transtorno do espectro autista, esclerose múltipla, Alzheimer e fibromialgia. A proposta visa alinhar as políticas de saúde pública brasileiras às práticas internacionais e fornecer acolhimento adequado aos pacientes42. Para obter os medicamentos, os pacientes deverão estar cadastrados no SUS e apresentar prescrição médica detalhada, incluindo laudo que justifique o uso do medicamento à base de CBD em comparação com alternativas terapêuticas existentes. O fornecimento será gratuito para aqueles que comprovarem incapacidade financeira para adquirir os medicamentos por conta própria. O projeto também prevê a possibilidade de parcerias técnico-científicas para incentivar pesquisas sobre os usos terapêuticos da canabis, além de permitir a aquisição de medicamentos de entidades nacionais, preferencialmente sem fins lucrativos, que possuam autorização legal para o cultivo e manipulação da planta para fins medicinais. A iniciativa busca ampliar o acesso aos cuidados de saúde e garantir um tratamento adequado para pacientes que necessitam de terapias com canabis medicinal42.
A aquisição de produtos com menos de 0,2% de THC também pode ser realizada com prescrição médica através de Habeas Corpus garantido pelo poder judiciário brasileiro para determinados pacientes e organizações não governamentais que buscam judicialmente o acesso ao cultivo de canabis e à manufatura legal de extratos oleosos34.
Em outubro de 2024, a ANVISA ampliou a regulamentação, permitindo a regularização de produtos à base de canabis para uso veterinário pelo Ministério da Agricultura e Pecuária. Essa medida autoriza médicos veterinários a prescreverem tais produtos, seguindo controles rígidos e mediante receitas especiais retidas nas farmácias, garantindo uso estritamente terapêutico43.
No âmbito legislativo, diversas outras propostas tramitam no Congresso Nacional visando regulamentar o cultivo e a comercialização da Cannabis para fins medicinais e industriais. Em fevereiro de 2025, o Superior Tribunal de Justiça determinou que a ANVISA estabeleça, até maio do mesmo ano, regras para autorizar o cultivo e a comercialização da canabis no país, exclusivamente para fins medicinais e farmacêuticos, e apenas por pessoas jurídicas44.
É importante notar que, apesar dos avanços na regulamentação para uso medicinal, o cultivo doméstico e o uso recreativo da canabis permanecem proibidos no Brasil. A legislação atual foca na garantia de acesso seguro e controlado a produtos terapêuticos derivados da planta, assegurando qualidade e eficácia para os pacientes que deles necessitam.
Controle de qualidade
O controle de qualidade de produtos à base de canabis no Brasil é regulamentado para garantir a segurança e eficácia desses produtos para os consumidores. A ANVISA estabelece diretrizes específicas para assegurar a qualidade, de todo o processo produtivo, ou seja, desde a matéria-prima até o produto final45.
A primeira etapa que precisa ser verificada em uma empresa que atua ou pretende atuar na área de produção de produtos à base de C. sativa é a autorização de funcionamento de empresa, prevista pela RDC N° 16/201446. Essa RDC determina a obrigatoriedade de apresentação dos seguintes documentos: contrato social ou ata aprovada pela junta comercial, cadastro nacional da pessoa jurídica (CNPJ), alvará de localização e planta arquitetônica, organograma dos cargos e contrato dos prestadores de serviço. Quanto aos requisitos técnicos são mandatórios: equipamentos e instalações adequadas, sistema da qualidade estabelecido, política de qualificação e validação de equipamentos, boas condições de higiene, armazenamento e operação, procedimentos de controle de qualidade e especificações dos produtos definidas e finalmente procedimentos operacionais padrão, escritos de forma clara e objetiva46.
A RDC n° 658/2022 é a resolução cuja finalidade é assegurar as Boas Práticas de Fabricação de Medicamentos. Parte do gerenciamento da qualidade que assegura que os produtos são continuamente produzidos e controlados, de acordo com o uso pretendido. O gerenciamento da qualidade é um conceito abrangente, que cobre todas as questões que determinam, isolada ou conjuntamente a qualidade de um produto45. Entende-se como controle de qualidade o conjunto de medidas operacionais, técnicas e atividades estabelecidas em um sistema de qualidade, que garantem que os produtos sejam fabricados e controlados consistentemente de acordo com os padrões de qualidade apropriados para seu uso pretendido. Cabe enfatizar que o controle de qualidade é realizado desde a avaliação da matéria prima, passando pela análise do rótulo, até finalmente ser aprovado pelo setor de garantia da qualidade45.
Quando se trata de produtos importados é importante enfatizar que todos os lotes de produtos de C. sativa importados devem passar por controle de qualidade em laboratórios localizados no Brasil. Essas análises podem ser terceirizadas para laboratórios credenciados pela Rede Brasileira de Laboratórios Analíticos em Saúde (REBLAS) ou realizadas por fabricantes que possuam a certificação de boas práticas de fabricação de medicamentos. Tanto os produtos importados quanto os fabricados no Brasil devem passar por análises onde o método aplicado seja validado conforme as normas vigentes, de modo a assegurar precisão e confiabilidade dos resultados. Os produtos devem atender a especificações de qualidade estabelecidas, desde a matéria prima vegetal até o produto acabado45,47. Apesar de não haver, até o presente momento, monografia na farmacopeia brasileira que trate especificamente de medicamentos à base de C. sativa, existem requisitos mínimos, exigidos que devem ser aplicados para droga vegetal. O primeiro desses requisitos trata da identificação botânica, cuja finalidade é a garantia da autenticidade da matéria prima vegetal. A identificação precisa da espécie vegetal é essencial para garantir que a planta utilizada é a correta e que, portanto, possui os compostos terapêuticos desejados. A legislação de vários países exige a identificação botânica como parte do processo de controle de qualidade47.
O segundo requisito trata da definição do quimiotipo da planta. É preciso diferenciar entre os quimiotipos THC dominante (THC no mínimo 5,0% e CBD no máximo 1,0%, da droga seca), THC/CBD intermediário (THC no mínimo 1,0% e CBD entre 0,2% a 5,0%, da droga seca) e CBD dominante (THC no máximo 0,1% e CBD no mínimo 5,0%, da droga seca)18. A definição das características macromorfológicas (atributos físicos visíveis a olho nu ou com o auxílio de uma lupa, sem a necessidade de um microscópio) e micromorfológicas (propriedades estruturais e anatômicas de um material que só podem ser observadas com o auxílio de um microscópio óptico ou eletrônico), são também exigidas47,48.
A determinação do teor de canabinoides, com ênfase, mas não excludente a CBD e THC, geralmente é realizada por CLAE-DAD, sendo fundamental para garantir a qualidade do medicamento em questão49. Outras análises que compõem os requisitos necessários para um medicamento de origem vegetal, são a determinação de pesticidas, a avaliação da presença de solventes residuais (realizadas por CG-EM), a determinação de metais pesados e o controle de qualidade microbiológico para verificar a presença de bactérias e ou fungos21. Como análises adicionais, estão testes que geralmente são aplicados a fitoterápicos, como a determinação de matéria orgânica estranha (onde não mais que 5,0% de caules com 3 mm ou mais de diâmetro e não mais que 2,0% de outros materiais estranhos estejam presentes); cinza total (não mais que 20%) e cinzas insolúveis em ácido (não mais que 4,0%)47.
É também necessário realizar estudos que comprovem a estabilidade do produto durante seu prazo de validade, assegurando que suas características permaneçam inalteradas ao longo do tempo. As informações presentes nos rótulos e embalagens devem estar em conformidade com as regulamentações, fornecendo dados claros sobre composição, concentração de canabinoides e instruções de uso. Após a comercialização, as empresas devem manter sistemas de farmacovigilância para monitorar e reportar quaisquer eventos adversos ou queixas técnicas relacionadas aos produtos.
Produtos e serviços capazes de trazer riscos à saúde são considerados de interesse da vigilância sanitária (VISA), que tem como objetivo desenvolver ações para eliminar, diminuir ou prevenir riscos à saúde e intervir em problemas sanitários decorrentes do meio ambiente, da produção e circulação de bens e da prestação de serviços de interesse da saúde50. A implementação desses procedimentos visa assegurar que os produtos à base de Cannabis disponíveis no mercado brasileiro atendam aos mais altos padrões de qualidade, proporcionando tratamentos seguros e eficazes para os pacientes. No âmbito dos medicamentos, as ações de VISA são aplicadas de acordo com a Lei 5.991 de 17 de dezembro de 1973, que dispõe sobre o controle sanitário do comércio de drogas, medicamentos, insumos farmacêuticos e correlatos e a Lei 6.360 de 23 de setembro de 1976, que dispõe sobre as normas de vigilância sanitária a que ficam sujeitos os medicamentos, as drogas, os insumos farmacêuticos e correlatos, os cosméticos, saneantes e outros produtos. Além destas, de acordo com a complexidade e etapa do ciclo de vida do produto, outras legislações, como Portarias e RDC da ANVISA, são aplicáveis51,52. Dentre as ações de VISA, avalia-se a qualidade de produtos através de análises que podem ser de natureza fiscal, de orientação ou de controle. Estas análises têm como objetivo diminuir a exposição da população a produtos que não atendam os requisitos de qualidade.
Portanto, para garantir a qualidade, eficácia e segurança dos produtos no âmbito sanitário à base de canabis, torna-se necessário quantificar os principais canabinoides utilizados para fins terapêuticos, CBD, THC, além dos canabinoides relacionados, como seus precursores, CBDA, THCA e o já conhecido produto de degradação do THC, o canabinol (CBN), que pode ocorrer dependendo das condições de armazenamento, temperatura e tempo5,53. Enquanto o THC e o CBD servem como indicadores do potencial das propriedades farmacológicas e toxicológicas dos extratos, seus precursores ácidos agem como parâmetros de avaliação da integridade da matéria-prima vegetal sendo seu monitoramento de interesse para a linha de produção5. O CBN é um produto de degradação do THC por descarboxilações sequenciais na presença de luz, calor e oxigênio, sendo um analito de interesse para o controle de qualidade como um parâmetro de degradação e um marcador do envelhecimento vegetal34.
Desafios no controle de qualidade
O desenvolvimento de um método farmacopeico torna-se imprescindível para estabelecer os requisitos mínimos de qualidade dos produtos que estão sendo comercializados no Brasil com fins terapêuticos, principalmente produzidos de forma artesanal pelas associações de pacientes, e os de importação individual, que não são autorizados ou registrados pela ANVISA. Sendo assim, o controle de qualidade através da verificação analítica destes produtos auxiliará na redução dos possíveis riscos sanitários.
Conforme avanços judiciais ocorrem, os métodos de avaliação de risco e de controle de qualidade devem evoluir e serem padronizados paralelamente, assim como o monitoramento e a fiscalização desses insumos farmacêuticos para a saúde pública4. A efeito comparativo, a regulamentação da canabis deve promover novos desafios ao ramo forense e aos setores farmacotoxicológicos de forma análoga a novos avanços no setor alimentício e na indústria do tabaco5,34. Isto ocorre porque mais de quarenta tipos diferentes de produtos derivados de canabis se encontram disponíveis comercialmente. Os extratos oleosos são fabricados de forma simples, não-laboriosa e não-padronizada, sendo suscetíveis a variações de processo e acarretando produtos com distinções de formulação, de eficiência e de teores13.
A diversidade físico-química e de atividade dos metabólitos da C. sativa representam um inestimável potencial farmacêutico. Atualmente, mais de seiscentas variantes vegetais da planta são reconhecidas e se encontram disponíveis, provendo acesso a uma infinidade de extratos medicinais que podem ser formulados com composições farmacologicamente complexas4. No entanto, para a completa elucidação dessa matriz e das propriedades a serem aproveitadas clinicamente, diversos elementos devem ser acessados, como as vias metabólicas e a integridade dos produtos de biossíntese. Este conhecimento é importante tanto pela garantia de segurança dos produtos desenvolvidos quanto para a elaboração de protocolos mais adequados no que se refere a práticas de cultivo e processos preparativos que viabilizem o desenvolvimento de novas tecnologias4,5.
Conclusão
O controle de qualidade e a regulamentação de produtos medicinais à base de C. sativa no Brasil representam desafios complexos, mas essenciais para garantir a segurança, eficácia e padronização desses produtos. A crescente demanda por terapias baseadas em canabinoides reforça a necessidade de um arcabouço regulatório sólido, aliado a técnicas analíticas avançadas que assegurem a qualidade dos produtos disponíveis no mercado.
A regulamentação brasileira, ainda em evolução, busca equilibrar o acesso a tratamentos inovadores com o rigor científico necessário para garantir a eficácia e a segurança dos medicamentos. No entanto, obstáculos como a ausência de normativas específicas, a falta de padronização nos métodos de cultivo e extração, e a variabilidade na composição dos produtos representam desafios para o setor.
Dessa forma, aprimorar o controle de qualidade, investir em pesquisas e avançar na regulamentação são passos fundamentais para consolidar o uso seguro e eficaz dos produtos medicinais à base de canabis no Brasil. O desenvolvimento de políticas mais estruturadas associadas a desconstrução do preconceito associado ao uso, e a ampliação dos estudos clínicos permitirão avanços significativos na oferta de medicamentos confiáveis, beneficiando pacientes e profissionais da saúde e promovendo uma maior integração da canabis medicinal ao sistema de saúde brasileiro.
Referências
- 1 Mariotti KC, Marcelo MCA, Ortiz RS, Borille BT, Reis M, Fett MS, et al. Seized cannabis seeds cultivated in greenhouse: A chemical study by gas chromatography-mass spectrometry and chemometric analysis. Sci Justice. 2016; 56(1): 35-41. Available in: [ https://doi.org/10.1016/j.scijus.2015.09.002 ].
» https://doi.org/10.1016/j.scijus.2015.09.002 - 2 Oga S, Camargo MMA, Batistuzzo JAO. Fundamentos de toxicologia. São Paulo: Atheneu; 2008.
- 3 Friedman D, Sirven JI. Historical perspective on the medical use of cannabis for epilepsy: Ancient times to the 1980s. Epilepsy Behav. 2017; 70: 298-301. Available in: [ https://pubmed.ncbi.nlm.nih.gov/28089286/ ]
» https://pubmed.ncbi.nlm.nih.gov/28089286/ - 4 Aliferis KA , Bernard-Perron D . Cannabinomics: Application of Metabolomics in Cannabis ( Cannabis sativa L.) research and Development. Front Plant Sci. 2020; 11: 554. Available in: [ https://doi.org/10.3389/fpls.2020.00554 ].
» https://doi.org/10.3389/fpls.2020.00554 - 5 Nie B, Henion J, Ryona I. The Role of Mass Spectrometry in the Cannabis Industry. J Am Soc Mass Spectrom. 2019; 30(5): 719-30. Available in: [ https://doi.org/10.1007/s13361-019-02164-z ].
» https://doi.org/10.1007/s13361-019-02164-z - 6 Stearn WT. Typification of Cannabis Sativa L. Bot Mus Lealf Harv Univ. [acesso em: 13 mar 2025] 1974; 23(9): 325-36. Available in: [ http://www.jstor.org/stable/41762284 ].
» http://www.jstor.org/stable/41762284 - 7 Nascimento IR, Costa HB, Souza LM, Soprani LC, Merlo BB, Romão W. Chemical identification of cannabinoids in street marijuana samples using electrospray ionization FT-ICR mass spectrometry. Anal Methods. 2015; 7(4): 1415-24. Available in: [ https://doi.org/10.1039/C4AY02355B ].
» https://doi.org/10.1039/C4AY02355B - 8 Carlini, Elisaldo; Rodrigues, Eliana; Galduróz JCF. Cannabis e Substâncias Cannabinóides em Medicina. Brasília, DF: Secretaria Nacional Antidrogas - SENAD; 2004.
- 9 Honório KM, Arroio A, Da Silva ABF. Aspectos terapêuticos de compostos da planta Cannabis sativa Quim Nova. 2006; 29(2): 318-25. Disponível em: [ https://doi.org/10.1590/S0100-40422006000200024 ].
» https://doi.org/10.1590/S0100-40422006000200024 - 10 ElSohly MA, Slade D. Chemical constituents of marijuana: The complex mixture of natural cannabinoids. Life Sci. 2005; 77(6): 539-48. Available in: [ https://doi.org/10.1016/j.lfs.2005.09.011 ].
» https://doi.org/10.1016/j.lfs.2005.09.011 - 11 Karch SB. Marijuana and the cannabinoids. Totowa, New Jersey: Editora Humana Press; 2007. [acesso em: 20 fev 2025]. Disponível em: [ www.humanapress.com ].
» www.humanapress.com - 12 Novotny M, Lee ML, Low CE, Raymond A. Analysis of marijuana samples from different origins by high-resolution gas-liquid chromatography for forensic application. Anal Chem. 1976; 48(1): 24-9. Available in: [ https://doi.org/10.1021/AC60365A039 ].
» https://doi.org/10.1021/AC60365A039 - 13 Deidda R, Avohou HT, Baronti R, Davolio PL, Pasquini B, Del Bubba M, et al. Analytical quality by design: Development and control strategy for a LC method to evaluate the cannabinoids content in cannabis olive oil extracts. J Pharm Biomed Anal. 2019; 166: 326-35. Available in: [ https://doi.org/10.1016/j.jpba.2019.01.032 ].
» https://doi.org/10.1016/j.jpba.2019.01.032 - 14 Meng Q , Buchanan B , Zuccolo J , Poulin MM , Gabriele J , Baranowski DC . A reliable and validated LC-MS/MS method for the simultaneous quantification of 4 cannabinoids in 40 consumer products. PLoS One. 2018; 13(5). Available in: [ https://doi.org/10.1371/journal.pone.0196396 ].
» https://doi.org/10.1371/journal.pone.0196396 - 15 Radwan MM, ElSohly MA, El-Alfy AT, Ahmed SA, Slade D, Husni AS, et al. Isolation and Pharmacological Evaluation of Minor Cannabinoids from High-Potency Cannabis sativa. J Nat Prod. 2015; 78(6): 1271-6. Available in: [ https://doi.org/10.1021/acs.jnatprod.5b00065 ].
» https://doi.org/10.1021/acs.jnatprod.5b00065 - 16 Wang M, Wang YH, Avula B, Radwan MM, Wanas AS, Mehmedic Z, et al. Quantitative Determination of Cannabinoids in Cannabis and Cannabis Products Using Ultra-High-Performance Supercritical Fluid Chromatography and Diode Array/Mass Spectrometric Detection. J Forensic Sci. 2017; 62(3): 602-11. Available in: [ https://doi.org/10.1111/1556-4029.13341 ].
» https://doi.org/10.1111/1556-4029.13341 - 17 Radwan MM, Chandra S, Gul S, Elsohly MA. Cannabinoids, phenolics, terpenes and alkaloids of cannabis. Molecules. 2021; 26(9). Available in: [ https://doi.org/10.3390/molecules26092774 ].
» https://doi.org/10.3390/molecules26092774 - 18 De Backer B, Maebe K, Verstraete AG, Charlier C. Evolution of the Content of THC and Other Major Cannabinoids in Drug-Type Cannabis Cuttings and Seedlings During Growth of Plants. J Forensic Sci. 2012; 57(4): 918-22. Available in: [ https://doi.org/10.1111/j.1556-4029.2012.02068.x ].
» https://doi.org/10.1111/j.1556-4029.2012.02068.x - 19 Shibuya EK, Souza Sarkis JE, Neto ON, Moreira MZ, Victoria RL. Sourcing Brazilian marijuana by applying IRMS analysis to seized samples. Forensic Sci Int. 2006; 160(1): 35-43. Available in: [ https://doi.org/10.1016/j.forsciint.2005.08.011 ].
» https://doi.org/10.1016/j.forsciint.2005.08.011 - 20 De Backer B, Debrus B, Lebrun P, Theunis L, Dubois N, Decock L, et al. Innovative development and validation of an HPLC/DAD method for the qualitative and quantitative determination of major cannabinoids in cannabis plant material. J Chromatogr B Anal Technol Biomed Life Sci. 2009; 877(32): 4115-24. Available in: [ https://doi.org/10.21577/0100-4042.20170457 ].
» https://doi.org/10.21577/0100-4042.20170457 - 21 Vanhove W, Van Damme P, Meert N. Factors determining yield and quality of illicit indoor cannabis ( Cannabis spp) production. Forensic Sci Int. 2011; 212(1-3): 158-63. Available in: [ https://doi.org/10.1016/j.forsciint.2011.06.006 ].
» https://doi.org/10.1016/j.forsciint.2011.06.006 - 22 Broséus J, Anglada F, Esseiva P. The differentiation of fibre- and drug type Cannabis seedlings by gas chromatography/mass spectrometry and chemometric tools. Forensic Sci Int. 2010; 200(1-3): 87-92. Available in: [ https://doi.org/10.1016/j.forsciint.2010.03.034 ].
» https://doi.org/10.1016/j.forsciint.2010.03.034 - 23 Hazekamp A. Cannabis: extracting the medicine. 2007. [acesso em: 13 mar 2025]. Available in: [ https://hdl.handle.net/1887/12297 ].
» https://hdl.handle.net/1887/12297 - 24 United Nations Office On Drugs And Crime. Identification and analysis of Cannabis and Cannabis products. Vienna. 2022. [acesso em: 20 fev 2025]. Disponível em: [ https://www.unodc.org/documents/scientific/Recommended_methods_for_the_Identification_and_Analysis_of_Cannabis_and_Cannabis_products.pdf ].
» https://www.unodc.org/documents/scientific/Recommended_methods_for_the_Identification_and_Analysis_of_Cannabis_and_Cannabis_products.pdf - 25 Borrelli F, Fasolino I, Romano B, Capasso R, Maiello F, Coppola D, et al. Beneficial effect of the non-psychotropic plant cannabinoid cannabigerol on experimental inflammatory bowel disease. Biochem Pharmacol. 2013; 85(9): 1306-16. Available in: [ https://doi.org/10.1016/j.bcp.2013.01.017 ]
» https://doi.org/10.1016/j.bcp.2013.01.017 - 26 Tran J, Elkins AC, Spangenberg GC, Rochfort SJ. High-Throughput Quantitation of Cannabinoids by Liquid Chromatography Triple-Quadrupole Mass Spectrometry. Molecules. 2022; 27(3). Available in: [ https://doi.org/10.3390/molecules27030742 ].
» https://doi.org/10.3390/molecules27030742 - 27 Gross JH. Mass Spectrometry. 2017 [acesso em: 20 fev 2025]. Available in: [ http://link.springer.com/10.1007/978-3-319-54398-7 ].
» http://link.springer.com/10.1007/978-3-319-54398-7 - 28 Christinat N , Savoy MC , Mottier P . Development, validation and application of a LC-MS/MS method for quantification of 15 cannabinoids in food. Food Chem. 2020; 318: 126469. Available in: [ https://doi.org/10.1016/j.foodchem.2020.126469 ].
» https://doi.org/10.1016/j.foodchem.2020.126469 - 29 McRae G, Melanson JE. Quantitative determination and validation of 17 cannabinoids in cannabis and hemp using liquid chromatography-tandem mass spectrometry. Anal Bioanal Chem. 2020; 412(27): 7381-93. [ https://doi.org/10.1007/s00216-020-02862-8 ]
» https://doi.org/10.1007/s00216-020-02862-8 - 30 Citti C , Braghiroli D , Vandelli MA , Cannazza G . Pharmaceutical and biomedical analysis of cannabinoids: A critical review. J Pharm Biomed Anal. 2018; 147: 565-79 . Available in: [ https://doi.org/10.1016/j.jpba.2017.06.003 ]
» https://doi.org/10.1016/j.jpba.2017.06.003 - 31 Leghissa A, Hildenbrand ZL, Schug KA. A review of methods for the chemical characterization of Cannabis natural products. J Sep Sci. 2018; 41(1): 398-415. Available in: [ https://doi.org/10.1002/jssc.201701003 ]
» https://doi.org/10.1002/jssc.201701003 - 32 Sisco E , Forbes TP . Forensic applications of DART-MS: A review of recent literature. Forensic Chem. 2021; 22. Available in: [ https://doi.org/10.1016/j.forc.2020.100294 ]
» https://doi.org/10.1016/j.forc.2020.100294 - 33 Dos Santos NA, Ortiz RS, Limberger RP, Lacerda Junior V, Romão W. Identification of ?9-tetrahydrocannabinol (?9-THC) in Cannabis seeds by electrospray ionization fourier transform ion cyclotron resonance mass spectrometry (ESI(-)FT-ICR MS). Orbital. 2018; 10(5): 381-5. Available in: [ https://doi.org/10.17807/orbital.v10i5.1149 ].
» https://doi.org/10.17807/orbital.v10i5.1149 - 34 Carvalho VM, Aguiar AFL, Baratto LC, Souza FLC, Rocha ED. Cannabinoids quantification in medicinal cannabis extracts by high performance liquid chromatography. Quim Nova. 2020; 43(1): 90-7. Available in: [ https://doi.org/10.21577/0100-4042.20170457 ].
» https://doi.org/10.21577/0100-4042.20170457 - 35 Johnson R . Hemp as an Agricultural Commodity. 2018. Available in: [ https://fas.org/sgp/crs/misc/RL32725.pdf ] .
» https://fas.org/sgp/crs/misc/RL32725.pdf - 36 Farinon B, Molinari R, Costantini L, Merendino N. The seed of industrial hemp ( Cannabis sativa l.): Nutritional quality and potential functionality for human health and nutrition. Nutrients. 2020; 12(7): 1-60. Available in: [ https://doi.org/10.3390/nu12071935 ].
» https://doi.org/10.3390/nu12071935 - 37 Brasil. Ministério da Saúde. Agência Nacional de Vigilância Sanitária (ANVISA). Portaria N o 344, de 12 de maio de 1998. Aprova o Regulamento Técnico sobre substâncias e medicamentos sujeitos a controle especial. 1998. [acesso em: 22 fev 2025]. Disponível em: [ https://bvsms.saude.gov.br/bvs/saudelegis/svs/1998/prt0344_12_05_1998_rep.html ].
» https://bvsms.saude.gov.br/bvs/saudelegis/svs/1998/prt0344_12_05_1998_rep.html - 38 ANVISA AN de VS. Registrado primeiro medicamento à base de Cannabis sativa. A solução oral Mevatyl ® será Destinado ao Tratamento clínico em pacientes não responsivos a Medicam. antiespásticos. 2017 [acesso em: 22 fev 2025]. Disponível em: [ https://www.gov.br/anvisa/pt-br/assuntos/noticias-anvisa/2018/registrado-primeiro-medicamento-a-base-de-cannabis-sativa ].
» https://www.gov.br/anvisa/pt-br/assuntos/noticias-anvisa/2018/registrado-primeiro-medicamento-a-base-de-cannabis-sativa - 39 Brasil. Ministério da Saúde. Agência Nacional de Vigilância Sanitária (ANVISA). Lei n o 13.840, de 5 de junho de 2019 - Nova Lei de Drogas. 2019 [acesso em: 22 fev 2025]. Disponível em: [ https://www.planalto.gov.br/ccivil_03/_ato2019-2022/2019/lei/l13840.htm ]
» https://www.planalto.gov.br/ccivil_03/_ato2019-2022/2019/lei/l13840.htm - 40 Verma R, Hoda F, Arshad M, Iqubal A, Siddiqui AN, Khan MA, et al. Cannabis, a Miracle Drug with Polyvalent Therapeutic Utility: Preclinical and Clinical-Based Evidence. Med Cannabis Cannabinoids. 2021; 4(1): 43-60. Available in: [ https://doi.org/10.1159/000515042 ].
» https://doi.org/10.1159/000515042 - 41 Brasil. Ministério da Saúde. Agência Nacional de Vigilância Sanitária (ANVISA). Anvisa aprova novo produto de Cannabis a ser fabricado no Brasil. 2022. [acesso em: 22 fev 2025]. Disponível em: [ https://www.gov.br/anvisa/pt-br/assuntos/noticias-anvisa/2022/anvisa-aprova-novo-produto-de-cannabis-a-ser-fabricado-no-brasil ]
» https://www.gov.br/anvisa/pt-br/assuntos/noticias-anvisa/2022/anvisa-aprova-novo-produto-de-cannabis-a-ser-fabricado-no-brasil - 42 Brasil. Ministério da Saúde. Agência Nacional de Vigilância Sanitária (ANVISA). Lei n° 89, de 2023 - Institui a Política Nacional de Fornecimento Gratuito de Medicamentos Formulados de Derivado Vegetal à Base de Canabidiol, em associação com outras substâncias canabinoides, incluindo o tetrahidrocanabinol. 2023 [acesso em: 22 fev 2025]. Disponível em: [ https://legis.senado.leg.br/sdleg-getter/documento?dm=9251801&ts=1681737802431&disposition=inline ].
» https://legis.senado.leg.br/sdleg-getter/documento?dm=9251801&ts=1681737802431&disposition=inline - 43 Brasil. Ministério da Saúde. Agência Nacional de Vigilância Sanitária (ANVISA). Produtos à base de Cannabis poderão ser regularizados para uso em animais. 2024 [acesso em: 22 fev 2025]. Disponível em: [ https://www.gov.br/anvisa/pt-br/assuntos/noticias-anvisa/2024/produtos-a-base-de-cannabis-poderao-ser-regularizados-para-uso-em-animais ].
» https://www.gov.br/anvisa/pt-br/assuntos/noticias-anvisa/2024/produtos-a-base-de-cannabis-poderao-ser-regularizados-para-uso-em-animais - 44 Brasil. Senado Federal. Congresso pode decidir sobre plantio e comercialização de Cannabis medicina. [acesso em: 22 fev 2025]. Disponível em: [ https://www12.senado.leg.br/noticias/materias/2025/02/18/congresso-pode-decidir-sobre-plantio-e-comercializacao-de-cannabis-medicinal ].
» https://www12.senado.leg.br/noticias/materias/2025/02/18/congresso-pode-decidir-sobre-plantio-e-comercializacao-de-cannabis-medicinal - 45 Brasil. Ministério da Saúde. Agência Nacional de Vigilância Sanitária-ANVISA. Resolução RDC nº 658, de 8 de março de 2022. - Estabelece requisitos para a produção, comercialização e controle de medicamentos derivados da cannabis [acesso em: 22 fev 2025]. Disponível em: [ https://www.gov.br/anvisa/pt-br/assuntos/noticias-anvisa/2022/rdc658 ].
» https://www.gov.br/anvisa/pt-br/assuntos/noticias-anvisa/2022/rdc658 - 46 Brasil. Resolução RDC nº 16, de 18 de fevereiro de 2014 - Dispõe sobre o registro de medicamentos à base de Cannabis [acesso em: em: 22 fev 2025]. Disponível em: [ https://www.gov.br/anvisa/pt-br/assuntos/rdc16 ].
» https://www.gov.br/anvisa/pt-br/assuntos/rdc16 - 47 Brasil. Ministério da Saúde. Agência Nacional de Vigilância Sanitária-ANVISA. Farmacopeia Brasileira. 5ª ed. Brasília, DF: Agência Nacional de Vigilância Sanitária; 2010.
- 48 Peschel W. Quality control of traditional Cannabis tinctures: Pattern, markers, and stability. Sci Pharm. 2016; 84(3): 567-84. Available in: [ https://doi.org/10.3390/scipharm84030567 ]
» https://doi.org/10.3390/scipharm84030567 - 49 Wang YH, Avula B, Elsohly MA, Radwan MM, Wang M, Wanas AS, et al. Quantitative Determination of ? 9 -THC, CBG, CBD, Their Acid Precursors and Five Other Neutral Cannabinoids by UHPLC-UV-MS. Pl Med. 2018; 84(4): 260-6. Available in: [ https://doi.org/10.1055/s-0043-124873 ].
» https://doi.org/10.1055/s-0043-124873 - 50 Brasil. Ministério da Saúde. Agência Nacional de Vigilância Sanitária-ANVISA. Lei nº 8.080, de 19 de setembro de 1990. Dispõe sobre as condições para a promoção, proteção e recuperação da saúde, a organização e o funcionamento dos serviços correspondentes.1990 [acesso em: 22 fev 2025]. Diário Oficial da União, Brasília, DF. Disponível em: [ https://www.planalto.gov.br/ccivil_03/LEIS/L8080.htm ].
» https://www.planalto.gov.br/ccivil_03/LEIS/L8080.htm - 51 Brasil. Ministério da Saúde. Agência Nacional de Vigilância Sanitária-ANVISA. Lei nº 5.991, de 17 de dezembro de 1973. Dispõe sobre o controle sanitário do comércio de medicamentos, drogas, insumos farmacêuticos e correlatos. 1973 [acesso em: 22 fev 2025]. Diário Oficial da União, Brasília, DF. Disponível em: [ https://www.planalto.gov.br/ccivil_03/Leis/L5991.htm ].
» https://www.planalto.gov.br/ccivil_03/Leis/L5991.htm - 52 Brasil. Ministério da Saúde. Agência Nacional de Vigilância Sanitária-ANVISA. Lei nº 6.360, de 23 de setembro de 1976. Dispõe sobre a vigilância sanitária a que ficam sujeitos os produtos, substâncias e objetos sujeitos à fiscalização sanitária.1976. [acesso em: 22 fev 2025]. Diário Oficial da União, Brasília, DF. Disponível em: [ https://www.planalto.gov.br/ccivil_03/LEIS/L6360.htm ].
» https://www.planalto.gov.br/ccivil_03/LEIS/L6360.htm - 53 Lewis MM, Yang Y, Wasilewski E, Clarke HA, Kotra LP. Chemical Profiling of Medical Cannabis Extracts. ACS Omega. 2017; 2(9): 6091-103. Available in: [ https://doi.org/10.1021/acsomega.7b00996 ].
» https://doi.org/10.1021/acsomega.7b00996
-
Fonte de Financiamento:
Não houve financiamento.
Datas de Publicação
- Publicação nesta coleção
02 Mar 2026 - Data do Fascículo
Mar 2026
Histórico
- Recebido
17 Jun 2025 - Aceito
05 Nov 2025
 Controle de Qualidade e Regulamentação de Produtos Medicinais à Base de Cannabis no Brasil
Controle de Qualidade e Regulamentação de Produtos Medicinais à Base de Cannabis no Brasil