Resumo
A pandemia da COVID-19, causada pelo SARS-CoV-2, destacou a importância da busca por novas abordagens terapêuticas, especialmente frente à rápida disseminação do vírus, à limitação de tratamentos eficazes e ao surgimento de novas variantes. O SARS-CoV-2 utiliza mecanismos de entrada celular mediados pela proteína Spike (S) e, após infecção, depende da ação de proteases virais essenciais — como a Mpro (protease principal) e PLpro (protease tipo papaína) — para sua replicação. Esses alvos se tornaram estratégicos para o desenvolvimento de novos fármacos antivirais. Neste contexto, os produtos naturais e seus derivados, como o ácido gálico (AG), emergem como alternativas promissoras, por serem amplamente reconhecido por suas propriedades antioxidantes, anti-inflamatórias e antivirais. Este artigo de revisão explora os mecanismos de replicação das proteases do SARS-CoV-2 e discute o potencial terapêutico do AG e seus derivados, como candidatos promissores a inibidores virais contra as proteases do SARS-CoV-2. Os dados significativos foram coletados de diferentes bancos de dados (PubMed, Scopus, Science Direct e Web os Science), usando palavras chaves como ácido gálico, SARS CoV-2 e inibidores de proteases. Estudos in sílico e in vitro tem demonstrado que o AG e seus derivados podem atuar como inibidores potenciais das proteases Mpro e PLpro do SARS-CoV-2.
Palavras-chave: Ácido gálico; SARS-CoV-2; inibidores de proteases
Abstract
The COVID-19 pandemic, caused by SARS-CoV-2, has highlighted the importance of seeking new therapeutic approaches, especially in light of the rapid spread of the virus, the limited availability of effective treatments, and the emergence of new variants. SARS-CoV-2 uses cell entry mechanisms mediated by the Spike (S) protein and, after infection, depends on the action of essential viral proteases—such as Mpro (main protease) and PLpro (papain-like protease)—for its replication. These targets have become strategic for the development of new antiviral drugs. In this context, natural products and their derivatives, such as gallic acid (GA), emerge as promising alternatives, as they are widely recognized for their antioxidant, anti-inflammatory, and antiviral properties. This review article explores the replication mechanisms of SARS-CoV-2 proteases and discusses the therapeutic potential of GA and its derivatives as promising candidates for viral inhibitors against SARS-CoV-2 proteases. Significant data were collected from different databases (PubMed, Scopus, Science Direct, and Web of Science) using keywords such as gallic acid, SARS-CoV-2, and protease inhibitors. In silico and in vitro studies have shown that GA and its derivatives can act as potential inhibitors of the Mpro and PLpro proteases of SARS-CoV-2.
Keywords: Gallic acid; SARS-CoV-2; protease inhibitors
Introdução
Doenças infecciosas provocadas por vírus, são doenças causadas por um agente nocivo (patógeno) em um hospedeiro em condições favoráveis. A infecção viral provoca a subversão das funções celulares nos hospedeiros, o qual pode ou não apresentar sinais ou sintomas clínicos[1]. A incidência da doença entre os infectados varia muito, podendo causar o que chamamos de síndrome, que consiste em um grupo de sinais e sintomas específicos. Sendo assim, podemos considerar que o tipo de alteração clínica, depende do patógeno específico e da suscetibilidade individual do hospedeiro[2].
Segundo Lemos et al.[3], pesquisadores da Fiocruz, no livro Tópicos em Virologia, a replicação viral consiste nas seguintes etapas: • Adsorção • Penetração do agente viral; • Desnudamento; • Expressão gênica (transcrição e tradução); • Replicação do genoma; • Maturação; • Liberação. O ciclo de infecção de um vírus começa pela ligação de uma proteína de superfície do vírus invasor a um receptor expresso na superfície de uma célula hospedeira (por adsorção)[4,5]. Após a fixação, ocorre a penetração do genoma viral no citoplasma, quando o envelope viral se funde diretamente com a membrana celular, ou em alguns casos, uma partícula viral penetra no interior da célula por endocitose[5,6].
Uma vez dentro da célula, o genoma infectante é liberado e transportado para o núcleo ou permanece no citoplasma, onde é transcrito em mRNA pelo RNA polimerase celular, para que a replicação do RNA viral prossiga. O mRNA direciona a célula hospedeira para sintetizar enzimas virais e para montar novos vírions infeciosos, a partir de moléculas biológicas sintetizadas. Na etapa de maturação ocorre a formação de partículas virais completas ou vírions, que em 29 seguida são liberadas no ambiente extracelular, onde podem infectar células adjacentes ou repetir o ciclo de replicação[7,8].
A capacidade de resposta imunológica a um antígeno viral depende da interação entre a virulência do vírus e a resposta imune do hospedeiro. Indivíduos com uma fraca resposta imunitária teriam, supostamente, dificuldades em controlar a infecção. Existe uma relação direta entre a constituição genética do hospedeiro e fatores fisiológicos (fatores nutricionais, idade, hormônios, estresse, gravidez, entre outros) com a resposta imunológica específica[9,10].
A transmissão de um agente viral pode ser de forma direta, de um hospedeiro para outro (contato físico e por secreção) e de forma indireta, através da manipulação de objetos contaminados, picada de artrópodes (vetor), pequenas lesões, mordida de animais e iatrogênica (intervenção humana)[11].
Um surto epidêmico causado por vírus, pode estar relacionado às mudanças nas características da interação patógeno-hospedeiro-ambiente[12]. Mudanças no ambiente hospedeiro (conjunto global de fatores, como: poluição, mudança climática, perda de biodiversidade e expansão da produção animal)[13], e na ecologia da doença (mutação ou modificação no reservatório do agente patogênico), são fundamentais para criar novos padrões de transmissão e seleção de novos patógenos com características genéticas distintas[14].
Novos vírus, emergentes ou não, são capazes de transmissão rápida por não haver resposta imune do hospedeiro ou vacinas disponíveis. Nesse contexto, quando um determinado agente se dissemina em diversos países e continentes, afetando um grande número de pessoas a nível mundial, essa doença se torna uma pandemia, segundo a Portaria nº 2259 de 23/11/2005/MS – Ministério da Saúde.
De todos os agentes patogênicos, o vírus é particularmente comum, na causa de pandemias. Desde o século XX, o enfrentamento de epidemias e pandemias de vírus se tornou possível graças à difusão de saneamento básico e pela intervenção de medicamentos e vacinas. A primeira pandemia de gripe, também conhecida como Influenza A (H1N1) ou Gripe Espanhola foi relatada em 1918, em termos numéricos, cerca de 500 milhões de pessoas foram infectadas e em torno de 50 a 100 milhões foram a óbito até 1919. Com outras variáveis durante o século XX, a gripe ocasionou outros surtos pandêmicos nos anos de 1957 (Influenza A (H2N2) e 1968 (influenza A 30 (H3N2)), conhecidas como gripe asiáticas. Já em 2009, autoridades sanitárias mexicanas identificaram uma nova cepa do vírus Influenza A, responsável por causar a pandemia da gripe espanhola entre os anos de 1918 e 1920. A doença foi designada como “Gripe suína”, por conter ADN (ácido desoxirribonucleico) típico de vírus suínos. O surto logo evoluiu para uma pandemia e começou a se espalhar por 75 países em todos os continentes[15-18].
Já no século XXI, as três principais pandemias virais envolveram vírus da família Coronaviridae, capazes de causar infecções emergentes associadas a quadros graves de insuficiência respiratória em humanos, causadores de SARS: Severe acute Respiratory Syndrome ou Síndrome Respiratória Aguda Severa (SARS CoV) (2002), Middle East Respiratory Syndrome ou Síndrome Respiratória do Oriente Médio (MERS-CoV) (2012) e Severe acute Respiratory Syndrome Coronavirus 2 ou Síndrome Respiratória Aguda Severa Coronavírus 2 (SARS-CoV-2) (2019)[19]. Diante deste contexto, este artigo de revisão tem como objetivo, explorar os mecanismos de replicação das proteases do SARS-CoV-2 e discutir o potencial terapêutico dos derivados de produtos naturais, com ênfase no Acido Gálico (AG) e seus derivados, como candidatos promissores à inibidores virais contra as proteases do SARS-CoV-2.
Metodologia
Este estudo foi realizado através de uma revisão bibliográfica, com base na pesquisa de publicações que abordam a temática. A busca foi realizada nas bases de dados (PubMed, Scopus, Science Direct e Web os Science), usando palavras chaves como ácido gálico, SARS CoV-2, derivados do ácido gálico e inibidores de proteases. Foram consideradas publicações em português e inglês.
Resultados e discussões
Pandemia da COVID-19
Em dezembro de 2019, as autoridades de saúde da China alertaram a OMS (Organização Mundial de Saúde) sobre o grande número de casos de pneumonia de etiologia desconhecida, na cidade de Wuhan, na província de Hubei. A maioria dos casos foram relatados por pacientes que trabalhavam ou viviam no mercado de frutos do mar do local. Até final de janeiro de 2020, haviam sido confirmados 7.736 casos e 12.167 casos suspeitos na China e 82 casos confirmados em 18 países, levando a OMS declarar o surto de SARS-CoV-2 como uma Emergência de Saúde Pública de Importância Internacional (ESPII). Este patógeno foi nomeado como coronavírus 2 da Síndrome Respiratória Aguda Grave (SARS-CoV-2) e a doença foi denominada como coronavírus 2019 (COVID-19) pela OMS[20,21].
A infecção por SARS-CoV-2, o agente etiológico da COVID-19, já foi confirmada em mais de 765.903.278 pessoas ao redor do mundo, sendo responsável por mais de 716.626 óbitos no Brasil (Painel Coronavírus, 08 de setembro de 2025[22]. O surto da Covid-19 criou uma crise global de saúde pública por conta do contágio rápido e massivo da população e do potencial limitado de atendimento no sistema de saúde. Por isso, as medidas higiênicas preventivas como uso de máscara, distanciamento social e a higienização foram adotadas em um primeiro momento. Naquela ocasião, essas medidas foram motivadas também pela falta de tratamento eficaz contra a COVID-19, seja por fármacos ou por uma vacina.
O vírus
O vírus SARS-CoV-2 (abreviação de Severe Acute Respiratory Syndrome Coronavirus 2, sigla em inglês para Coronavírus da Síndrome Respiratória Aguda Grave 2), causador da COVID-19 (abreviação de Coronavírus Disease 2019), é um β coronavírus, membro da família Coronaviridae e pertence à ordem Nidovirales. São considerados o maior grupo de vírus de RNA de cadeia grande que causam infecções respiratórias. São vírus envelopados e de fita simples, cuja membrana lipídica externa é composta por no mínimo 4 proteínas estruturais, incluindo a proteína Spike (S), um tipo de glicoproteína que se projeta na membrana, dando ao vírus a forma característica de uma coroa (do latim: Corona)[23,24].
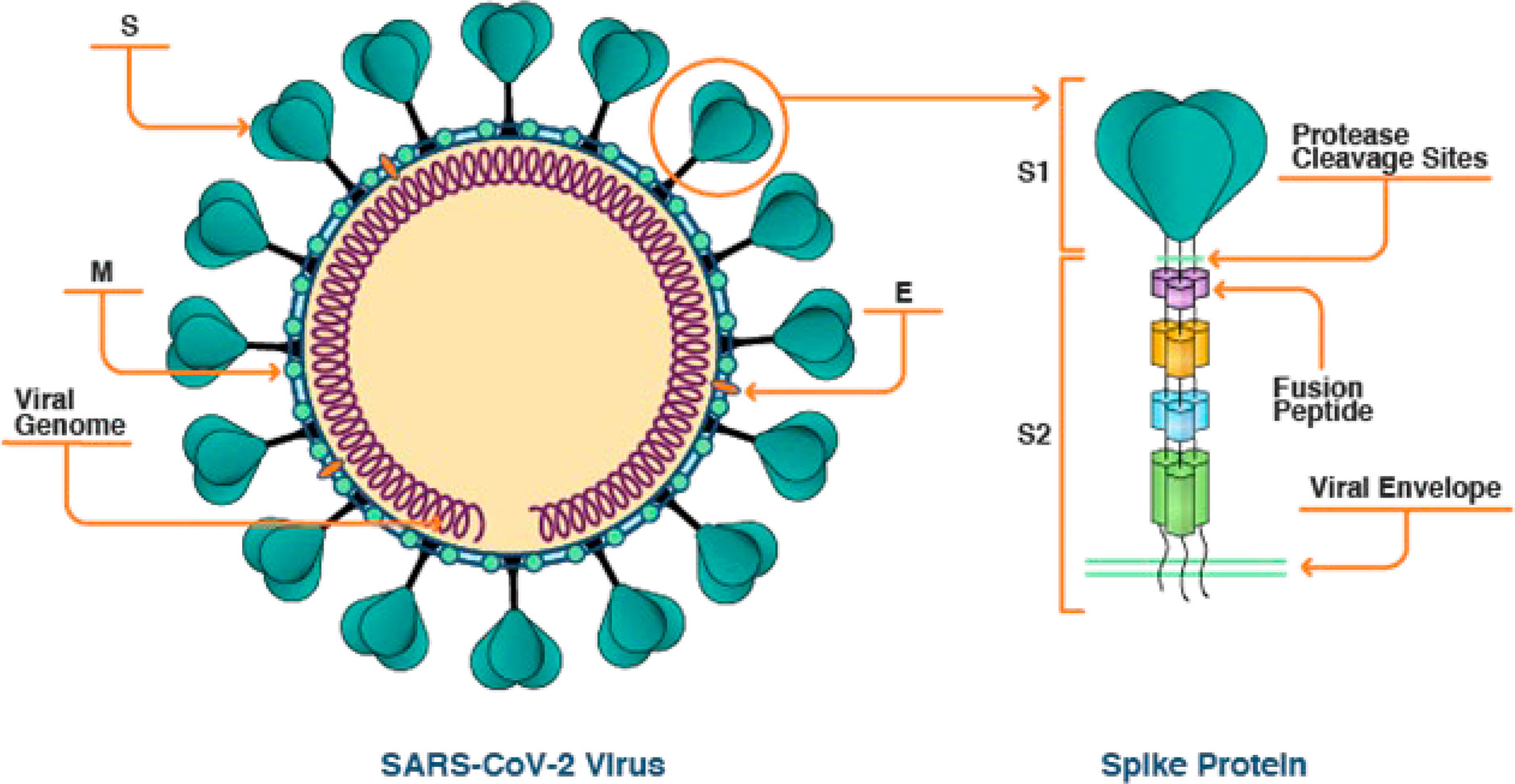
Do ponto de vista estrutural, esses vírus são circundados por um envelope contendo a proteína S que age como receptor do vírus, incluindo a proteína do nucleocapsídeo (N), responsável por envelopar o material genético viral, a proteína de membrana (M) e a proteína do envelope (E), presentes na superfície do envelope do virion. O genoma é empacotado em um nucleocapsídeo helicoidal, o qual confere um formato esférico. Os nucleocapsídeos consistem em uma sequência de RNA genômico associado à nucleoproteína N, cuja função é proteger o genoma viral. A presença de proteínas em sua superfície (proteína de adsorção viral), formam estruturas denominadas espículas, com um formato aparente de coroa, característica que dá origem ao nome coronavírus. Três proteínas S se unem para formar um trímero, que tem a forma de um “parafuso”. Esse “parafuso” é composto de uma cabeça chamada de subunidade S1, e a parte restante é chamada de subunidade S2, que está mais próxima da membrana viral (FIGURA 1)[25-28].
A entrada da partícula viral ocorre devido ao reconhecimento das espículas por receptores específicos, localizados na superfície da membrana plasmática da célula hospedeira[30]. Segundo Hu e colaboradores[31], o novo betacoronavírus partilha 79% de RNA genômico do SARS-CoV e 50% dos componentes estruturais que formam a partícula viral (S, E, M e N) do MERS-CoV, sugerindo que o mecanismo de infecção entre elas pode ser semelhante[31,32].
A transmissão do vírus ocorre pela secreção do sistema respiratório infectado, como fluídos salivares, partículas retidas sobre o ar em forma de aerossol de espirro ou tosse, contato com pessoas e superfícies contaminadas. As manifestações clínicas da COVID-19, vão desde indivíduos assintomáticos, até quadro de falência múltipla de órgãos e morte. Os sintomas mais comuns são: febre, tosse seca e falta de ar[33,34].
Mecanismo de infecção e replicação viral
A entrada do SARS-CoV-2 nas células hospedeiras humanas podem ocorrer por dois mecanismos: A) por internalização via endocitose e B) fusão do envelope viral com a membrana plasmática da célula hospedeira, ocorrendo no compartilhamento endossomal (FIGURA 2). Em ambos os casos, as subunidades S1 e S2 presentes na superfície do vírus medeiam a ligação e a entrada do vírus, ligando-se aos receptores 33 celulares do hospedeiro, como a enzima conversora de angiotensina 2 (ACE2)[25,35].
: Ciclo de vida do coronavírus: A) por internalização via endocitose; B) por fusão do envelope viral.
No primeiro mecanismo, por via endossomal, conforme FIGURA 2A, a proteína S1 se liga as proteínas ACE2 do hospedeiro, ocorrendo a fusão por via endocítica, em um ambiente acidificado, ocasionando a internalização do genoma viral no citoplasma da célula[36-38]. Por sua vez, no segundo mecanismo (FIGURA 2B), a glicoproteína S presente na superfície do vírus é clivada em dois locais pelas proteases do hospedeiro como as catepsinas, a tripsina humana de via área humana (HAT) e Transmembrana Serina 2 (TMPRRS2). O primeiro local é no limite das subunidades S1/S2, que reconhece e se liga à enzima ACE2, mediando a entrada do vírus na célula hospedeira. Em seguida, a subunidade S2, chamada de pré-fusão, ao entrar em contato com as proteases da célula hospedeira, passa por alterações conformacionais, tais como redução do pH, que facilitam a exposição da subunidade S2, ocasionando a fusão da partícula viral e a liberação do material genético do vírus no interior da célula[25,39-42].
Assim que o vírus entra na célula, o RNA viral é liberado e submetido à tradução imediata. Essa tradução sintetiza poliproteínas não estruturais individuais (pp1a e pp1ab), que translocam-se para as membranas do retículo endoplasmático (RE) onde interagem com o RNA genômico viral recentemente produzido, formando um complexo de replicação e transcrição viral. A replicação viral é iniciada pela transcrição de cópias genômicas que em seguida são secretadas pela célula infectada por exocitose[35,43-45].
A liberação do genoma do coronavírus no citoplasma da célula hospedeira após a entrada, marca o início de um sistema complexo de expressão gênica viral. Dezesseis proteínas não estruturais são liberadas, co-traduzidas e pós-traduzidas em duas longas fitas polipeptídicas, denominadas pp1a (nsp1-11) e pp1ab (nsp1-10, nsp12-16), que sofrem clivagem proteolítica por duas proteases de cisteína que estão localizadas dentro de nsp3 (PLpro, protease semelhante à papaína) e nsp5 (protease semelhante à quimotripsina), contudo, frequentemente referida como protease tipo 3C (3CLpro) ou como protease principal (Mpro), responsável pelo processamento proteolítico da maioria das poliproteínas nos locais de clivagem. A Mpro é uma protease correspondente à nsp5, responsável pela clivagem das poliproteínas (nsps) em 11 sítios conservados, envolvendo a sequência de aminoácidos Leu-Gln/Ser-Ala-Gly, no qual a clivagem acontece entre os sítios Gln e Ser [46,47].
As proteínas não estruturais (nsp) constituem o complexo viral conhecido como complexo replicação-transcrição (RTC, do inglês replicase-transcriptase complex), que possuem domínios e funções enzimáticas específicas. Todas as nsp’s contribuem para a construção de um ambiente favorável à síntese de RNA viral. Todas as 35 proteínas estruturais ou não estruturais são cruciais para a formação da estrutura do SARS-CoV-2, especialmente as proteínas S, a PLpro e a Mpro, as quais são interessantes candidatas para alvos terapêuticos contra o SARS-CoV-2[48-52].
Uso de produtos naturais como fontes de medicamentos
O uso de produtos naturais exclusivamente de plantas para fins terapêuticos é tão antigo e difundido quanto a medicina. Na pré-história, a utilização de plantas era atribuída aos espíritos e aos elementos naturais a responsabilidade de doenças. Na América do Sul existem registros do uso de plantas medicinais na América pré-colombiana pela cultura Maia e Asteca[53,54]. Outras escrituras destacam que o sistema de medicina tradicional mais antigo conhecido é o Ayurveda, proveniente da Índia e datado no período de 2000-1000 a.C. O Ayurveda utiliza técnicas de massagem, nutrição (a base de ervas) e meditação, como método de diagnóstico, prevenção e cura de problemas emocionais ou traumas físicos que dão origem a doenças[55].
No Brasil, o sistema Ayurveda foi reconhecido pela OMS em 2017 (Portaria N° 849), como um sistema efetivo e comprovado cientificamente para prevenir e curar doenças[56]. Durante milênios, os humanos recorreram ao mundo natural em busca de medicamentos para tratar uma série de condições, desde infecções de forma geral a síndromes psiquiátricas. Os ensinamentos que descrevem a produção de muitos destes medicamentos, foram transmitidos através de gerações, muitas vezes através de curandeiros, que formaram a base do conhecimento farmacológico[57,58].
Os remédios à base de substâncias naturais provêm de diversas fontes, como plantas, micro-organismos terrestres, macro e micro-organismos marinhos, bem como invertebrados terrestres e vertebrados. Segundo Newman e Cragg[59], durante o período de 1940 até final de 2014, das 175 moléculas aprovadas pelo FDA para o tratamento de câncer, 49% são de produtos naturais ou derivados dele. Os produtos naturais também são utilizados como protótipos em síntese de moléculas de interesse farmacológico. Embora o uso destes compostos na preparação de medicamentos fitoterápicos remonta há milhares de anos, a descoberta e o desenvolvimento de medicamentos modernos começaram apenas no século XIX[60].
No Brasil, pelo menos quatro fitoterápicos oriundos de plantas nativas brasileiras foram aprovados pela ANVISA (Agência Nacional de Vigilância Sanitária), sendo os mais conhecidos, o analgésico e anti-inflamatório Acheflan® e o Melagrião®, utilizado no tratamento de tosse e asma61]. Medicamentos à base de produtos naturais, tem atraído a atenção das indústrias farmacêuticas, por possibilitar a obtenção de híbridos com uma biodiversidade estrutural, o que resultaria em diversidade nas suas atividades biológicas. A biodiversidade oferece inúmeras possibilidades para o desenvolvimento de novos fármacos, e em combinação com novas tecnologias, desempenham um papel importante no tratamento de doenças humanas[62].
Produtos naturais como protótipos de novos fármacos para o tratamento da COVID-19
Historicamente, existem evidências científicas sobre a eficácia terapêutica dos produtos naturais, como mencionado anteriormente. As plantas produzem uma grande diversidade de metabólitos secundários que apresentam atividades biológicas interessantes. Sendo assim, a natureza forneceu muitos modelos que fundamentaram estudos de relação estrutura-atividade biológica e inspiraram o desenvolvimento da síntese orgânica aplicada à química medicinal[63].
A pandemia de COVID-19 impulsionou uma mobilização global com o objetivo de desenvolver rapidamente novos fármacos capazes de inibir as proteases virais e, assim, combater não apenas o SARS-CoV-2, mas também outras doenças causadas por coronavírus. Neste contexto, o papel mais importante está centrado no desenvolvimento de derivados e híbridos moleculares inspirados em produtos naturais bioativos isolados de plantas. Produtos naturais e os seus derivados são usados na medicina popular para tratar diversas doenças, incluindo infecções virais[64,65].
Estudos in sílico envolvendo produtos naturais com atividades biológicas conhecidas, principalmente atividade antiviral, apontaram que algumas classes de compostos como flavonoides, florotaninos, pseudopeptídeos, alguns alcalóides e cumarinas, possuem grande potencial de atuar como inibidores eficientes da enzima Mpro do vírus SARS-CoV-2 [66]. Embora todos estes resultados apresentados sejam de estudos a partir de docking molecular, faz-se necessário, pesquisas in vitro e in vivo para confirmar o potencial desses compostos na inibição do SARS-CoV-2[67].
Apesar de já existirem opções de tratamento aprovadas por agências reguladoras, ainda há limitações em termos do perfil do paciente e do estágio da doença [68], de modo que o tratamento de casos mais graves ainda carece de uma solução eficiente que consiga reduzir de forma expressiva o índice de mortalidade. Dentro do cenário atual, um rápido desenvolvimento de candidatos vacinais ocorreu de forma nunca vivenciada pela comunidade científica[69].
No ano de 2023, Katalin Karikó e Drew Weissman foram laureados com o Prêmio Nobel de medicina, pelas descobertas de como o mRNA modificado interage com o sistema imunológico, possibilitando o desenvolvimento de vacinas de mRNA eficazes contra COVID-19. As vacinas de mRNA carregam uma parte do código genético do vírus com as instruções para que as células do corpo produzam proteínas específicas do agente que se quer imunizar. Com essa produção, a proteína é exposta ao sistema imunológico que identifica as moléculas como “estranha” e ativa uma reação contra elas[70].
No entanto, apesar das vacinas já estarem sendo disponibilizadas, a cobertura de toda a população mundial ainda representa um grande desafio. Sendo assim, mesmo no contexto da existência de vacinas, faz-se necessário a busca por alternativas terapêuticas, como os antivirais, uma vez que os casos de COVID-19 ainda continuarão a acontecer e novas variantes podem continuar surgindo[71,72].
A maioria dos fármacos utilizados na terapêutica moderna são de origem sintética. A modificação estrutural de fármacos com atividade farmacológica bem conhecida, na descoberta de novos medicamentos está vinculada fortemente com a Química Medicinal, a qual está relacionada com o planejamento, o desenho estrutural de novas estruturas químicas, síntese e desenvolvimento de agentes químicos com uso terapêutico[73].
Com o avanço tecnológico, o processo de desenvolvimento de novos fármacos vem se atualizando, e com isso, a modelagem molecular tem ganhado cada vez mais destaque. Isso se deve ao desenvolvimento de modelos computacionais que consistem num conjunto de ferramentas baseadas em métodos químicos teóricos e dados experimentais, que mimetizam o comportamento de moléculas, permitindo a previsão de suas propriedades moleculares e sua correlação com atividade biológica[74-75].
Segundo o Relatório Estatístico do Centro Tufts para o Desenvolvimento de Medicamentos (CSDD), o processo de início da descoberta de um medicamento até a sua aprovação, pode custar em torno de 2,6 milhões de dólares. Diante desse cenário de altos custos, uma das técnicas que está provando enfrentar esses obstáculos pela pesquisa e descoberta de novos fármacos é o Docking Molecular, técnica crucial na identificação de moléculas para testes experimentais tanto in vitro quanto in vivo[76,77].
A técnica de docking molecular é um método in sílico para prever os modos de ligação predominantes entre o promissor candidato à fármaco (conhecido nessa técnica como ligante) e uma proteína alvo, combinando e otimizando variáveis físico-químicas entre si, bem como elucidando processos bioquímicos fundamentais. Durante a pandemia da COVID-19, essa técnica foi uma grande aliada dos cientistas na aplicação de uma triagem in sílico de pequenas moléculas na descoberta de potenciais inibidores virais. Isso só foi possível devido à poderosa visualização em escala atômica da estrutura tridimensional (3D) de diferentes proteínas do SARS-CoV-2 por cristalografia de raios X, RMN (Ressonância Magnética Nuclear) e técnicas de Criomicroscopia. Segundo Pushkaran e colaboradores[78], cerca de 330 estruturas de proteínas são responsáveis por alvos terapêuticos de SARS-CoV-2 e estão disponíveis no banco de dados de proteínas (PDB- do inglês Protein Data base) gratuitamente[79,80].
Ácido gálico e derivados: fonte de inspiração para o desenvolvimento de novos princípios ativos
Os compostos fenólicos, também conhecidos como polifenóis, formam uma importante classe de antioxidantes naturais, possuindo inúmeras atividades biológicas. Atualmente são mais de 8 mil estruturas conhecidas, constituídas quimicamente de grupos heterogêneos com anéis fenil contendo um ou mais hidroxilas. Dentre os vários polifenóis, o ácido gálico (AG) (ácido 3,4,5-tri hidroxibenzoíco) (FIGURA 3), um composto trifenólico, emergiu como um potencial candidato no tratamento de diversas doenças e distúrbios neurológicos[81,82].
O AG e seus derivados são amplamente encontrados no reino vegetal como metabólitos secundários e podem ser isolados de várias frutas como, a uva-ursina (Arctostaphylos) e amora (Caesalpinia, Mimosoideae), em plantas, incluindo folhas de agrião, casca de carvalho, noz de areca e nozes[83].
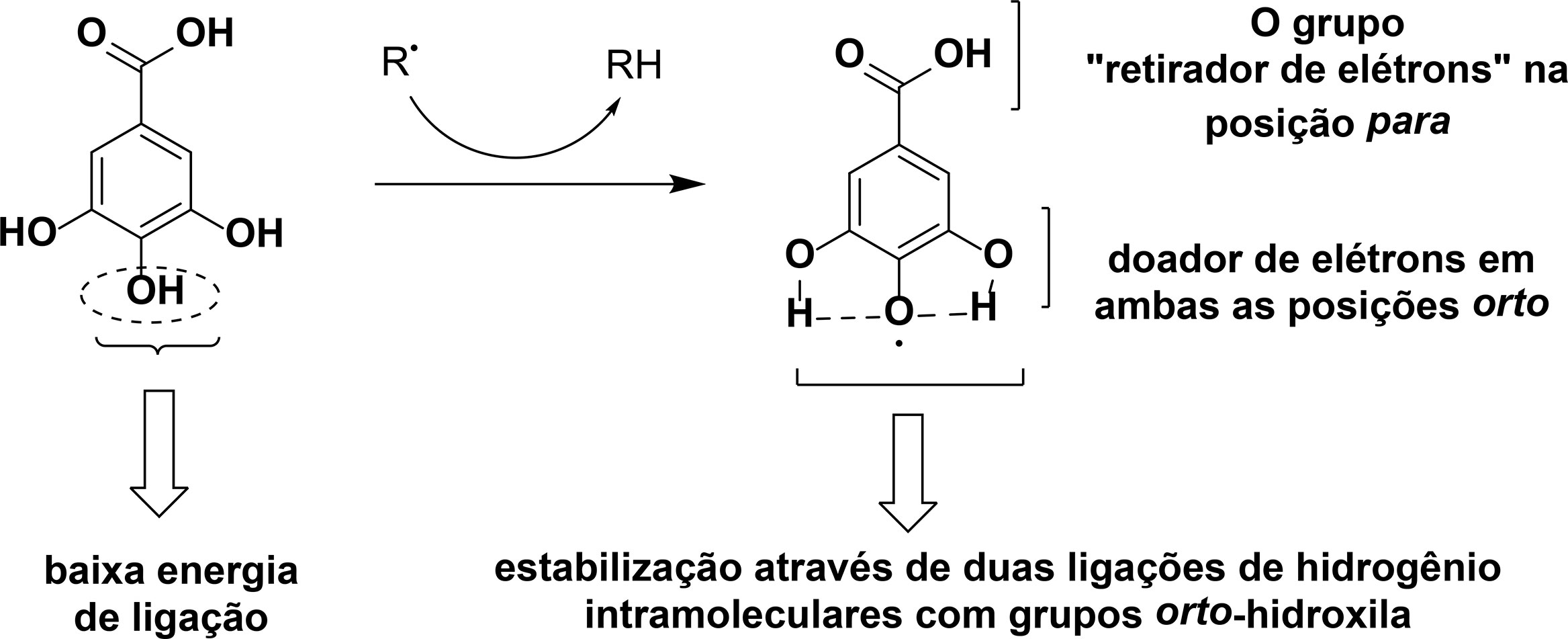
Estudos sobre a relação estrutura-atividade do ácido gálico e seus derivados, mostraram que estes atuam como anti-radicais e antioxidantes devido a presença dos grupos hidroxilas. A principal razão por trás de seu potencial como antioxidante está relacionada ao número e a posição dos grupos hidroxilas e aos efeitos de conjugação e ressonância[84].
O AG por apresentar um arranjo aromático fenólico, resulta na tendência de doação de hidrogênios da porção fenólica, podendo ser por HAT (Transferência de Átomos de Hidrogênio, traduzido do inglês) ou por SET (Transferência de Único Elétron, traduzido do inglês). O grupo carboxílico facilmente ionizável contribuiu para essa tendência, através da doação de um hidrogênio[85-87].
Badhani e pesquisadores81,85], afirmam que o grupo OH para-substituído são responsáveis pela ação de eliminação de radicais, enquanto os outros dois grupos hidroxila fornecem estabilidade por meio de ligações de hidrogênio intramolecular e ligações de hidrogênio de baixa entalpia de dissociação (FIGURA 4).
A produção de EROs (Espécies Reativas de Oxigênio) em infecções virais é muito comum, e a infecção por SARS-CoV-2 não é uma exceção. Segundo Tirado Kulieva e colaboradores[89], compostos fenólicos previnem o dano oxidativo e ampliam a resposta inflamatória à ação das EROs, com o intuito de ajudar a manter o sistema imunológico competente. Isso ocorre, devido à sua ação inibitória contra enzimas produtoras de EROs e o aumento da atividade de enzimas antioxidantes[90].
Além de seus efeitos antioxidantes, o GA exibe atividade anti-inflamatória significativa ao modular vias inflamatórias importantes. A inflamação é uma resposta imune à infecção, frequentemente exacerbada por citocinas pró-inflamatórias. A infecção por SARS-CoV-2 ativa macrófagos e promove liberação excessiva de citocinas, especialmente IL-1 e IL-6, contribuindo para a síndrome do desconforto respiratório agudo (SDRA). Citocinas pró-inflamatórias liberadas por macrófagos fortalecem a resposta imune do hospedeiro, sendo importantes no controle da inflamação. No entanto, sua produção excessiva e sustentada pode levar a dano tecidual significativo[91,92].
A ativação da cascata inflamatória e à "tempestade de citocinas" descontrolada, com aumento de IL-1β, IL-6 e TNF-α, a COVID-19 tem a capacidade de causar alterações, as quais estão associadas a complicações pulmonares, hepáticas, cardíacas e renais em pacientes com COVID-19 grave[93,94]. Apesar destes mecanismos destacarem o potencial do AG no tratamento de condições inflamatórias e antioxidantes, a aplicação clínica do AG é limitada, devido a sua baixa biodisponibilidade oral[81,95].
É bem conhecido que a síntese de análogos a partir de princípios ativos isolados naturalmente tem contribuído para a obtenção de novos agentes terapêuticos. A importância da fitomedicina tem ganhado muita atenção pelas publicações na academia científica sobre o papel de derivados de produtos naturais que podem ser obtidos através de extratos brutos ou de isolados puros contra diferentes vírus respiratórios, incluindo a COVID-19[96,97].
Derivados de AG no Combate às proteases virais do SARS-CoV-2
Umar e colaboradores[90], realizaram estudos in sílico com o AG e 15 derivados à cinco proteínas não estruturais, a Mpro (nsp5), a Plp (nsp3), a RNA polimerase dependente de RNA (RdRp/nsp12), a helicase (nsp13) e a endorribonuclease específica de uridilato (NendoU/nsp15) do SARS-COV-2. Os derivados incluem galato de propila, galato de lauril, galato de octila, teaflavina, ácido tânico, galato de (−)-epigalocatequina (EGCG), (−)-epigalocatequina (EGC), galato de (−)-epicatequina (ECG) e (+)-epicatequina (EC). Os resultados deste estudo, revelou que 3-O-(6-galoilglicosídeo), 4-O-(6-galoilglicosídeo) e galato de epicatequina, podem ser inibidores promissores das proteínas não estruturais selecionadas do SARS-CoV-2 e uma possível opção de tratamento contra a atual pandemia de COVID-19. O derivado 4-O-(6-galoilglicosídeo) foi o único que apresentou as melhores energias de ligação contra 4 proteínas não estruturais, sendo elas Nsp3, Nsp12, Nsp13 e Nsp15 com -6,8, -8,9, -9,1 e -7,5 kcal/mol, respectivamente.
Yushu e colaboradores[98], realizaram experimentos de RMN (Ressonância Magnética Nuclear) do AG e da proteína não estrutural 7 do SARS-CoV-2 (nsp7) marcado com 15 N nos pH 7,5 e 6,5. Foi possível observar uma mudança nos deslocamentos químicos, indicando que o composto se ligou a uma cavidade da superfície centrada em uma das quatro α-hélices da proteína (α2). A identificação da superfície de ligação do ácido gálico na nsp7 do SARS-CoV-2 permite o acoplamento virtual e outras modalidades de descoberta de fármacos.
Souza e pesquisadores[99], após estudos fitoquímicos dos galhos Mangifera indica, levaram à identificação do galato de metila. A partir disso, foi realizado a síntese de 13 ésteres de galato preparados a partir do AG com álcoois naturais e não naturais. Seus efeitos inibitórios foram avaliados contra Mpro do SARS-CoV-2. Dois compostos se mostraram mais ativos, o galato de isoamilo e galato de linalilo com valores de IC50 de 2,60 e 4,0 μM, respectivamente. Análise in sílico mostraram fortes probabilidades de interações com a protease.
Nesse mesmo ano, Carvalho e colaboradores[100], mostram o efeito inibitório de amidas derivadas do AG (galamidas e selenogalamidas) contra a protease Mpro, juntamente com a avaliação da citotoxicidade e estudos de docking molecular. Os compostos N -(4-Fluorofenil)-3,4,5-tri-hidroxibenzamida, N -(2,4-Dimetoxifenil)-3,4,5-tri-hidroxibenzamida, 3,4,5-Triidroxi- N -[4-(trifluorometil)fenil]benzamida, apresentaram a maior inibição enzimática com IC 50 = 0,26 ± 0,19 µM, 0,80 ± 0,38 µM e 2,87 ± 1,17 µM, respectivamente. A selenogalamida, 3,4,5-Tri-hidroxi- N- [4-iodo-2 (fenilselanil)fenil]benzamida , exibiu valores de IC50 de 5,42 ± 2,89 µM e uma comparação com seu congênere não selenilado, 3,4,5-Triidroxi- N- (4-iodofenil)benzamida, mostra que a inserção da fração calcogênica melhorou a capacidade inibitória do composto em aproximadamente 10 vezes. Em relação à toxicidade celular em células THP-1 e Vero, a maioria dos compostos não induzem toxicidade celular substancial nas concentrações testadas. Os resultados de docking molecular para os compostos mais ativos, mostraram que as interações de ligação de hidrogênio envolvendo os grupos hidroxila (OH) da fração galato são relevantes, bem como o grupo carbonila para inibição da protease.
Conclusão
Os vírus, ao longo da história, têm sido agentes centrais em grandes desafios de saúde pública, como evidenciado pela pandemia de COVID-19. A compreensão dos mecanismos moleculares de infecção, replicação e interação vírus-hospedeiro é essencial para o desenvolvimento de estratégias eficazes de combate a essas ameaças. Nesse contexto, os produtos naturais, como o ácido gálico e seus derivados, demonstram-se promissoras fontes de novos fármacos antivirais, com potencial de atuação sobre alvos virais específicos.
O avanço das tecnologias in silico, aliado ao uso racional da biodiversidade, permite acelerar o processo de descoberta de medicamentos seguros e eficazes. Mesmo diante das dificuldades, a pandemia impulsionou uma nova era de inovação científica. Assim, é fundamental que continuemos investindo em pesquisa interdisciplinar, na integração entre ciência tradicional e moderna, para que estejamos cada vez mais preparados para enfrentar futuras emergências sanitárias globais.
A ciência mostrou que é possível responder com agilidade a crises, mas é o conhecimento contínuo, sustentado e colaborativo que garante soluções duradouras. A natureza continua sendo uma fonte inesgotável de inspiração — e a curiosidade científica, o maior combustível para o progresso.
Agradecimentos
Ao Governo Federal Brasileiro e à CAPES pela oportunidade de fazer parte de um Edital Emergencial intitulado Fármacos e lmunologia n° 011/2020, o qual tinha como objetivo, estudos sobre o reposicionamento de fármacos voltados ao combate à COVID-19. Este artigo de revisão faz parte da tese de doutorado da autora.
Referências
- 1 Silva SM. Fatores de virulência microbianos e terapias emergentes. S586f. Organizadores: Barbosa AV, Silva SM, Silva FHS, Assunção MAS, Anjos FBR. São José dos Pinhais: Latin American Publicações, 2022. 354 p. ISBN: 978-65-996545-0-3. Disponível em: [ https://www.researchgate.net/profile/Francisco-Silva-98/publication/359969282_Fatores_de_virulencia_microbianos_e_terapias_emergentes/links/6259b0e19be52845a906029f/Fatores-de-virulencia-microbianos-e-terapias-emergentes.pdf ].
» https://www.researchgate.net/profile/Francisco-Silva-98/publication/359969282_Fatores_de_virulencia_microbianos_e_terapias_emergentes/links/6259b0e19be52845a906029f/Fatores-de-virulencia-microbianos-e-terapias-emergentes.pdf - 2 Organização Pan-Americana da Saúde. Módulos de Princípios de Epidemiologia para o Controle de Enfermidades (OPAN/OMS). Módulo 2: Saúde e doença na população / Organização Pan-Americana da Saúde. Brasília: Organização Pan-Americana da Saúde. Ministério da Saúde, 2010. 48 p.: il. 7 volumes. ISBN 978-85-7967-020-6. Disponível em: [ https://iris.paho.org/handle/10665.2/54407?show=full ].
» https://iris.paho.org/handle/10665.2/54407?show=full - 3 Lemos ERS, Villar LM, Leon LAA, et al. T674t. Tópicos em virologia. - Rio de Janeiro. Editora Fiocruz, 2023. 7 MB: il. color; tab. (Coleção Bio) ISBN: 978-65-5708-151-8. Disponível em: [ https://books.scielo.org/id/5bhdb/pdf/lemos-9786557082119.pdf ].
» https://books.scielo.org/id/5bhdb/pdf/lemos-9786557082119.pdf - 4 Hoenen T, Groseth A. Virus-Host Cell Interactions. Cells. 2022 Feb 25; 11(5): 804. Disponível em: [ https://www.mdpi.com/2073-4409/11/5/804 ].
» https://www.mdpi.com/2073-4409/11/5/804 - 5 Klasse PJ, Bron R, Marsh M. Mechanisms of enveloped virus entry into animal cells. Adv Drug Deliv Rev. 1998 Oct 5; 34(1): 65-91. Disponível em: [ https://pubmed.ncbi.nlm.nih.gov/10837671/ ].
» https://pubmed.ncbi.nlm.nih.gov/10837671/ - 6 Villanueva RA , Rouillé Y , Dubuisson J . Interactions between virus proteins and host cell membranes during the viral life cycle. Int Rev Cytol. 2005; 245: 171-244. Disponível em: [ https://pubmed.ncbi.nlm.nih.gov/16125548/ ].
» https://pubmed.ncbi.nlm.nih.gov/16125548/ - 7 Schatzmayr HG , Cabral MC . A virologia no Estado do Rio de Janeiro: uma visão global. 2 a Edição - Rio de Janeiro: FIOCRUZ, 2012. 176 p, 111p. 172 - 175. Disponível em: [ https://www.ioc.fiocruz.br/sites/default/files/Livro_Virologia_nova_edicao.pdf ].
» https://www.ioc.fiocruz.br/sites/default/files/Livro_Virologia_nova_edicao.pdf - 8 Louten J . Virus Replication. Essential Human. Virology. 2016; 49-70. Disponível em: [ https://pmc.ncbi.nlm.nih.gov/articles/PMC7149683/ ] .
» https://pmc.ncbi.nlm.nih.gov/articles/PMC7149683/ - 9 Rouse BT, Sehrawat S. Immunity and immunopathology to viruses: what decides the outcome? Nat Rev Immunol. 2010 Jul; 10(7): 514-26. Disponível em: [ https://www.nature.com/articles/nri2802 ].
» https://www.nature.com/articles/nri2802 - 10 Marshall JS, Warrington R, Watson W, Kim HL. An introduction to immunology and immunopathology. Allergy Asthma Clin Immunol. 2018; 14(Suppl 2): 49. Disponível em: [ https://aacijournal.biomedcentral.com/articles/10.1186/s13223-018-0278-1 ].
» https://aacijournal.biomedcentral.com/articles/10.1186/s13223-018-0278-1 - 11 Chappell JD, Dermody T. S.134 - Biology of Viruses and Viral Diseases. Editor(s): Bennett JE, Dolin R, Blaser MJ, Mandell, Douglas and Bennett's. Principles and Practice of Infectious Diseases (Eighth Edition), W.B. Saunders, 2015, Pages 1681-1693.e4. ISBN 9781455748013. Disponível em: [ https://doi.org/10.1016/B978-1-4557-4801-3.00134-X ]
» https://doi.org/10.1016/B978-1-4557-4801-3.00134-X - 12 Seventer JMVS, Hochberg N. Principles of Infectious Diseases: Transmission, Diagnosis, Prevention, and Control. Editor(s): Stella R. Quah, International Encyclopedia of Public Health (Second Edition). Academic Press. 2017, Pages 22-39. ISBN 9780128037089. Disponível em: [ https://doi.org/10.1016/B978-0-12-803678-5.00516-6 ].
» https://doi.org/10.1016/B978-0-12-803678-5.00516-6 - 13 Zanella JRC. Zoonoses emergentes e reemergentes e sua importância para saúde e produção animal. Pesq Agropec Bras [online]. 2016; 51(05): 510-519. Disponível em: [ https://doi.org/10.1590/S0100-204X2016000500011 ].
» https://doi.org/10.1590/S0100-204X2016000500011 - 14 Engering A, Hogerwerf L, Slingenbergh J. Pathogen-host environment interplay and disease emergence. Emerg Microb Infec. 2013; 2(1): 1-7. Disponível em: [ https://doi.org/10.1038/emi.2013.5 ].
» https://doi.org/10.1038/emi.2013.5 - 15 Piret J , Boivin G . Pandemics Throughout History. Front Microbiol. 2021 Jan 15; 11: 631736. Disponível em: [ https://pubmed.ncbi.nlm.nih.gov/33584597/ ].
» https://pubmed.ncbi.nlm.nih.gov/33584597/ - 16 Baker RE , Mahmud AS , Miller IF , et al . Infectious disease in an era of global change. Nat Rev Microbiol. 2022; 20: 193-205. Disponível em: [ https://doi.org/10.1038/s41579021-00639-z ].
» https://doi.org/10.1038/s41579021-00639-z - 17 Elkhatib WF , Abdelkareem SS , Khalaf W , et al . Narrative review on century of respiratory pandemics from Spanish flu to COVID-19 and impact of nanotechnology on COVID-19 diagnosis and immune system boosting. Virol J. 2022; 19: 167. Disponível em: [ https://doi.org/10.1186/s12985-022-01902-2 ].
» https://doi.org/10.1186/s12985-022-01902-2 - 18 Organização Pan-Americana da Saúde Módulos de Princípios de Epidemiologia para o Controle de Enfermidades (OPAN/OMS). Influenza, SARS-CoV-2, RSV and other Respiratory Viroses. [acesso em: 10 set. 2023]. Disponível em: [ https://www.paho.org/en/topics/influenza-sars-cov-2-rsvand-other-respiratory-viruses ].
» https://www.paho.org/en/topics/influenza-sars-cov-2-rsvand-other-respiratory-viruses - 19 Barrero CAB , Beam KS , Bernardini LB , Ramos EGC , Davenport PE , et al . COVID-19: neonatal-perinatal perspectives. J Perinatol. 2021; 41: 940-951. Disponível em: [ https://doi.org/10.1038/s41372-020-00874-x ].
» https://doi.org/10.1038/s41372-020-00874-x - 20 Harapan H, Itoh N, Yufika A, Winardi W, et al. Coronavirus disease 2019 (COVID-19): A literature review. J Infect Public Health. 2020 May; 13(5): 667-673. Disponível em: [ https://doi.org/10.1016/j.jiph.2020.03.019 ].
» https://doi.org/10.1016/j.jiph.2020.03.019 - 21 Haghani M, Bliemer MCJ, Goerlandt F, Li J. The scientific literature on Coronaviruses, COVID-19 and its associated safety-related research dimensions: A scientometric analysis and scoping review. Saf Sci. 2020 Sep; 129: 104806. Disponível em: [ https://doi.org/10.1016/j.ssci.2020.104806 ].
» https://doi.org/10.1016/j.ssci.2020.104806 - 22 Painel Coronavírus. [acesso em: set 2025]. Disponível em: [ https://covid.saude.gov.br/ ].
» https://covid.saude.gov.br/ - 23 Pal M, Berhanu G, Desalegn C, KandI V. Severe Acute Respiratory Syndrome Coronavirus-2 (SARS-CoV-2): An Update. Cureus. 2020 Mar 26; 12(3): e7423. Disponível em: [ https://doi.org/10.7759/cureus.7423 ].
» https://doi.org/10.7759/cureus.7423 - 24 Hognon C , Bignon E , Monari A , Marazzi M , Garcia IC . Revealing the Molecular Interactions between Human ACE2 and the Receptor Binding Domain of the SARS-CoV-2 Wild-Type, Alpha and Delta Variants. Int J Mol Sci. 2023; 24: 2517. Disponível em: [ https://doi.org/10.3390/ijms24032517 ].
» https://doi.org/10.3390/ijms24032517 - 25 Belouzard S , Millet JK , Licitra BN , Whittaker GR . Mechanisms of Coronavirus Cell Entry Mediated by the Viral Spike Protein. Viruses. 2012; 4: 1011-1033. Disponível em: [ https://doi.org/10.3390/v4061011 ].
» https://doi.org/10.3390/v4061011 - 26 Dhama K , Khan S , Tiwari R , Sircar S , et al . Coronavirus Disease 2019-COVID-19. Clin Microbiol Rev. 2020 Jun 24; 33(4): e00028-20. Disponível em: [ https://doi.org/10.1128/CMR.00028-20 ].
» https://doi.org/10.1128/CMR.00028-20 - 27 Zhang J , Xiao T , Cai Y , Chen B . Structure of SARS-CoV-2 spike protein. Curr Opin Virol. 2021 Oct; 50: 173-182. Disponível em: [ https://doi.org/10.1016/j.coviro.2021.08.010 ].
» https://doi.org/10.1016/j.coviro.2021.08.010 - 28 Tran A , Kervin TA , Overduin M . Multifaceted membrane binding head of the SARS-CoV-2 spike protein. Curr Res Struct Biol. 2022 May 16; 4: 146-157. Disponível em: [ https://doi.org/10.1016/j.crstbi.2022.05.001 ].
» https://doi.org/10.1016/j.crstbi.2022.05.001 - 29 Wang H , Zhao T , Yang S , et al . Reactive force field-based molecular dynamics simulation of the interaction between plasma reactive oxygen species and the receptor-binding domain of the spike protein in the capsid protein of SARS-CoV-2. J Phys D: Appl Phys. 2022; 55(9): 095401. Disponível em: [ https://iopscience.iop.org/article/10.1088/1361-6463/ac360e ].
» https://iopscience.iop.org/article/10.1088/1361-6463/ac360e - 30 Yan R, Zhang Y, Li Y, et al. Structural basis for the recognition of SARS-CoV-2 by full-length human ACE2. Sci. (New York, N.Y.). 2020; 367(6485): 1444-1448. Disponível em: [ https://doi.org/10.1126/science.abb2762 ].
» https://doi.org/10.1126/science.abb2762 - 31 Hu Q , Xiong Y , Zhu G , et al . The SARS-CoV-2 main protease (Mpro): Structure, and emerging therapies 19. MedComm. 2022; 3: e151. Disponível em: [ https://doi.org/10.1002/mco2.151 ].
» https://doi.org/10.1002/mco2.151 - 32 Li X , Song Y . Structure and function of SARS-CoV and SARS-CoV-2 main proteases and their inhibition: A comprehensive review. Europ J Medic Chem. 2023; 260: 115772. Disponível em: [ https://doi.org/10.1016/j.ejmech.2023.115772 ].
» https://doi.org/10.1016/j.ejmech.2023.115772 - 33 World Health Organization (WHO). COVID-19 Cases, World. [acesso em: 02 mai. 2023]. Disponível em: [ https://covid19.who.int/ ].
» https://covid19.who.int/ - 34 Dhand R, Li J. Coughs and Sneezes: Their Role in Transmission of Respiratory Viral Infections, Including SARS-CoV-2. Am J Respir Crit Care Med. 2020 Sep 1; 202(5): 651-659. Disponível em: [ https://doi.org/10.1164/rccm.202004-1263PP ].
» https://doi.org/10.1164/rccm.202004-1263PP - 35 Emrani J, Ahmed M, Jeffers-francis L, Teleha JC, et al. SARS-COV-2, infection, transmission, transcription, translation, proteins, and treatment: A review. J Biol Macromol. 2021 Dec 15; 193(PtB): 1249-1273. Disponível em: [ https://doi.org/10.1016/j.ijbiomac.2021.10.172 ].
» https://doi.org/10.1016/j.ijbiomac.2021.10.172 - 36 Dimitrov DS. Virus entry: molecular mechanisms and biomedical applications. Nat Rev Microbiol. 2004; 2(2): 109-22. Disponível em: [ https://doi.org/10.1038/nrmicro817 ].
» https://doi.org/10.1038/nrmicro817 - 37 Más V , Melero JA . Entry of Enveloped Viruses into Host Cells: Membrane Fusion. In: Mateu M . (eds) Structure and Physics of Viruses. Subcellular Biochemistry. 2013; 68: 467. Springer, Dordrecht. Disponível em: [ https://doi.org/10.1007/978-94-007-6552-8_16 ].
» https://doi.org/10.1007/978-94-007-6552-8_16 - 38 Shang J , Wan Y , Luo C , Ye G , et al . Cell entry mechanisms of SARS-CoV-2. Proc Natl Acad Sci USA. 2020, 26; 117(21): 11727-11734. Disponível em: [ https://doi.org/10.1073/pnas.2003138117 ].
» https://doi.org/10.1073/pnas.2003138117 - 39 Pillay TS. Gene of the month: the 2019-nCoV/SARS-CoV-2 novel corona virus spike protein. J Clin Pathol, 2020, Jul;73(7):366-369. Disponível em: [ https://doi.org/10.1136/jclinpath-2020-206658 ].
» https://doi.org/10.1136/jclinpath-2020-206658 - 40 Letko M, Marzi A, Munster V. Functional assessment of cell entry and receptor usage for SARS-CoV-2 and other lineage B betacoronaviruses. Nat Microbiol. 2020; 5(4): 562-569. Disponível em: [ https://doi.org/10.1038/s41564-020-0688-y ].
» https://doi.org/10.1038/s41564-020-0688-y - 41 Örd M , Faustova I , Loog M . The sequence at Spike S1/S2 site enables cleavage by furin and phospho-regulation in SARS-CoV2 but not in SARS-CoV1 or MERS CoV. Sci Rep 10. 2020, 16944. Disponível em: [ https://doi.org/10.1038/s41598-020-74101-0 ].
» https://doi.org/10.1038/s41598-020-74101-0 - 42 Huang Y , Yang C , Xu X , Xu W , Liu S . Structural and functional properties of SARS-CoV-2 spike protein: potential antivirus drug development for COVID 19. Acta Pharmacol Sin. 2020; 41: 1141-1149. Disponível em: [ https://doi.org/10.1038/s41401-020-0485-4 ].
» https://doi.org/10.1038/s41401-020-0485-4 - 43 Chinchar VG. Replication of Viruses. Encyclop Virology 1999: 1471–8. Disponível em: [https://doi.org/10.1006/rwvi.1999.0245].
» https://doi.org/10.1006/rwvi.1999.0245 - 44 Pišlar A , Mitrovic A , Sabotic J , Fonovic PU , Nanut MP , et al . The role of cysteine peptidases in coronavirus cell entry and replication: The therapeutic potential of cathepsin inhibitors. PLoS Pathog. 2020; 16(11): e1009013. Disponível em: [ https://doi.org/10.1371/journal.ppat.1009013 ].
» https://doi.org/10.1371/journal.ppat.1009013 - 45 V'kovski P , Kratzel A , Steiner S , Stalder H , Thiel T . Coronavirus biology and replication: implications for SARS-CoV-2. Nat Rev Microbiol 2021; 19: 155-170. Disponível em: [ https://doi.org/10.1038/s41579-020-00468-6 ].
» https://doi.org/10.1038/s41579-020-00468-6 - 46 Qamar MT , Ul ASM , Alamri MA , Chen LL . Structural basis of SARS-CoV-2 3CLpro and anti-COVID-19 drug discovery from medicinal plants. J Pharmac Anal. 1 ago. 2020; 10(4): 313. Disponível em: [ https://doi.org/10.1016/j.jpha.2020.03.009 ].
» https://doi.org/10.1016/j.jpha.2020.03.009 - 47 Yan L , Zhang Y , Ge J , Zheng L , Gao Y , et al . Architecture of a SARS CoV-2 mini replication and transcription complex. Nat Commun. 2020 Nov 18; 11(1): 5874. Disponível em: [ https://doi.org/10.1038/s41467-020-19770-1 ].
» https://doi.org/10.1038/s41467-020-19770-1 - 48 Pluskota-karwatka D, Hoffmann M, Barciszewski J. Reducing SARS-CoV-2 pathological protein activity with small molecules. J Pharmac Anal. 2021; 11(4): 383-397. ISSN 2095-1779. Disponível em: [ https://doi.org/10.1016/j.jpha.2021.03.012 ].
» https://doi.org/10.1016/j.jpha.2021.03.012 - 49 Saville JW, Berezuk, AM, Srivastava SS, Subramaniam S. Three-Dimensional Visualization of Viral Structure, Entry, and Replication Underlying the Spread of SARS-CoV-2. Chem Ver. 2022; 122(17): 14066-14084. Disponível em: [ https://doi.org/10.1021/acs.chemrev.1c01062 ].
» https://doi.org/10.1021/acs.chemrev.1c01062 - 50 NoorI R, Sardar M. An outlook on potential protein targets of COVID-19 as a druggable site. Mol Biol Rep. 2022; 49: 10729-10748. Disponível em: [ https://doi.org/10.1007/s11033-022 07724-3].
» https://doi.org/10.1007/s11033-022 07724-3 - 51 Le K , Kannappan S , Kim T , Lee, JH , Lee H , Kim KK . Structural understanding of SARS-CoV-2 virus entry to host cells. Front Mol Biosci. 2023 Nov 2; 10: 1288686. Disponível em: [ https://doi.org/10.3389/fmolb.2023.1288686 ].
» https://doi.org/10.3389/fmolb.2023.1288686 - 52 Rocha LPB, Alves JVO, Aguiar IFS, et al. Uso de plantas medicinais: Histórico e relevância. Res Society Develop. 2021; 10(10): e44101018282. (CC BY 4.0) | ISSN 2525-3409. Disponível em: [ http://dx.doi.org/10.33448/rsd-v10i10.18282 ].
» http://dx.doi.org/10.33448/rsd-v10i10.18282 - 53 Dar RA, Shahnawaz M, Rasool S, Qazi PH. Natural product medicines: A literature update. J Phytopharmacol. 2017; 6(6): 340 342. ISSN 2320-480X.
- 54 Carneiro DM. Ayuerveda - Saúde e Longevidade na Tradição Milenar da Índia. Editora Pensamento. 2009. ISBN: 9788531516153, 8531516153.
- 55 Organização Mundial da Saúde - OMS. Gabinete do Ministério da Saúde. Portaria Nº 849, de 27 de mar de 2017. [acesso em: 22 set. 2023]. Disponível em: [ https://bvsms.saude.gov.br/bvs/saudelegis/gm/2017/prt0849_28_03_2017.html ].
» https://bvsms.saude.gov.br/bvs/saudelegis/gm/2017/prt0849_28_03_2017.html - 56 Wright GD. Unlocking the potential of natural products in drug Discovery. Microbial Biotechnol. 2019. 12(1): 55-57. Disponível em: [ https://doi.org/10.1111/1751-7915.13351 ].
» https://doi.org/10.1111/1751-7915.13351 - 57 Dzobo K. The Role of Natural Products as Sources of Therapeutic Agents for Innovative Drug Discovery. Compr Pharmacol. 2022; 408-22. Disponível em: [ https://doi.org/10.1016/B978-0-12 820472-6.00041-4].
» https://doi.org/10.1016/B978-0-12 - 58 Newman DJ , Cragg GM . Natural Products as Sources of New Drugs from 1981 to 2014. J Nat Prod. fev. 2016; 79: 629-661. Disponível em: [ https://doi.org/10.1021/acs.jnatprod.5b01055v ].
» https://doi.org/10.1021/acs.jnatprod.5b01055v - 59 Veeresham C. Natural products derived from plants as a source of drugs. J Adv Pharm Technol Res. 2012 Oct; 3(4): 200-1. Disponível em: [ https://doi.org/10.4103/2231-4040.104709 ].
» https://doi.org/10.4103/2231-4040.104709 - 60 Leite PM , Camargos LM , Castilho RO . Recent progess in phytotherapy: A Brazilian perspective. Europ J Integr Medic. 2021; 41: 101270. Disponível em: [ https://doi.org/10.1016/j.eujim.2020.101270 ].
» https://doi.org/10.1016/j.eujim.2020.101270 - 61 Yuan H , Ma Q , Ye L , Piao G . A Medicina Tradicional e a Medicina Moderna a partir de Produtos Naturais. Molecules. 2016; 21: 559. Disponível em: [ https://doi.org/10.3390/molecules21050559 ].
» https://doi.org/10.3390/molecules21050559 - 62 Dias DA, Urban S, Roessner UTE. A Historical Overview of Natural Products in Drug Discovery. Metabolites. 2012; 2: 303-336. Disponível em: [ https://doi.org/10.3390/metabo2020303 ].
» https://doi.org/10.3390/metabo2020303 - 63 Ganjhu RKumar , Mudgal PP , Maity H , Dowarha D , et al . Herbal plants and plant preparations as remedial approach for viral diseases. Virus Disease. Dez 2015; 26: 225-236. Disponível em: [ https://doi.org/10.1007/s13337-015-0276-6 ].
» https://doi.org/10.1007/s13337-015-0276-6 - 64 Liu C , Zhou Q , Li Y , Garner LV , et al . Research and development on therapeutic agents and vaccines for Covid-19 and related human coronavirus diseases. ACS Cent Sci. mar. 2020; 6: 315-331. Disponível em: [ https://doi.org/10.1021/acscentsci.0c00272v ].
» https://doi.org/10.1021/acscentsci.0c00272v - 65 Prasansuklab A, Theerasri A, Rangsinth P, et al. Anti COVID-19 drug candidates: A review on potential biological activities of natural products in the management of new coronavirus infection. J Trad Complement Medic. 2021; 11(2): 144-157. Disponível em: [ https://doi.org/10.1016/j.jtcme.2020.12.001 ].
» https://doi.org/10.1016/j.jtcme.2020.12.001 - 66 Rakib A , Nain Z , Sami AS , Mahmud S , Islam A , et al . A molecular modelling approach for identifying antiviral selenium-containing heterocyclic compounds that inhibit the main protease of SARS-CoV-2: an in silico investigation. Brief Bioinformat. March 2021; 22(2): 1476-1498. Disponível em: [ https://doi.org/10.1093/bib/bbab045 ].
» https://doi.org/10.1093/bib/bbab045 - 67 FDA. [acesso em: 11 mai. 2023]. Disponível em: [ https://www.fda.gov/consumers/consumer-updates/know-yourtreatment-options-covid19 ].
» https://www.fda.gov/consumers/consumer-updates/know-yourtreatment-options-covid19 - 68 Tregoning J.S, Brown ES, Cheeseman HM, Flight KE, Higham SL, Lemm NM, et al. Vaccines for COVID-19. Clinic Experim Immunol. 2020; 202(2): 162- 192. Disponível em: [ https://doi.org/10.1111/cei.13517 ].
» https://doi.org/10.1111/cei.13517 - 69 Academia Brasileira de Ciências (ABC). Nobel de medicina vai para cientistas que possibilitaram vacinas contra a COVID-19. [acesso em: 16 out. 2023]. Disponível em: [ http://www.abc.org.br/2023/10/02/nobel-de-medicina-vai-para-cientistas-que-possibilitaram as-vacinas-contra-a-covid-19/].
» http://www.abc.org.br/2023/10/02/nobel-de-medicina-vai-para-cientistas-que-possibilitaram as-vacinas-contra-a-covid-19/ - 70 Vasireddy D, Vanaparthy R, Mohan G, Malayala SV, Atlurl P. Review of COVID-19 Variants and COVID-19 Vaccine Efficacy: What the Clinician Should Know? J Clin Med Res. 2021 Jun; 13(6): 317-325. Disponível em: [ https://doi.org/10.14740/jocmr4518 ].
» https://doi.org/10.14740/jocmr4518 - 71 Tao K , Tzou PL , Nouhin J , et al . The biological and clinical significance of emerging SARS-CoV-2 variants. Nat Rev Genet 2021; 22: 757-773. Disponível em: [ https://doi.org/10.1038/s41576-021-00408-x ].
» https://doi.org/10.1038/s41576-021-00408-x - 72 Lombardino JG, Lowe JA. The role of the medicinal chemist in drug discovery - then and now. Nat Rev Drug Discov 2024; 3: 853-862. Disponível em: [ https://doi.org/10.1038/nrd1523 ].
» https://doi.org/10.1038/nrd1523 - 73 Nadendla RR . Molecular modeling: A powerful tool for drug design and molecular docking. Reson. 2004; 9: 51-60. Disponível em: [ https://doi.org/10.1007/BF02834015 ].
» https://doi.org/10.1007/BF02834015 - 74 Durrant JD , Mccammon J . Molecular dynamics simulations and drug discovery. BMC Biol 2011; 9: 71. Disponível em: [ https://doi.org/10.1186/1741-7007-9-71 ].
» https://doi.org/10.1186/1741-7007-9-71 - 75 Aminpour M, Montemagno C, TuszynskI JA. An Overview of Molecular Modeling for Drug Discovery with Specific Illustrative Examples of Applications. Molecules. 2019 Apr; 30; 24(9): 1693. Disponível em: [ https://doi.org/10.3390/molecules24091693 ].
» https://doi.org/10.3390/molecules24091693 - 76 Agu PC, Afiukwa CA, Orji OU, Ezeh EM, Ofoke IH, et al. Molecular docking as a tool for the discovery of molecular targets of nutraceuticals in diseases management. Sci Rep. 2023 Aug 17; 13(1): 13398. Disponível em: [ https://doi.org/10.1038/s41598-023-40160-2 ].
» https://doi.org/10.1038/s41598-023-40160-2 - 77 AdelusI T , Oyedele AQK , Boyenle IA , Ogunlana AT , Adeyemi RO , et al . Molecular modeling in drug Discovery. Informatics in Medicine Unlocked. 2022; 29: 100880. Disponível em: [ https://doi.org/10.1016/j.imu.2022.100880 ].
» https://doi.org/10.1016/j.imu.2022.100880 - 78 Pushkaran AC , En PN , Melge AR , Puthiyedath R , Mohan GC . Searching Phytochemical based Medication for SARS-CoV 2 infection by Molecular docking models towards Spike glycoprotein and Main Protease. RSC Av. 2021; 11: 12003-12014. Disponível em: [ https://doi.org/10.1039/D0RA10458B ].
» https://doi.org/10.1039/D0RA10458B - 79 Morris GM, Lim-wilby M. Molecular docking. Methods Mol Biol. 2008; 443: 365-82. Disponível em: [ https://doi.org/10.1007/978-1-59745-177-2_19 ].
» https://doi.org/10.1007/978-1-59745-177-2_19 - 80 Rogers DM , Agarwal R , Vermaas JV , et al . SARS-CoV2 billion compound docking. Sci Data. 2023; 10: 173. Disponível em: [ https://doi.org/10.1038/s41597-023-01984-9 ].
» https://doi.org/10.1038/s41597-023-01984-9 - 81 BadhanI B , Sharma N , Kakkar R . Gallic acid: a versatile antioxidant with promising therapeutic and industrial applications. RSC Adv. 2015; 5: 27540-27557. Disponível em: [ https://doi.org/10.1039/C5RA01911G ]
» https://doi.org/10.1039/C5RA01911G - 82 Bhuia MDS , Rahaman MDM , Islam T , et al . Neurobiological effects of gallic acid: current perspectives. Chin Med. 2023; 18: 27. Disponível em: [ https://doi.org/10.1186/s13020 023-00735-7].
» https://doi.org/10.1186/s13020 023-00735-7 - 83 Fernandes FHA, Salgado HRN. Gallic Acid: Review of the Methods of Determination and Quantification. Critical Rev Analytic Chem. 2016; 46(3): 257-265. Disponível em: [ https://doi.org/10.1080/10408347.2015.1095064 ].
» https://doi.org/10.1080/10408347.2015.1095064 - 84 Baraskar K, Thakur P, Shrivastava R, Shrivastava VK.Therapeutic Role of Phytophenol Gallic Acid for the Cure of COVID-19. Pathogen Endoc Metab Imm Disord - Drug Targets. 2023; 23(4). Disponível em: [ https://dx.doi.org/10.2174/1871530322666220829141401 ].
» https://dx.doi.org/10.2174/1871530322666220829141401 - 85 Badhani B , Kakkar R . Influence of intrinsic and extrinsic factors on the antiradical activity of Gallic acid: a theoretical study. Struct Chem. 2018; 29: 359-373. Disponível em: [ https://doi.org/10.1007/s11224-017-1033-9 ].
» https://doi.org/10.1007/s11224-017-1033-9 - 86 LeopoldinI M, Pitarch IP, Russo N, Toscano M. Structure, Conformation, and Electronic Properties of Apigenin, Luteolin, and Taxifolin Antioxidants. A First Principle Theoretical Study. J Physic Chem A. 2004; 108(1): 92-96. Disponível em: [ https://doi.org/10.1021/jp035901j ].
» https://doi.org/10.1021/jp035901j - 87 Sroka Z, Cisowski W. Hydrogen peroxide scavenging, antioxidant and anti-radical activity of some phenolic acids. Food Chem Toxicol. 2003; 41(6): 753-758. [ https://doi.org/10.1016/s0278-6915 (02)00329-0].
» https://doi.org/10.1016/s0278-6915 (02)00329-0 - 88 Zahrani NA , Al ES , Reda M , Asiri M . Recent developments of gallic acid derivatives and their hybrids in medicinal chemistry: A review. Europ J Medic Chem. 2020; 204: 112609. Disponível em: [ https://doi.org/10.1016/j.ejmech.2020.112609 ]
» https://doi.org/10.1016/j.ejmech.2020.112609 - 89 Tirado-kulieva VA , Hernández-martínez E , Choque R , Tania J . Phenolic compounds versus SARS-CoV-2: An update on the main findings against COVID-19. Heliyon. 2022; 8(9): e10702. Disponível em: [ https://doi.org/10.1016/j.heliyon.2022.e10702 ].
» https://doi.org/10.1016/j.heliyon.2022.e10702 - 90 Umar HI, Siraj B, Ajayi A, Jimoh TO, Prosper Obed. Molecular docking studies of some selected gallic acid derivatives against five non-structural proteins of novel coronavirus. J Genet Eng Biotechnol. 2021; 19(1): 16. Disponível em: [ https://doi.org/10.1186/s43141-021-00120-7 ].
» https://doi.org/10.1186/s43141-021-00120-7 - 91 Hadidi M, Liñán-Atero R, Tarahi M, Christodoulou MC, Aghababaei F. The Potential Health Benefits of Gallic Acid: Therapeutic and Food Applications. Antioxidants (Basel). 2024 Aug 18; 13(8): 1001. Disponível em: [ https://doi.org/10.3390/antiox13081001 ].
» https://doi.org/10.3390/antiox13081001 - 92 Alhyari D , Qinna NA , Sheldrake HM , Kantamneni S , Ghanem BY , Paluch KJ . Antioxidant, Anti-Inflammatory, and Oral Bioavailability of Novel Sulfonamide Derivatives of Gallic Acid. Antioxidants. 2025; 14: 374. Disponível em: [ https://doi.org/10.3390/antiox14040374 ].
» https://doi.org/10.3390/antiox14040374 - 93 Aghasafari P , George U , Pidaparti R . A review of inflammatory mechanism in airway diseases. Inflamm Res. 2019; 68: 59-74. Disponível em: [ https://doi.org/10.1007/s00011-018-1191-2 ].
» https://doi.org/10.1007/s00011-018-1191-2 - 94 Chavda VP , Bezbaruah R , Ahmed N , Alom S , Bhattacharjee B , Nalla LV , et al . Proinflammatory Cytokines in Chronic Respiratory Diseases and Their Management. Cells. 2025: 14: 400. Disponível em: [ https://doi.org/10.3390/cells14060400 ].
» https://doi.org/10.3390/cells14060400 - 95 Alhyari D , Qinna NA , Sheldrake HM , Kantamneni S , Ghanem BY , Paluch KJ . Antioxidant, Anti-Inflammatory, and Oral Bioavailability of Novel Sulfonamide Derivatives of Gallic Acid. Antioxidants. 2025; 14: 374. Disponível em: [ https://doi.org/10.3390/antiox14040374 ].
» https://doi.org/10.3390/antiox14040374 - 96 Aatl HY, IsmaiL A, Rateb ME, Aboulmagd AM, Hassan HM, Hetta MH. Garcinia cambogia Phenolics as Potent Anti-COVID-19 Agents: Phytochemical Profiling, Biological Activities, and Molecular Docking. Plants (Basel). 2022 Sep 26; 11(19): 2521. Disponível em: [ https://doi.org/10.3390/plants11192521 ].
» https://doi.org/10.3390/plants11192521 - 97 Khan T , Khan MA , Mashwanl ZUR , Ullah N , Nadhman A . Therapeutic potential of medicinal plants against COVID-19: The role of antiviral medicinal metabolites. Biocatal Agric Biotechnol. 2021 Jan; 31: 101890. Disponível em: [ https://doi.org/10.1016/j.bcab.2020.101890 ].
» https://doi.org/10.1016/j.bcab.2020.101890 - 98 Yushu G, Miaomiao L, Bart LS, Garry WB, Ronald JQ. Drug-Repurposing Screening Identifies a Gallic Acid Binding Site on SARS-CoV-2 Non-structural Protein 7. ACS Pharmacol Translat Sci. 2023; 6(4): 578-586. Disponível em: [ https://doi.org/10.1021/acsptsci.2c00225 ].
» https://doi.org/10.1021/acsptsci.2c00225 - 99 Souza GB, Pontes CLM, Costa GO, et al. Inhibitory Effects of Mangifera indica Secondary Metabolites and Their Synthetic Derivatives against SARS-CoV-2 M pro and NS2B/NS3 (ZIKV and DENV-2). ACS Omega. 2024; 9(44): 44624-44638. Disponível em: [ https://doi.org/10.1021/acsomega.4c07148 ].
» https://doi.org/10.1021/acsomega.4c07148 - 100 Carvalho MAG , Souza GB , Tizziani T , et al . Synthesis, in vitro and in silico evaluation of gallamide and selenogallamide derivatives as inhibitors of the SARS-CoV-2 main protease. Arch Pharm. 2024; 357: e2400253. Disponível em: [ https://doi.org/10.1002/ardp.202400253 ].
» https://doi.org/10.1002/ardp.202400253
-
Fonte de Financiamento:
CAPES pelo Edital Emergencial intitulado Fármacos e lmunologia n° 011/2020.
Datas de Publicação
- Publicação nesta coleção
4 Mai 2026 - Data do Fascículo
2026
Histórico
- Recebido
18 Out 2025 - Aceito
04 Mar 2026
 Ácido Gálico e seus derivados: candidatos promissores no combate às proteases virais do SARS-CoV-2
Ácido Gálico e seus derivados: candidatos promissores no combate às proteases virais do SARS-CoV-2
 Fonte: Adaptado de Wang[29].
Fonte: Adaptado de Wang[29].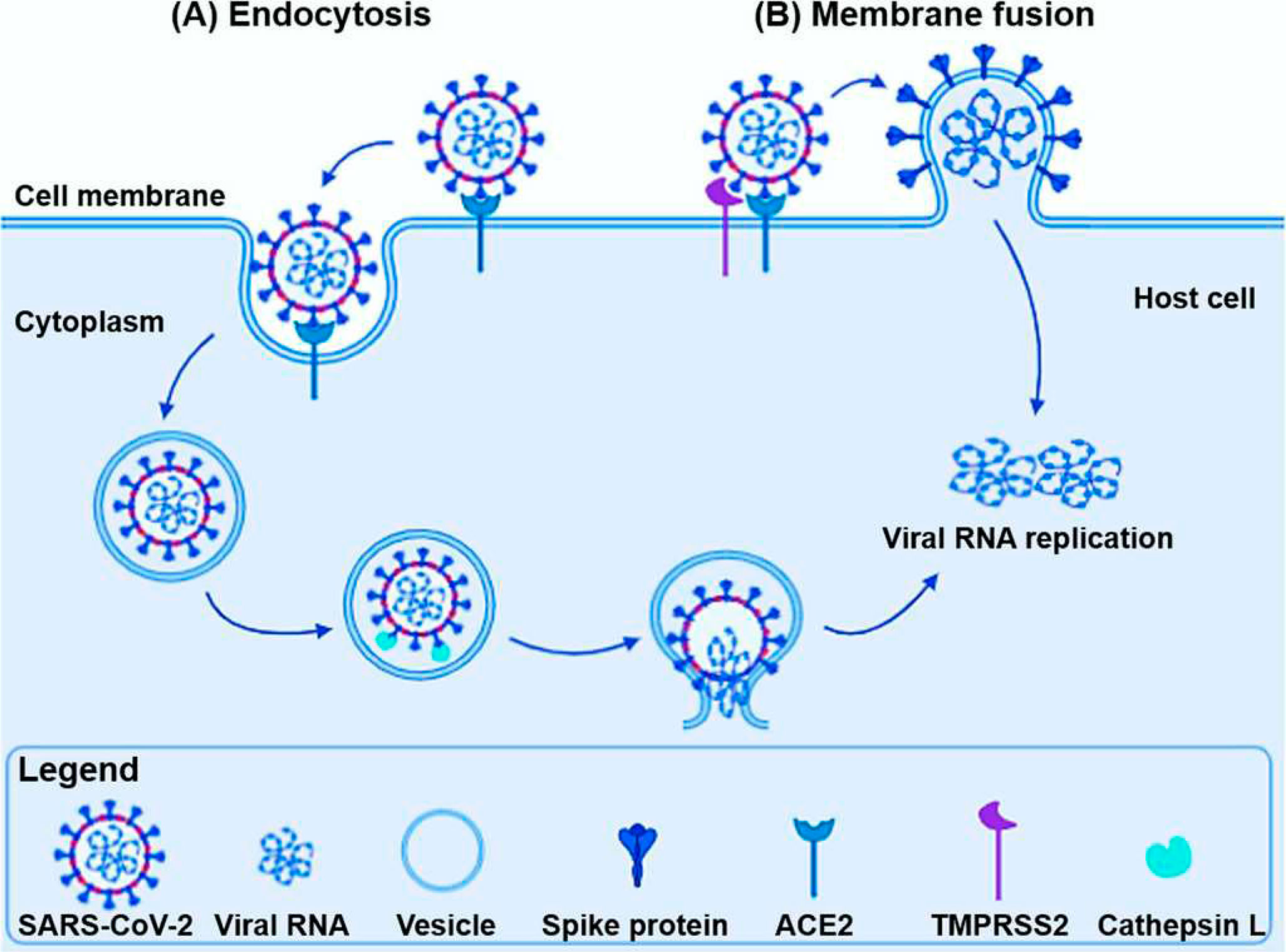 Fonte: Adaptado de Pislar[44].
Fonte: Adaptado de Pislar[44].
 Fonte: Adaptado de Zahrani[88].
Fonte: Adaptado de Zahrani[88].