Estado da Arte
Extração Supercrítica: Aspectos Técnicos e Econômicos
Supercritical Extraction: Technical and Economical Issues
Resumo
Este trabalho discute alguns aspectos técnicos e econômicos da extração supercrítica. As principais etapas para o desenvolvimento do processo são discutidas em termos da elaboração de extratos de macela (Achyrocline alata e Achyrocline satureioides) e cravo-da-índia (Eugenia caryophyllus). Dados de processo tais como a temperatura, a pressão e o rendimento são apresentados para a obtenção de extratos de pimenta-do-reino (Piper nigrum), capim limão (Cymbopogon citratus), bacuri (Platonia insignis), recuperação de carotenóides de resíduos das fibras de dendê (Elaeis guineensis), Artemísia (Artemisia annua), erva-baleeira (Cordia verbenacea), funcho (Foeniculum vulgare), alecrim (Rosmarinus officinalis), gengibre (Zingiber officinale), erva-doce (Pimpinela anisum), etc..
- Unitermos
- Extração Supercrítica.
- Dióxido de Carbono Pressurizado.
- Dióxido de Carbono Comprimido.
- Projeto de Processo..
Abstract
This work discusses some technical and economical issues related to supercritical extraction. The major steps in process development are discussed as applied to obtaining extracts from macela (Achyrocline alata and Achyrocline satureioides) and clove buds (Eugenia caryophyllus). Process data such as temperature, pressure, and yield are presented for obtaining extracts from black pepper (Piper nigrum), lemongrass (Cymbopogom citratus), bacuri (Platonia insignis), recovery of carotenoids from palm (Elaes guineensis) residue, Artemisia (Artemisia annua), ervabaleeira (Cordia verbenacea), fennel (Foeniculum vulgare), rosemary (Rosmarinus officinalis), ginger (Zingiber officinale), anise (Pimpinella anisum), etc.
- Key words
- Supercritical Fluid Extraction.
- Pressurized Carbon Dioxide.
- Compressed Carbon Dioxide.
- Process Design..
Introdução
O fenômeno do aumento do poder de solvatação de alguns gases, quando próximos ao ponto crítico, é conhecido desde o século XIX, tendo sido descrito pela primeira vez por Hannay e Hogarth em 1979, segundo McHugh e Krukonis (1986). Em 1936 foi concedida a primeira patente na área para desasfaltação de petróleo (McHUGH e KRUKONIS, 1986). Por volta de 1973, quando da primeira grande crise da indústria petrolífera, parte da comunidade acadêmica acreditou que a extração supercrítica (SFE = Supercrítical Fluid Extraction) pudesse ser uma alternativa aos processos convencionais de extração. Isto, por ser menos intensiva no uso de energia. No entanto, atualmente, com o desenvolvimento de uma base sólida de conhecimento técnico, sabe-se que as motivações pelo uso da SFE estão respaldadas em dois pontos: (1) obtenção de produtos de maior qualidade e (2) uso de tecnologia não agressiva ao meio ambiente. Nos processos de extração convencionais, mesmo quando o solvente de extração é benigno, como o etanol, misturas etanol e água, ou solventes similares, existem inúmeras vantagens para se optar pela SFE. Estes fatos só ficam aparentes quando se considera o processo de produção de um extrato botânico de maneira sistêmica, ou seja, consideram-se todas as etapas do processo tais como: preparo da matriz botânica, extração, remoção do solvente e/ ou umidade, remoção do solvente da torta sólida, padronização do extrato, destinação dos co-produtos, etc. Por exemplo, do funcho podemos obter o óleo volátil por destilação por arraste a vapor, neste caso teríamos como produto o óleo volátil e como subproduto ou co-produto o resíduo sólido que depois de submetido ao processo de secagem poderia ser, por exemplo, utilizado na produção de saches aromatizantes. Se, alternativamente, SFE fosse empregada, além do óleo volátil e do resíduo sólido, um outro co-produto poderia ser obtido: o óleo fixo formado por uma mistura de ácidos graxos e substâncias lipídicas presentes abundantemente nas sementes de funcho (MOURA et al., 2005). Nesta alternativa de processo, na qual nos primeiros 60 minutos de processo se obtém o óleo volátil, e em seguida o óleo fixo; podem-se apontar duas vantagens: (1) a extração das substâncias lipídicas deixaria o resíduo sólido menos vulnerável à oxidação e conseqüente menos vulnerável ao surgimento de artefatos que degradariam a qualidade odorífera do sache, (2) o resíduo sólido não requer secagem. Outro exemplo contundente é o do extrato de vetiver conforme mostrado por Martinez e colaboradores (2004), cujo tempo de extração por SFE é de cerca de 1h a 200 bar e 40 oC e com rendimento de 3,2 % (base planta seca - b.s.). Para o processo de hidrodestilação após vários tratamentos das raízes de vetiver, tais como o uso de N2, NaOH e enzimas, o rendimento do processo foi de 1,8 % (b.s.) num período de 16 horas. Certamente, o aumento no rendimento do extrato obtido por SFE deveu-se à co-extração de compostos mais pesados, que, em principio, não representam um problema de processo, pois estas substâncias podem encontrar facilmente uma destinação lucrativa, além do que, a fração mais volátil do extrato pode ser separada durante o processo de extração.
Extração Supercrítica: uma tecnologia estabelecida
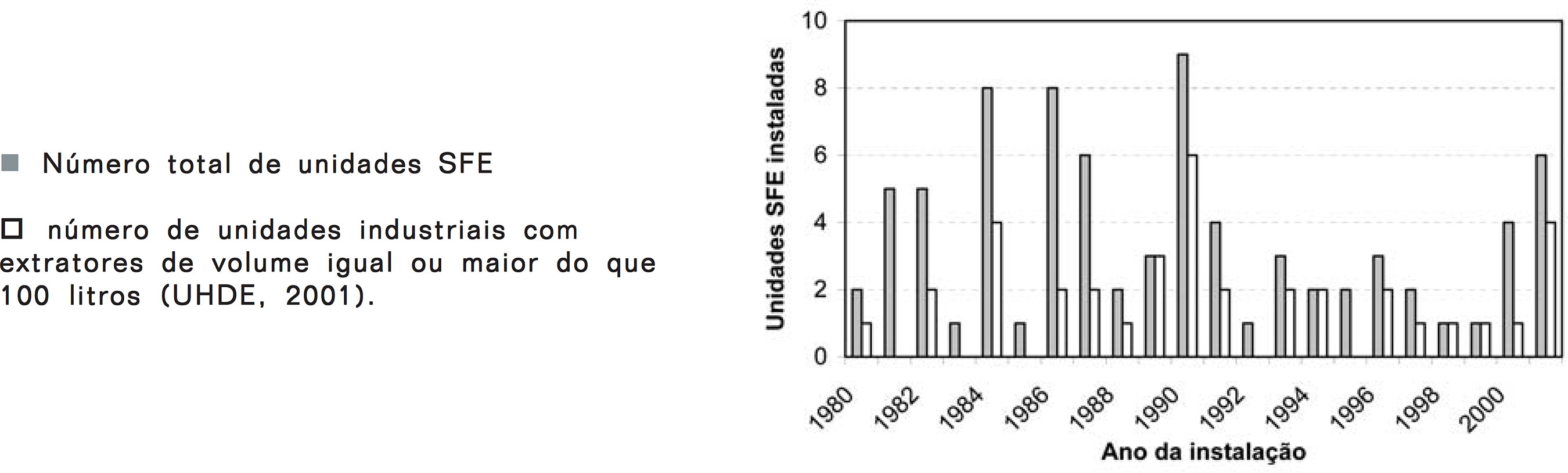
SFE a partir de matrizes sólidas é considerada uma tecnologia já estabelecida. Numa pesquisa bibliográfica realizada para o período de janeiro de 2001 a junho de 2003, nas bases de dados: ‘ISI Web of Science’ e na ‘Scirus for scientific information only’ foram encontrados 514 e 696 artigos, respectivamente (MEIRELES, 2003). A pesquisa brasileira na área é bastante expressiva no cenário mundial conforme compilação de dados realizada por Rosa e Meireles (2005b) para o período de 1994 até 2004. Na Figura 1 encontra-se os números de unidades SFE instaladas, por um dos maiores fabricantes de equipamentos SFE, de 1980 até 2002. Na Figura 1 mostram-se também os números de unidades SFE industriais, ou seja, aquelas cujos extratores têm volume igual ou maior do que 100 litros, com capacidade de processar aproximadamente 50 kg de matéria-prima seca por batelada. Estes números corroboram que a tecnologia já se disseminou no ambiente industrial, embora no Brasil ou em qualquer outro país da América do Sul, nenhuma planta industrial tenha sido instalada. Segundo Fukuzato (2003), durante a década de 1980 foram instaladas 9 industrias no Japão com extratores de 200 a 1.200 litros. Na década de 1990 foram instaladas fábricas no Japão (4), na Coréia (2), em Taiwan (1) e na China (6) com extratores de 170 a 500 litros, enquanto que a partir do ano 2000 foram instaladas 8 fabricas na China e apenas 1 no Japão, cujos extratores têm volume de 500 a 3.500 litros. Estes números indicam um movimento importante dos países asiáticos na adoção da tecnologia SFE.
O que é extração supercrítica?
Originalmente, era o nome dados aos processos que empregam gases pressurizados como solvente de extração. Atualmente, extração supercrítica pode designar uma variedade de processos tais como: (1) processos nos quais o solvente de extração é um gás quando nas condições normais de temperatura e pressão. O melhor exemplo de solvente para este caso é o dióxido de carbono por suas características tais como: ser inerte ao corpo humano e à matriz biológica, ter condições críticas amenas (31 oC e 73,8 bar); mas, outros gases como o propano, etano, NO2 também são utilizados; (2) processos nos quais o solvente de extração é um líquido quando nas condições normais de temperatura e pressão. Neste caso, os processos de extração com água superaquecida representam os melhores exemplos; (3) processos onde o solvente de extração é formado por uma mistura de duas ou mais substâncias, em geral, sendo que nas condições normais de temperatura e pressão uma delas é um gás e a(s) outra(s) líquida(s). Por exemplo, o etanol foi utilizado por diversos autores como cosolvente ou modificador do dióxido de carbono para extração de substâncias mais polares (Tabela 1). Neste caso, o processo denomina-se de SFE com cosolvente.
| Nome vulgar | Nome botânico | Principio ativo | Cosolvente | Temperatura ( o C) | Pressão (bar) | Rendimento
|
Referência |
| Bacuri | Platonia insignis | Ácidos graxos | Etanol | 16 - 21 | 63 - 70 | 0,22 - 0,49 | |
| Cúrcuma | Curcuma longa | Curcuminóides | Etanol | 30 | 200 - 300 | 5,8 | |
| Isopropanol | 30 | 200 - 300 | 5,7 - 8,0 | ||||
| Etanol + Isopropanol | 30 | 200 - 300 | 5,9 - 8,0 | ||||
| Estévia | Stevia rebaudiana | Glicosídeos | Água | 16 - 45 | 120 - 200 | 3,4 - 0,59 | |
| Etanol | 16 - 45 | 65 - 200 | 0,12 - 0,34 | ||||
| Água + Etanol | 16 - 45 | 120 - 200 | 0,39 - 0,41 | ||||
| Gengibre | Zingiber officinalis | Oleoresina | Etanol | 25 - 35 | 200 - 250 | 1,9 - 2,5 | |
| Isopropanol | 25 - 35 | 200 - 250 | 2,0 - 2,2 | ||||
| Khoa | Satureja boliviana | Óleo essencial | Etanol | 16 - 21 | 65 - 70 | 3,2 - 5,0 | |
| Leiteira de 2 irmãos | Tabernaemontana catharinensis | Coronaridina + voacangina | Etanol | 35 - 55 | 200 - 300 | 0,42 - 0,70 | |
| Água | 45 | 250 | 15,8 | ||||
| Etanol | 45 | 250 | 2,5 | ||||
| Isopropanol | 45 | 250 | 2,5 | ||||
| Etanol + Isopropanol | 45 | 250 | 2,3 | ||||
| Manjericão | Ocimum basilicum fenólicos | Compostos | Água | 30 | 100 - 300 | 8,0 - 11,0 | |
| 1 Rendimento em extrato bruto. | |||||||
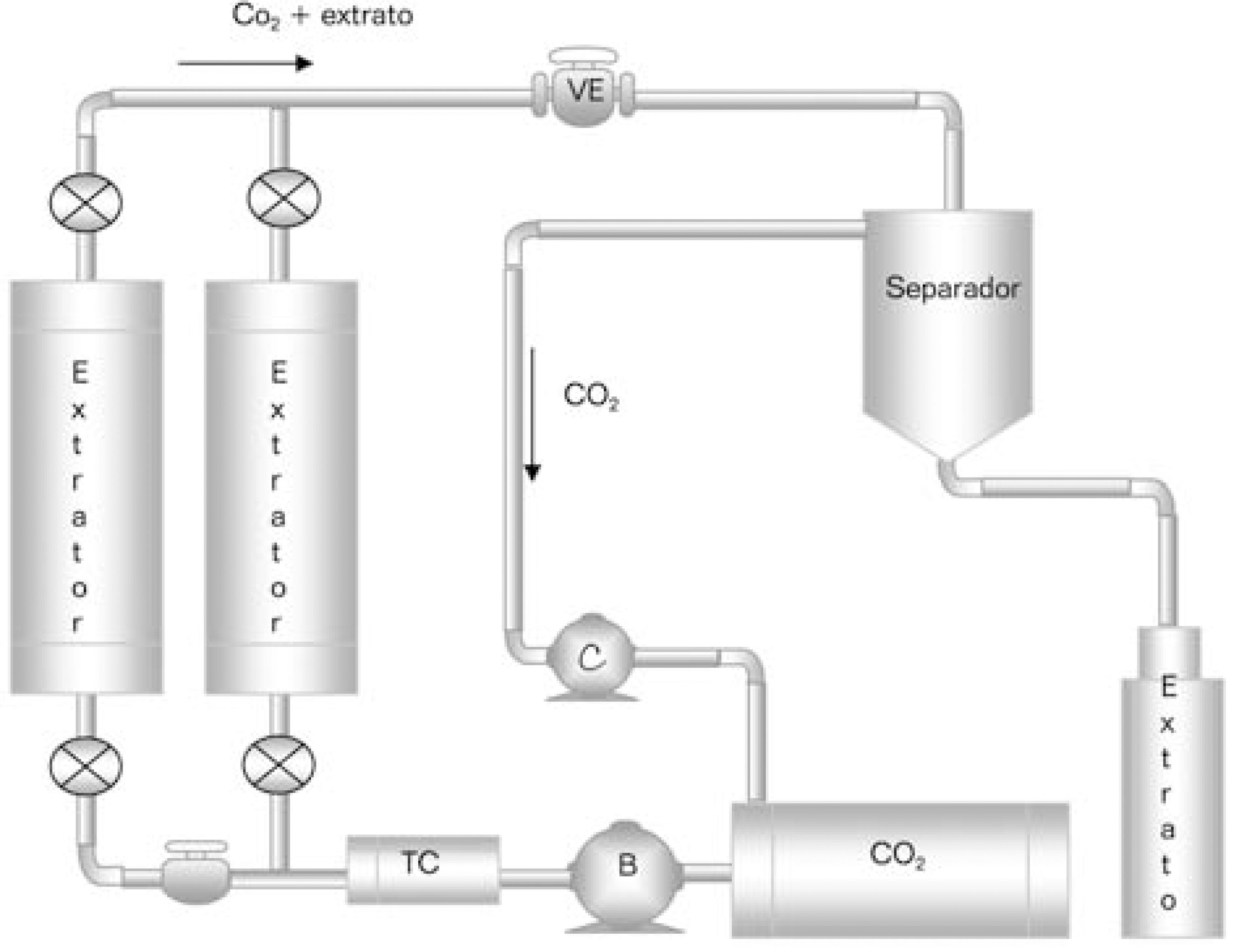
Independentemente do solvente utilizado, o processo SFE é realizado a pressões bem acima da pressão atmosférica, portanto, o solvente de extração é pressurizado através de bombas ou compressores até a pressão de processo. A Figura 2 mostra como a densidade do dióxido de carbono varia devido à aplicação de pressão sobre o mesmo; esta mudança na densidade é acompanhada por um aumento no poder de solvatação do fluido. Na Figura 3 encontrase um fluxograma de uma unidade SFE, na qual dióxido de carbono é o solvente de extração. Geralmente, as instalações industriais possuem 2 extratores, sendo que um deles se encontra em operação durante o ciclo de extração e o outro está sendo limpo e preparado para entrar em operação; desta forma, o processo pode se aproximar de operação contínua. No reservatório de solvente (CO2) a pressão é de aproximadamente 20 bar, para ser utilizado no processo o dióxido de carbono é pressurizado com a bomba (B) a pressões, em geral, acima de 100 bar e, se for necessário, é aquecido no trocador de calor (TC). O solvente na condição de processo passa por um dos extratores e, na seqüência, a mistura extrato/ solvente é submetida à descompressão no sistema válvula de expansão (VE)/separador. Nesta etapa, a pressão do sistema decresce, o solvente perde o poder de solvatação, o extrato se separa e o solvente retorna ao tanque de armazenamento com o auxílio do compressor (C). Portanto, SFE é conduzida em equipamentos que resistem às pressões de processo, desta forma, estamos falando de custo de investimento elevado quando comparado com o custo de extratores e/ou destiladores que operam a baixas pressões. Por exemplo, uma unidade SFE piloto contendo 2 extratores de 5 litros (capacidade para aproximadamente 2,5 kg de matéria prima) pode custar de US$ 100 a 200 mil dependendo da instrumentação e dos periféricos. Por outro lado, o custo de uma unidade industrial com 2 extratores de 400 litros (capacidade para aproximadamente 200 kg de matéria prima), custava, em 1998, cerca de US$ 2 milhões, atualmente, o preço varia de US$ 1,5 a 1,8 milhões; o decréscimo no custo deve-se ao desenvolvimento da engenharia do processo SFE. Logo, para a manutenção das características de tecnologia amigável com o meio ambiente e, simultaneamente, justificar os custos de investimento, é importante que os solventes utilizados em SFE sejam do tipo GRAS (Generally Recognized as Safe). Seria pouco defensável o uso de SFE no caso de se utilizar solventes que sejam nocivos à saúde humana e/ou agridam o meio ambiente. No entanto, existem algumas exceções, o consumo de solventes para, por exemplo, preparo de amostras, pode ser enormemente diminuído com o uso de SFE com cosolvente. Braga e colaboradores (2003) mostraram que a quantidade de etanol necessária para a obtenção de extratos de cúrcuma é 10 vezes menor para SFE com cosolvente quando comparada com o processo de extração à pressão ambiente. Portanto, o uso de solventes não GRAS em SFE pode ser justificável quando é uma solução para a redução do consumo de solventes mais agressivos, seja em cromatografia preparativa seja no processo em escala industrial.

Protocolo para desenvolvimento do processo SFE
Quando SFE é considerada uma alternativa de processo e o solvente selecionado é o dióxido de carbono, de imediato deve-se excluir a obtenção de extratos ricos em proteínas e carboidratos, uma vez que proteínas e carboidratos são insolúveis em dióxido de carbono. Tendo-se optado pelo uso de SFE, uma das primeiras etapas do projeto do processo será a de redução da umidade da matriz biológica. A água, muito embora seja usada como cosolvente em alguns processos para a extração de alcalóides (McHUGH; KRUKONIS, 1986) e glicosídeos (PASQUEL et al., 2000), influi negativamente na extração de várias substâncias tais como terpenóides e substâncias lipídicas. Em geral, a umidade da matriz biológica não deve ser superior a 18% (base úmida), para flores, folhas e sementes um processo de secagem simples pela exposição ao ar pode ser empregado. No caso de alguns rizomas, como cúrcuma e gengibre, cujas umidades originais são maiores do que 70% será necessário usar um secador com circulação forçada de ar. As próximas etapas para o desenvolvimento do processo SFE serão agrupadas em 3 categorias: (1) Seleção da condição de temperatura e pressão de extração, (2) Seleção do tempo de extração e, (3) Estudo do aumento de escala para o processo. A literatura contém grande quantidade de informações para as 2 primeiras etapas do desenvolvimento do processo SFE como atestam as inúmeras publicações na área (MEIRELES, 2003; ROSA; MEIRELES, 2005b). Em relação ao aumento de escala as informações são bastante restritas, alguns poucos trabalhos recentes se dedicaram a este estudo (BRAVI et al., 2002; CARVALHO Jr et al., 2005; MOURA et al., 2005; PERRUT, 2000), a maior parte da informação é detida pelos fabricantes de equipamentos que comercializam tanto os equipamentos quanto o desenvolvimento do processo SFE.
Etapa 1: Seleção da temperatura e pressão de operação
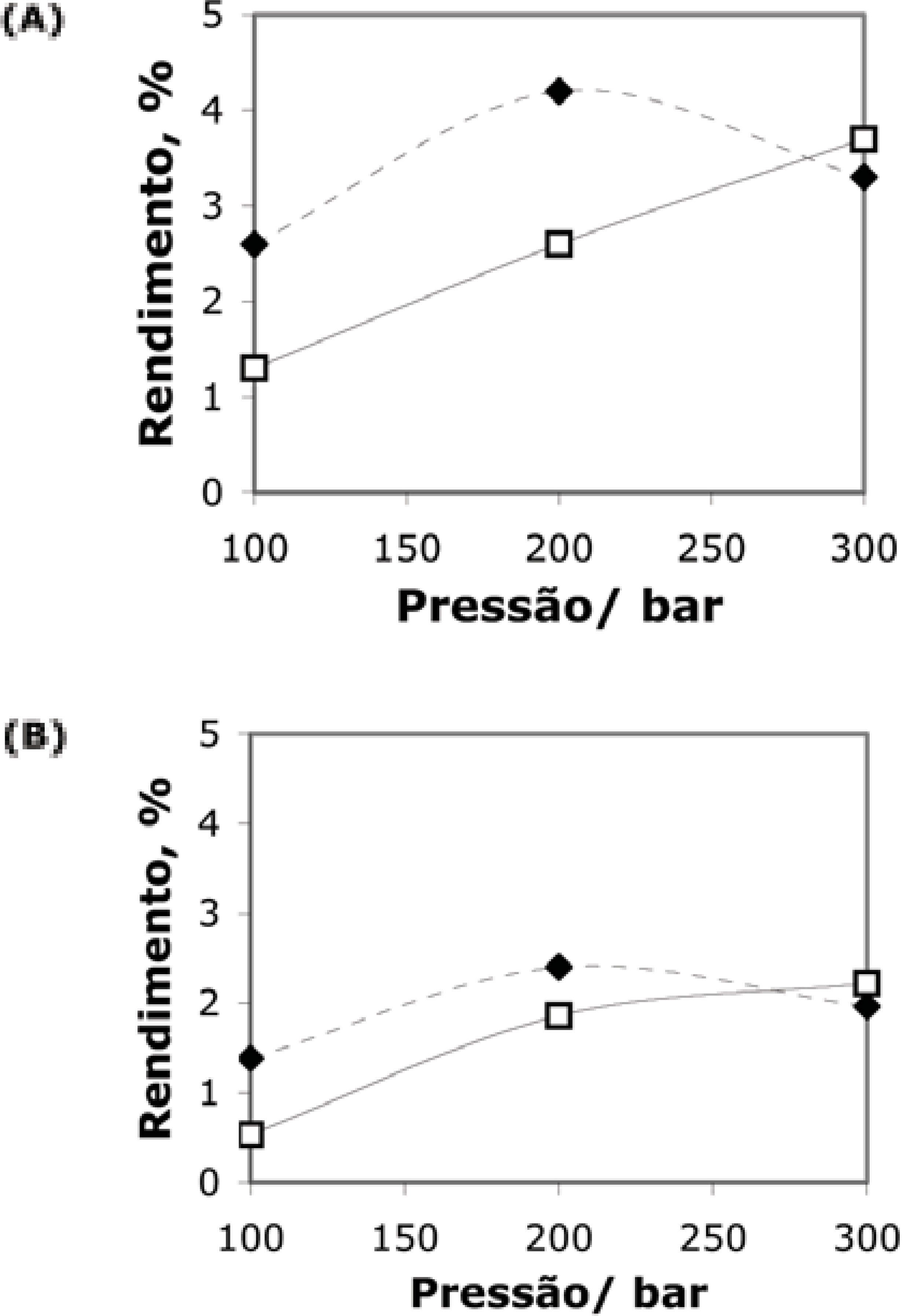
Esta etapa do projeto do processo SFE é decisiva para a posterior otimização do processo. Inicialmente, a definição do composto alvo ou biomarcador indicará ou não a necessidade do uso de cosolvente (Tabela 1). A seguir, deve-se proceder à determinação das isotermas de rendimento global (GYI = Global Yield Isotherms) em pelo menos 2 temperaturas, muito embora o ideal sejam 3 temperaturas para que as pressões de inversão possam ser corretamente identificadas. A Figura 4 mostra as (GYI) para SFE de espécies de macela onde a pressão de inversão é aproximadamente igual a 280 bar. Leal (2005) determinou que os compostos majoritários dos extratos das folhas de macela, detectáveis por CG-DIC, são o beta-cariofileno e o alfa-humuleno. O extrato SFE obtido a 200 bar e 30 oC contém 25,7 % (área relativa) e 4,4% de beta-cariofileno para A. alata e A. satureioides, respectivamente. O extrato SFE de A. alata obtido a 300 bar e 40 oC contém 31,9% e o da A. satureioides apenas traços desta substância. Uma análise da Figura 4 mostra que o rendimento global a 200 bar e 30 oC foi maior do que o obtido a 300 bar e 40 oC para ambas as espécies. Para a seleção da condição de extração será necessário considerar o composto alvo. Supondo que o beta-cariofileno seja selecionado como composto alvo, então, a 200 bar e 30 oC obter-se-iam 10,8 mg/100g de planta seca e a 300 bar e 40 oC 11,8 mg/100g de planta seca. Portanto, a decisão sobre a condição de extração dependerá de um balanço energético aonde sejam considerados os custos de refrigeração (operação a 30 oC) e pressurização (operar a 200 ou 300 bar), para verificar se o aumento de 1 mg/100 g de planta seca no rendimento, justifica a operação da unidade SFE a 300 bar e 40 oC. Nesta etapa do projeto, os dados experimentais podem ser obtidos em unidades SFE com extratores de 5 a 50 mL; o uso de extratores de maior volume é possível, muito embora não indicado pelo expressivo acréscimo do tempo de experimentação e, conseqüentemente, dos custos.
Etapa 2: Seleção do tempo de extração
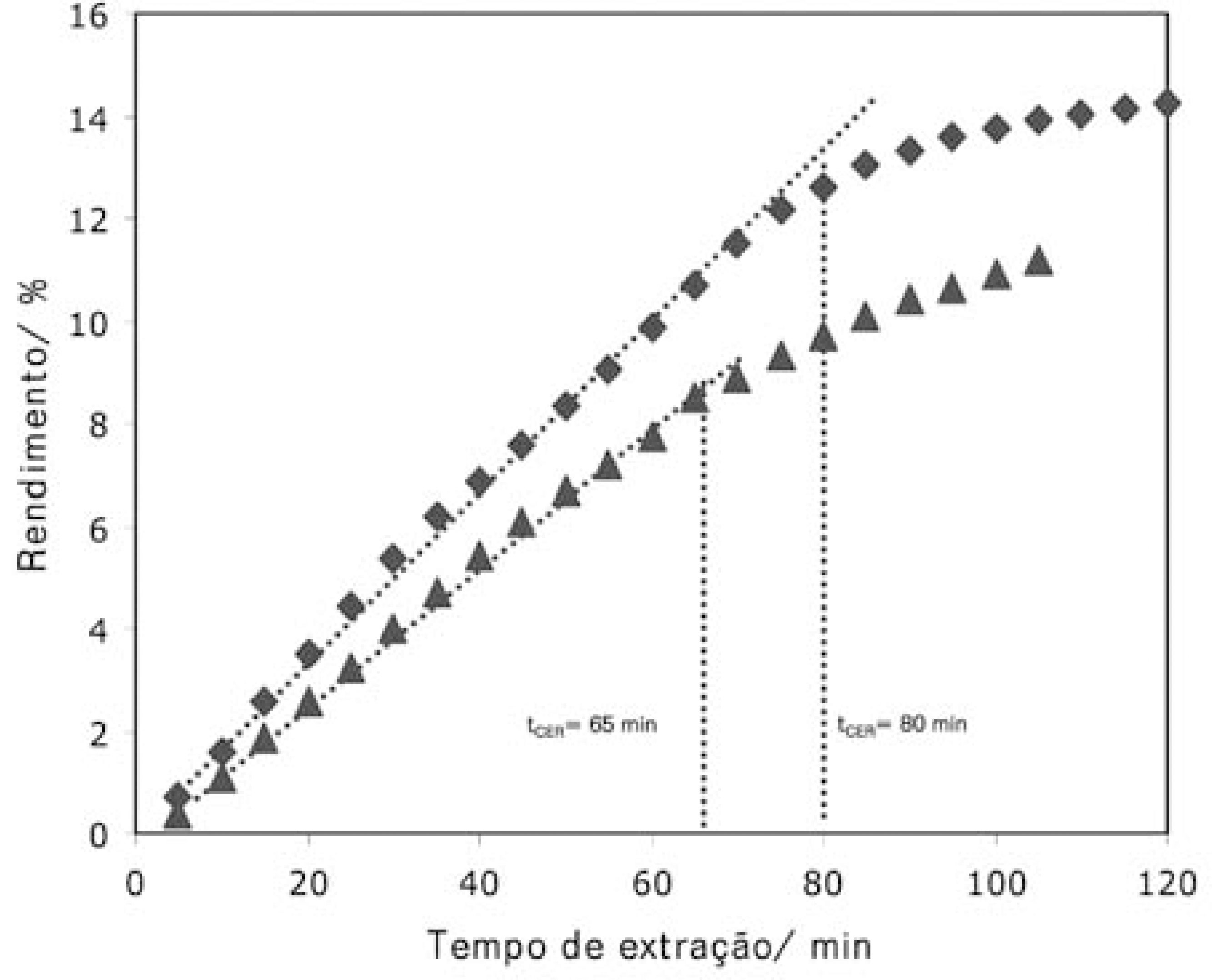
A determinação do tempo de processo é feita pela análise de uma curva global de extração (OEC = overall extraction curve) que permite a determinação da velocidade de extração. A experimentação deve ser conduzida em unidades SFE com extratores de volume de 50 a 500 mL; em alguns casos, para matrizes sólidas muito diluídas recomenda-se o uso de extratores de maior volume, mas apenas excepcionalmente. A Figura 5 mostra curvas de extração para o sistema óleo-decravo + CO2 (RODRIGUES, 2001). A curva de extração indica que o processo de extração pode ser dividido em 3 etapas: (1) período de velocidade constante de extração (CER = Constant extraction rate) no qual o soluto facilmente acessível ao solvente é extraído, (2) período de velocidade decrescente de extração (FER = falling extraction rate) no qual tanto os solutos de fácil quanto o de difícil acesso são extraídos e, (3) período difusional (DC = diffusion controlled) no qual apenas soluto de difícil acesso é extraído. Da curva de extração, por um ajuste de spline linear com 2 retas (FREUND e LITTELL, 1995) obtém-se o tempo de extração (tCER), ou seja, a duração da etapa CER e a velocidade de extração (MCER) neste período. Em geral, a análise econômica indicará que o processo de extração deve ser conduzido até o final da etapa CER, continuar com o processo de extração para além deste tempo só se justificará em casos especiais, por exemplo, quando o composto alvo é obtido justamente durante o período de velocidade decrescente ou controlado pela difusão. Na Figura 5 estão indicados os tempos de extração tCER para as temperaturas de 25 e 35 oC; nestas temperaturas as velocidades de extração são MCER = 0,35 g/min e MCER = 0,27 g/min, respectivamente. Desta forma, o aumento de temperatura resultou em diminuição da velocidade de extração, indicando que para este sistema a extração na temperatura de 25 oC é mais vantajosa. A curva de extração para a temperatura de 25 oC mostra claramente que o ganho de rendimento após 80 min, cerca de 2% dificilmente justificará a continuidade do processo para além de tCER.
Etapa 3: Aumento de escala e otimização do processo
Esta etapa, que requer o uso de unidades SFE com extratores de pelo menos 5 litros; curvas de extração serão obtidas de modo que por um processo de tentativa/aprendizado sejam otimizados o tempo de extração, o consumo de solvente e as condições de separação. Nesta etapa, as informações obtidas serão utilizadas para estimativas do custo de manufatura. Rosa e Meireles (2005a) fizeram, usando dados de Rodrigues et al. (2002) e Martínez et al. (2003a), cálculos de custos de manufatura para óleo de cravoda-índia e oleoresina de gengibre. Os valores calculados foram US$ 9,0/kg de óleo de cravoda-índia e US$ 100/kg de oleoresina de gengibre. Nos dois casos, os custos representam estimativas iniciais, pois foram obtidos usando-se as informações experimentais medidas em unidades SFE de tamanho de laboratório. Estimativas mais realistas dos custos só podem ser determinadas a partir de dados experimentais medidos em unidades SFE de tamanho piloto, ou seja, com extratores de volume igual ou maior do que 5 litros.
Desenvolvimento do processo SFE: alguns exemplos do LASEFI
Nas Tabelas 1 acima e na 2 abaixo são mostrados alguns exemplos de processos em desenvolvimento no LASEFI. Na Tabela 1 encontram-se sistemas para os quais cosolvente foi utilizado para possibilitar a extração do(s) composto(s) de interesse; nestes exemplos, as quantidades de cosolvente variaram de 5 a 10% (massa). Na Tabela 2, para algumas plantas as condições de extração já foram otimizadas, para o composto alvo indicado, como é o caso do alecrim, artemísia, erva-baleeira, funcho.
Outras aplicações de fluidos supercríticos
Os fluidos supercríticos têm encontrado inúmeras outras aplicações em diferentes áreas do processamento de materiais biológicos e químicos. Por exemplo, nas áreas de polímeros, cerâmica, espumas, aerogéis, desenho de partículas, limpeza a seco, esterilização e ruptura celular, microencapsulamento, reações, produção de biodiesel, cromatografia supercrítica, etc (BRUNNER et al., 2003). O bagaço de gengibre foi utilizado por Moreschi et al. (2004) para hidrólise com água e dióxido de carbono. Adicionalmente a todas estas aplicações, a produção de frações bioativas de referência poderia representar um uso especialmente interessante de SFE, tendo em vista que unidades SFE com extratores de volume pequenos (500 a 100 mL) podem ser perfeitamente adequadas a esta aplicação.
| Nome vulgar | Nome botânico | Principio ativo | Temperatura ( o C) | Pressão (bar) | Rendimento 1 (%) | Referência |
| Alecrim 2 | Rosmarinus officinalis | Extrato bruto | 40 | 300 | 5,0 | |
| Alecrim pimenta 3 | Lippia sidoides | Óleo volátil/timol | 10 - 28 | 66,7 - 78,5 | 2,2 - 3,3 | |
| Alfavaca-cravo | Ocimum gratissimum | Óleo volátil/eugenol | 40 | 100 - 300 | 0,8 - 1,8 | |
| Artemísia 3 | Artemisia annua. | Artemisinina | 50 | 300 | 6,3 | |
| Camomila 4 | Chamomilla recutita | Óleo volátil/oleoresina | 30 - 40 | 100 - 200 | 0,82 - 4,3 | |
| Canela-de-cunhã 4 | Croton zehntneri | Óleo volátil/ anetol | 10 - 28 | 66.7 - 78.5 | 2,1 - 3,8 | |
| Capim-limão | Cymbopogon citratus | Óleo volátil | 5 - 24 | 69 - 74 | 0,30 - 0,40 | |
| Cidrão | Aloysia triphylla | Óleo volátil/oleoresina | 35 - 45 | 100 - 350 | 0,58 - 1,5 | |
| Citronela | Cymbopogon winterianus | Óleo volátil | 16 - 25 | 70 - 160 | 0,45 - 1,0 | Müller at al. (2001) |
| Cravo-da-índia | Eugenia caryophyllus | Óleo volátil | 10 - 25 | 66,7 - 100 | 9,6 - 14,1 | |
| Erva doce | Pimpinella anisum | Óleo volátil/anetol | 30 | 80 - 180 | 10,8 | |
| Erva-baleeira | Cordia verbenacea | Beta-cariofileno | 26 - 54 | 80 - 341 | 0,5 - 3,9 | |
| Erva-cidreira | Lippia alba | Óleo volátil | 40 - 50 | 80 - 120 | 1,5 - 5,0 | |
| Espirulina | Spirulina maxima | Ácidos graxos e carotenóides | 30 - 70 | 150 - 180 | 0,43 - 0,80 | |
| Estévia | Stevia rebaudian a | Óleo volátil | 30 | 200 | 2,9 | |
| Eucaliptos | Eucalyptus citriodora | Óleo volátil | 16 - 25 | 70 - 160 | 0,31 - 0,68 | |
| Fibra de dendê | Elaeis guineensis | Carotenóides | 45 - 55 | 200 - 300 | 1,8 - 5,3 | |
| Funcho3 | Foeniculum vulgare | Anetol e fenchona | 40 | 250 | 12,0 | |
| Gengibre | Zingiber officinale | Oleoresina | 25 - 35 | 200 - 250 | 1,9 - 2,5 | |
| Macela (folhas) | Achyrocline alata | Óleo volátil/flavonóides | 30 - 40 | 100 - 300 | 1,3 - 4,2 | |
| Achyrocline satureioides | Óleo volátil/flavonóides | 30 - 40 | 100 - 300 | 0,5 - 2,6 | ||
| Manga (folhas) | Mangifera indica | Antioxidantes | 45 | 250 | 1,0 | |
| Manjericão | Ocimum basilicum | Óleo volátil | 30 - 50 | 100 - 300 | 1,0 - 2,0 | |
| Palmarosa | Cymbopogon martini | Óleo volátil | 16 - 25 | 70 - 160 | 0,07 - 0,20 | |
| Pimenta-do-reino | Piper nigrum | Oleoresina | 13 - 20 | 63,5 - 73,5 | 1,0 - 2,6 | |
| Pimenta-longa | Piper aduncum | Óleo volátil/oleoresina | 30 - 40 | 100 - 300 | 1,4 - 1,8 | |
| Vetiver3 | Vetiveria zizanioides | Óleo volátil/ oleoresina | 40 | 200 | 3,2 |
Referências
1. BRAGA, M.E.M., EHLERT, P.A.D., MING, L.C., MEIRELES, M.A.A. Supercritical fluid extraction from Lippia alba: global yields, kinetic data, and extract chemical composition. Journal of Supercritical Fluids, v.34, p.149-156, 2005.
2. BRAGA, M.E.M., LEAL, P.F., CARVALHO, J.E., MEIRELES, M.A.A. Comparison of Yield, Composition, and Antioxidant Activity of Turmeric (Curcuma longa L.) Extracts Obtained Using Various Techniques. Journal of Agricultural and Food Chemistry, v.51, p.6604-6611, 2003.
3. BRAVI, M., BUBBICO, R., MANNA, F., VERDONE, N. Process optimization in sunflower oil extraction by supercritical CO2. Chemical Engineering Science, v.57, p.2753-2764, 2002.
4. BRUNNER, G., KIKIC, M., PERRUT, M. (org.) Proceedings of the 6th International Symposium on Supercritical Fluids, ISASF: Nancy, França, v. 1-3, 2124p., 2003
5. CANELA, A.P.R.F., ROSA, P.T.V., MARQUES, M.O.M., MEIRELES, M.A.A. Supercritical Fluid Extraction of Fatty Acids and Carotenoids from the Microalgae Spirulina maxima. Industrial & Engineering Chemistry Research, v.41, n.12, p.3012-3018, 2002.
6. CARVALHO JÚNIOR, R.N., MOURA, L.S., ROSA, P.T.V., MEIRELES, M.A.A. Supercritical Fluid Extraction from Rosemary (Rosmarinus officinallis): kinetic data, extract’s global yield, composition, and antioxidant activity. Journal of Supercritical Fluids, v.35, n.3, p.197-204, 2005.
7. FERREIRA, S.R.S., MEIRELES, M.A.A., CABRAL, F.A. Extraction of Essential Oil of Black Pepper with Liquid Carbon Dioxide. Journal of Food Engineering, v.20, p.121-133, 1993.
8. FERRUA, F.Q., MEIRELES, M.A.A. Cinética de Extração do Óleo Essencial de Capim-limão com Dióxido de Carbono Líquido. Ciência e Tecnologia de Alimentos, v. 14, n. Sup., p.93-100, 1994.
9. FRANÇA, L.F., MEIRELES, M.A.A. Modeling the Extraction of Carotene and Lipids from Pressed Palm Oil (Elaes guineensis) Fibers Using Supercritical CO2. Journal of Supercritical Fluids, v.18, p.35-47, 2000.
10. FREUND, R.J.; LITTELL, R.C. SAS System for Regression. SAS Series in Statistical Applications, 2a ed.; Cary: SAS Institute, p. 211, 1995.
11. FUKUZATO, R. Current Status of Supercritical Fluid Technology in the East Asia. In BRUNNER, G., KIKIC, M., PERRUT, M. (org.) Proceedings of the 6th International Symposium on Supercritical Fluids, ISASF: Nancy, França, p.1-10, 2003.
12. LEAL, P.F., SATO, D.N, CHAVES, F.C., MING, L.C., MARQUES, M.O.M., MEIRELES, M.A.A. Antioxidant an Antimycobacterial activities of Basil (Ocimum gratissimum) extracts obtained by SFE. In BRUNNER, KIKIC, M., PERRUT, M. (org.) Proceedings of the 6th International Symposium on Supercritical Fluids, ISASF: Nancy, França, p.183-188, 2003.
13. LEAL, P.F. Obtenção de extratos vegetais com propriedades funcionais usando tecnologia supercrítica: uso de CO2 e CO2 + H2O. Campinas, 163p. Tese (Mestrado) - Faculdade de Engenharia de Alimentos, Universidade Estadual de Campinas, 2005.
14. McHUGH, M., KRUKONIS, V. Supercritical Fluid Extraction: principles and practice. Stoneham: Butterworth Publishers, 1986.
15. MARTÍNEZ, J., MONTEIRO, A.R., MARQUES, M.O.M, MEIRELES, M.A.A Multicomponent Model To Describe Extraction of Ginger Oleoresin with Supercritical Carbon Dioxide. Industrial & Engineering Chemistry Research, v.42, p.1057-1063, 2003a.
16. MARTÍNEZ, J., ROSA, P.T.V., MING, L.C., MARQUES, M.O.M., MEIRELES, M.A.A. Extraction of Volatile Oil from Piper aduncum Leaves with Supercritical Carbon Dioxide. In BRUNNER, G., KIKIC, M., PERRUT, M. (org.) Proceedings of the 6th International Symposium on Supercritical Fluids, ISASF: Nancy, França, p.65-70, 2003b.
17. MARTÍNEZ, J., ROSA, P.T.V., MENUT, C., LEYDET, A., PALLET, D., MEIRELES, M.A.A. Valorization of Brazilian Vetiver (Vetiveria zizanioides (L.) Nash ex Small) Oil. Journal of Agricultural and Food Chemistry, v.52, p.6578-6584, 2004.
18. MEIRELES, M.A.A. Supercritical Extraction from Solid: process design data (2001-2003). Current Opinion in Solid State and Material Science, v.7, n.4, p.321-330, 2003.
19. MONTEIRO, A.R., MEIRELES, M.A.A., MARQUES, M.O.M., PETENATE, A.J. Extraction of the Soluble Material from the Shells of the Bacuri Fruit (Platonia insignis Mart) with Pressurized CO2 and Other Solvents. Journal of Supercritical Fluids, v.11, n.1/2, p.91-102, 1997.
20. MORESCHI, S.R.M., PETENATE, A.J., MEIRELES, M.A.A. Hydrolysis of Ginger Bagasse Starch in Subcritical Water and Carbon Dioxide. Journal of Agricultural and Food Chemistry, v.52, n. 6, p.1753-1758, 2004.
21. MOURA, L.S., CARVALHO JÚNIOR, R.N., STEFANINI, M.B., MING, L.C., MEIRELES, M.A.A. Supercritical fluid extraction from fennel (Foeniculum vulgare): global yield, composition and kinetic data. Journal of Supercritical Fluids, v.35, n.3, p.212-219, 2005.
22. MÜLLER, C.M.O., MONTEIRO, A.R., RODRIGUES, V.M., VASCONCELLOS, V.R., MEIRELES, M.A.A., MARQUES, M.O.M. Supercritical Extraction of Essential Oils of Cymbopogon martini, Cymbopogon winterianus, and Eucalyptus citriodora with Carbon Dioxide. CPS The Chemistry Preprint Server, 2001. http://www.sciencedirect.com/preprintarchive.
23. PASQUEL, A., MEIRELES, M.A.A., MARQUES, M.O.M., PETENATE, A.J. Extraction of Stevia Glycosides with CO2 + Water, CO2 + Ethanol, and CO2 + Water + Ethanol. Brazilian Journal of Chemical Engineering, v.17, n. 3, p.271-282, 2000.
24. PEREIRA, C.G; MARQUES, M.O.M, SIANI, A.C., MEIRELES, M.A.A. Supercritical extraction of indole alkaloids from Tabernaemontana catharinensis: an evaluation of the cosolvent on the extract compositions. In BRUNNER, KIKIC, M., PERRUT, M. (org.) Proceedings of the 6th International Symposium on Supercritical Fluids, ISASF: Nancy, França, p.47-52, 2003.
25. PEREIRA, C.G., MARQUES, M.O.M., BARRETO, A.S., SIANI, A.C., FERNANDES, E.C., MEIRELES, M.A. Extraction of indole alkaloids from Tabernaemontana catharinensis using supercritical CO2 + ethanol: an evaluation of the process variables and the raw material origin. Journal of Supercritical Fluids, v.30, p.51-61, 2004.
26. PEREIRA, C.G. Obtenção de extratos de leiteira de dois irmãos (Tabernaemontana catharinensis A. DC.), cidrão (Aloysia triphylla L’Herit. Britton) e manga (Mangifera indica L.) por extração supercrítica: estudo dos parâmetros de processo, caracterização e atividade antioxidante dos extratos. Campinas, 225p. Tese (Doutorado) - Faculdade de Engenharia de Alimentos, Universidade Estadual de Campinas, 2005.
27. PERRUT, M. Supercritical Fluid Applications: Industrial Developments and Economic Issues. Industrial & Engineering Chemistry Research v.39, p.4531-4535, 2000.
28. PORTILLO, R. Extração do Óleo Essencial de Khoa (Satureja boliviana Benth Briq) por Diferentes Processos: Destilação por Arraste a Vapor, Solventes Orgânicos e Dióxido de Carbono Pressurizado. Campinas, 192p. Tese (Doutorado) - Faculdade de Engenharia de Alimentos, Universidade Estadual de Campinas, 1999.
29. POVH, N.P., MARQUES, M.O.M., MEIRELES, M.A.A. Supercritical CO2 Extraction of Essential Oil and Oleoresin from Chamomile (Chamomilla recutita [L.] Rauschert). Journal of Supercritical Fluids, v.21, p.245-256, 2001.
30. QUISPE-CONDORI, S. Determinação de parâmetros de processo nas diferentes etapas do processo de extração supercrítica de produtos naturais: Artemisia annua, Cordia verbenacea, Ocimum selloi e Foeniculum vulgare. Campinas, 239p. Tese (Doutorado) - Faculdade de Engenharia de Alimentos, Universidade Estadual de Campinas, 2005.
31. QUISPE-CONDORI, S., SANCHEZ, D., FOGLIO, M.A., ROSA, P.T.V., ZETZL, C., BRUNNER, G., MEIRELES, M.A.A. Global yield isotherms and kinetic of artemisinin extraction from Artemisia annua L leaves using supercritical carbon dioxide. Journal of Supercritical Fluids, v.36, p.40-48, 2005.
32. RODRIGUES, V.M. Determinação da Solubilidade em Sistemas Pseudo-Ternários: Cravo-da-Índia (Eugenia caryophyllus) + CO2, Gengibre (Zingiber officinale) + CO2 e Erva Doce (Pimpinella anisum) + CO2. Campinas, 320p. Tese (Doutorado) - Faculdade de Engenharia de Alimentos, Universidade Estadual de Campinas, 2001.
33. RODRIGUES, V.M., ROSA, P.T.V., MARQUES, M.O.M., PETENATE, A.J., MEIRELES, M.A.A. Supercritical Extraction of Essential Oil from Aniseed (Pimpinella anisum L.) Using CO2: Solubility, kinetics, and Composition Data. Journal of Agricultural and Food Chemistry, v.51, p.1518-1523, 2003.
34. RODRIGUES, V.M., SOUSA, E.M.B.D., MONTEIRO, A.R., CHIAVONE FILHO, O., MARQUES, M.O.M., MEIRELES, M.A.A. Determination of the Solubility of Extracts from Vegetable Raw Material in Pressurized CO2: A Pseudo-Ternary Mixture Formed by Cellulosic Structure + Solute + Solvent. Journal of Supercritical Fluids, v.22, p.21-36, 2002.
35. ROSA, P.T.V., MEIRELES, M.A.A. Rapid estimation of manufacturing cost of extracts obtained by supercritical fluid extraction. Journal of Food Engineering, v.67, p.235-240, 2005a.
36. ROSA, P.T.V., MEIRELES, M.A.A. Supercritical technology in Brazil: system investigated (1994 - 2003). Journal of Supercritical Fluids, v.34, p.109-117, 2005b.
37. SOUSA, E.M.B.D., CHIAVONE FILHO, O., MORENO, M.T.S., SILVA, D.N., MARQUES, M.O.M., MEIRELES, M.A.A. Experimental Results for the Extraction of Essential Oil from Lippia sidoides Cham. using Pressurized CO2. Brazilian Journal of Chemical Engineering, v.19, n.2, p.229-241, 2002.
38. SOUSA, E.M.B.D., MARTÍNEZ, J., CHIAVONE FILHO, O., ROSA, P.T.V., DOMINGOS, T., MEIRELES, M.A.A. Extraction of volatile oil from Croton zehntneri Pax et Hoff with pressurised CO2: solubility, composition and kinetics. Journal of Food Engineering, v.69, p.325-333, 2005.
39. UHDE (Alemanha; http://www.uhde-co2.com/index.html). Comunicação pessoal, 2001.
40. ZANCAN, K.C., MARQUES, M.O.M., PETENATE, A.J., MEIRELES, M.A.A. Extraction of ginger (Zingiber officinale Roscoe) oleoresin with CO2 and co-solvents: a study of the antioxidant action of the extracts. Journal of Supercritical Fluids, v.24, p.57-76, 2002.