Artigo original
Utilização do Monitoramento Seletivo de Íons como Ferramenta para a Detecção de Adulterações em Óleos de Copaíba
Selective Ion Monitoring as a Tool for Detecting Adulterated Copaiba Oil
Resumo
Através da cromatografia gasosa de alta resolução acoplada à espectrometria de massas foi utilizado o monitoramento seletivo e simultâneo de íons para a detecção de marcadores biológicos e de adulterantes em óleos de copaíba (Copaifera sp.) comerciais adquiridos na cidade do Rio de Janeiro. Adulterações com óleos vegetais e minerais foram detectadas através de fragmentos específicos de hidrocarbonetos e ésteres metílicos de ácidos graxos lineares saturados e insaturados. Além disso, a técnica foi utilizada para a detecção do marcador dos óleos de copaíba, o ácido copálico, e de co-eluições deste com outros diterpenos também encontrados nos óleos de copaíba.
- Unitermos:
- CG-EM.
- Monitoramento seletivo de íons.
- adulterações em óleos de copaíba.
- óleo de copaíba.
- Copaifera.
Abstract
Using high-resolution gas chromatography coupled with mass spectrometry, the simultaneous and selective ion monitoring was used to detect biomarkers and adulterations at commercial copaiba oils acquired at the Rio de Janeiro city. Adulterations with vegetal and mineral oils were detected by analyzing specific fragments originated from the hydrocarbons and saturated and unsaturated fatty acids methyl esters present in the copaiba oils. Copalic acid, a biomarker in copaiba oil, was also detected by the same technique as well as by co-elutions with other diterpenes present in copaíba oils.
- Key words:
- HRGC-MS.
- Selective Ion Monitoring.
- Adulterations at copaiba oil.
- Copaifera.
Introdução
A cromatografia a gás acoplada à espectrometria de massas (CG-EM) é uma das técnicas mais poderosas de que se dispõe para a análise de misturas complexas voláteis de baixo e médio pesos moleculares. Devido a sua rapidez e grande reprodutibilidade, a CG-EM está cada vez mais presente nas análises de rotina nos laboratórios de química de produtos naturais e no setor de controle de qualidade dos laboratórios farmacêuticos (SIQUEIRA et al., 2003).
Os equipamentos de CG-EM podem ser calibrados para detectar um único íon (Monitoramento Seletivo de Íon) ou para monitorar simultaneamente vários íons (Monitoramento Simultâneo de Íons), com extrema rapidez e sensibilidade. Ao invés de se varrer uma faixa de massas moleculares para se obter um perfil dos fragmentos formados devido às quebras de ligações das moléculas, no chamado cromatograma de íons totais (CIT), o monitoramento seletivo ou simultâneo de íons permite, como o próprio nome já indica, a seleção de um ou mais fragmentos que caracterizam famílias de moléculas. A observação de um determinado fragmento, pertencente a uma molécula que funcione como um marcador da amostra, pode servir para autenticar esta amostra. Por outro lado, um fragmento proveniente de uma molécula que não deveria estar presente na amostra pode indicar a adulteração desta amostra.
A utilização do monitoramento seletivo ou simultâneo de íons (MSI) é um método poderoso para detectar adulterações ou para a certificação de fitoterápicos. Neste artigo, apresentaremos o uso desta ferramenta na detecção de adulterações de óleos de copaíba, adquiridos em farmácias do Rio de Janeiro.
Materiais e Métodos
Os óleos de copaíba analisados foram comprados em farmácias de produtos naturais do município do Rio de Janeiro, entre 2001 e 2002.
Os óleos de copaíba foram previamente metilados com diazometano antes de serem cromatografados. Os constituintes químicos destes óleos foram identificados através da interpretação dos seus espectros de massas, por comparação dos seus espectros com os armazenados na Espectroteca Wiley e com dados de padrões.
As análises cromatográficas foram realizadas em cromatógrafo a gás (Hewlett Packard - modelo 5890), coluna SE-54 com 20 m de comprimento, 0,25 mm de diâmetro interno e 0,25 μm de espessura de fase; nas seguintes condições: gás de arraste Hidrogênio, com vazão de 2 ml/min e divisão de fluxo (split 1:20). A temperatura inicial foi ajustada em 120 oC, com taxa de aquecimento de 2 oC/min até 160 oC, a partir desta temperatura a taxa de aquecimento foi selecionada em 8 oC /min até 290 oC. A temperatura final foi mantida constante durante 5 minutos.
As análises por CG-EM (equipamento Hewlett Packard - modelo 6890 MSD) foram realizadas utilizando a mesma programação de elevação da temperatura do forno, coluna semelhante à primeira, DB5 com 20 m de comprimento, 0,25 mm de diâmetro, 0,25 μm de espessura de fase; e gás de arraste Hélio, com vazão de 1,6 ml/min, sem divisão de fluxo (Splitless).
Resultados e Discussão
Os chamados óleos de copaíba são óleo-resinas naturais, exudados através de furo feito com trado no tronco das copaíbas, a mais ou menos 1 metro de altura da árvore (VEIGA JR.; PATITUCCI; PINTO, 1997). Esses óleos são constituídos por misturas de sesquiterpenos e de diterpenos. Os sesquiterpenos dissolvem as substâncias mais pesadas, os chamados ácidos resinosos (diterpenos) (VEIGA JR. et al, 1995; TAPPIN et al, 2004). A viscosidade do óleo será maior quanto maior for o seu conteúdo de diterpenos. Obtido das árvores do gênero Copaifera localizadas em todo o Brasil, principalmente na Amazônia, este óleo possui variadas aplicações medicinais (VEIGA JR.; PINTO, 2002). Diversos estudos, realizados recentemente, comprovam algumas das atividades farmacológicas descritas pelos primeiros cronistas, que chegaram ao Brasil com base na sua utilização pelos índios, e o seu uso, nos dias atuais, como antiinflamatório (BASILE et al, 1988; FERNANDES; PEREIRA; PAULO, 1992; VEIGA JR. et al, 2001) e anti-tumoral (LIMA et al, 2003).
O comércio deste óleo é uma atividade econômica importante tanto para as pequenas comunidades da Amazônia, que têm sua auto-sustentabilidade baseada no extrativismo, quanto para as empresas de grandes centros, como Manaus e Belém, que o exportam para a Europa e Estados Unidos, onde é utilizado nas indústrias de perfumes e cosméticos em geral (VEIGA JR.; PINTO, 2002).
O fato do óleo de copaíba só poder ser coletado em épocas específicas do ano e das árvores estarem escassamente distribuídas por regiões amplas nas matas, cerca de 1 árvore em cada 10 hectares, faz com que este seja comumente misturado a outros óleos para aumentar seu volume e garantir o suprimento do mercado durante todo o ano (VEIGA JR. et al, 1997; VEIGA JR.; PINTO, 2002).
Por apresentar um aroma muito característico, com forte odor de madeira, a falsificação do óleo de copaíba é bastante incomum. Já as adulterações, realizadas através de diluições dos óleos de copaíba com outros óleos, de origem vegetal ou mineral, de menor valor agregado, são bastante comuns, tendo sido descritas na literatura a partir do início do século passado (FREISE, 1937). Entre os óleos vegetais, destacam-se os óleos de outras leguminosas e os óleos comestíveis, como os óleos de soja e milho. Entre os óleos minerais utilizados como adulterantes destacam-se o nujol® e o óleo diesel.
A maior parte das metodologias já propostas para a detecção de adulterações nos óleos de copaíba utiliza características físicas como a densidade, cor e aroma. Entretanto, no caso do adulterante ser o óleo de soja ou um óleo mineral, a detecção através destes métodos será mais difícil, particularmente pela grande variação na relação entre sesquiterpenos e diterpenos nos óleos de copaíba, que altera sobremaneira a sua densidade e a sua viscosidade.
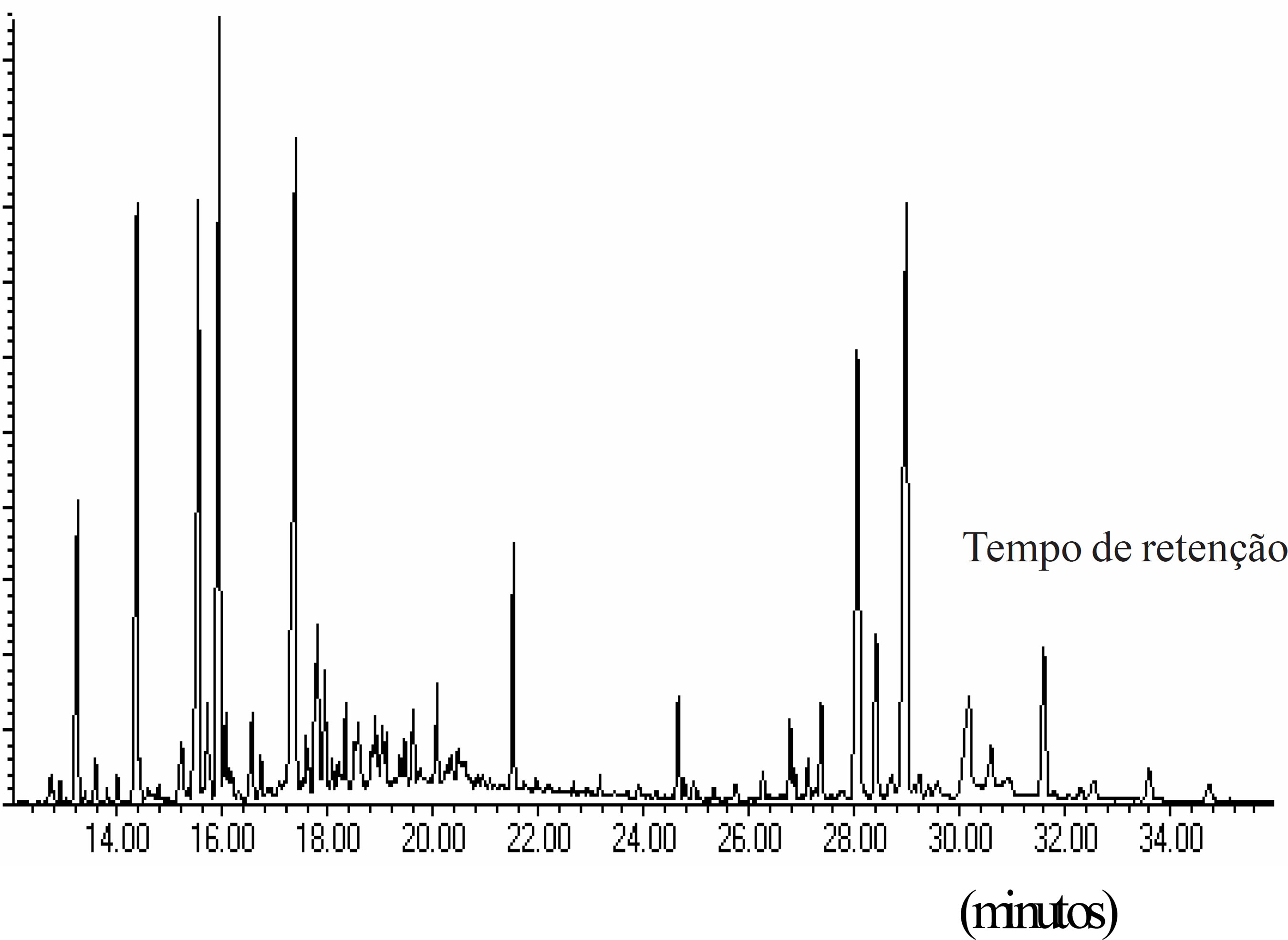
Uma vez que os óleos de copaíba possuem somente sesquiterpenos e diterpenos em sua composição, a detecção de agentes adulterantes pode ser percebida utilizando-se fragmentos característicos destas substâncias. A Figura 1 ilustra um cromatograma de íons totais de um óleo de copaíba puro, contendo duas regiões de eluição, de sesquiterpenos (a primeira, até 20 minutos) e a de diterpenos (a região mais à direita, após 20 minutos).
A detecção, através de monitoramento simultâneo de íons (MSI), de fragmentos que caracterizam hidrocarbonetos lineares, como m/z 57 e m/z 71, pode ser utilizada para a detecção da presença de um óleo mineral. Na Figura 2A, o CIT de um óleo de copaíba contendo óleo mineral como adulterante é apresentado. A principal característica observada neste cromatograma é a ausência ou diminuição na altura dos picos da região de sesquiterpenos.
Através do monitoramento simultâneo dos íons de m/z 57 e m/z 71 pode se observar no cromatograma resultante (Figura 2B) os hidrocarbonetos presentes no óleo adulterado, característicos de óleos minerais.
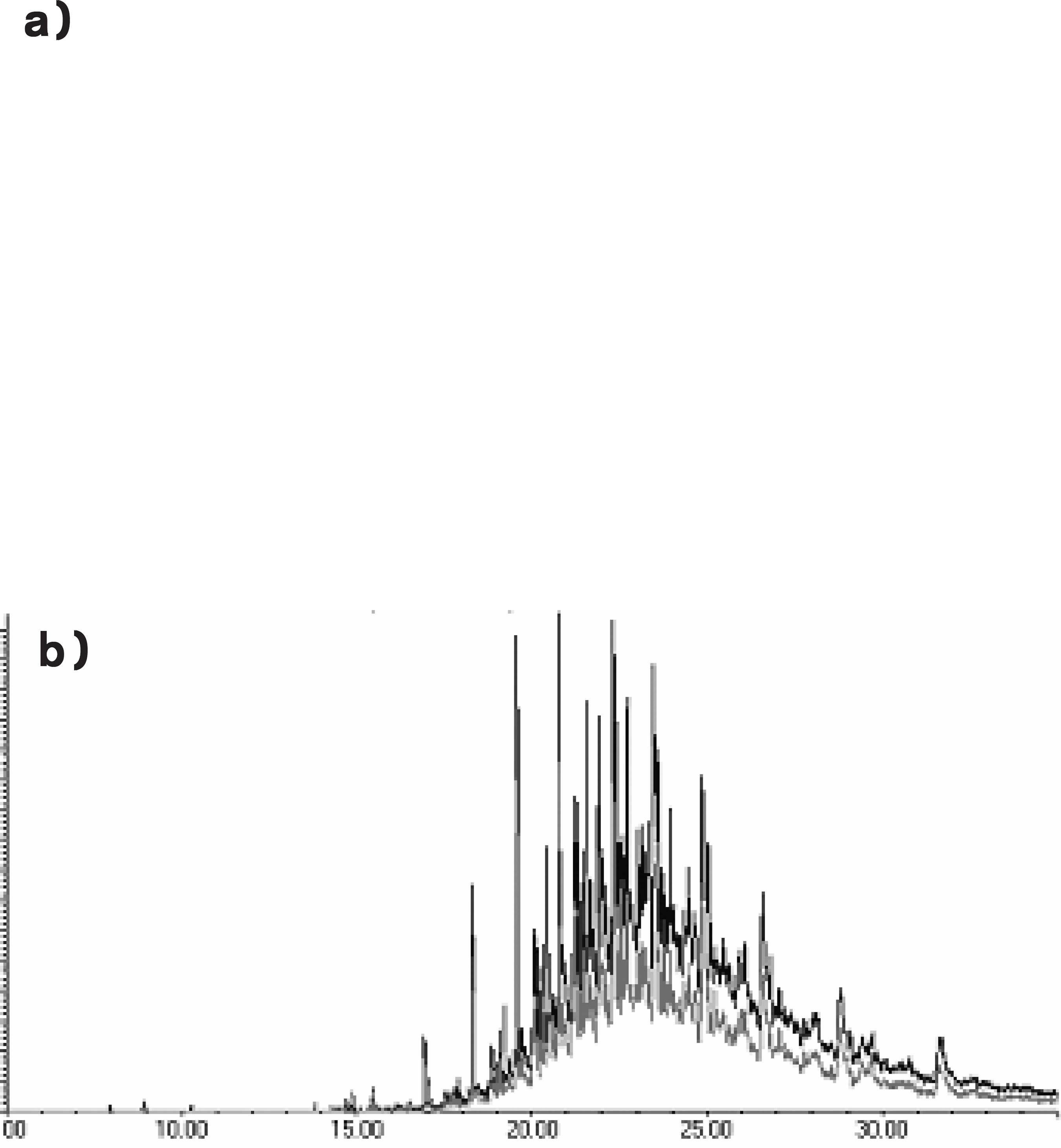
A presença destes íons com grande abundância e em vários picos indica a presença de uma mistura de hidrocarbonetos lineares. Como esta composição não é característica dos óleos de copaíba, sua presença é uma evidência inequívoca de sua adulteração.
No CIT do óleo de copaíba comercial apresentado na Figura 2 observou-se a elevação da linha base, sugerindo a superposição de picos característica de misturas muito complexas. O fragmentograma dos íons m/z 57 e m/z 71 permite a caracterização desta mistura como sendo proveniente de uma mistura de hidrocarbonetos.
Através de uma extração ácido-base deste óleo de copaíba comercial foram obtidas duas frações, uma ácida e outra neutra. Na fração ácida, somente os ácidos diterpênicos foram observados. A fração neutra, entretanto, apresentou perfil semelhante à do MSI da Figura 2B e, ainda, picos na região anterior do cromatograma, relativos aos sesquiterpenos presentes originalmente no óleo, confirmando, desta forma, a adulteração e os achados obtidos através do MSI.
Quando a adulteração é realizada com um óleo vegetal, pequenas quantidades de ácidos graxos livres estarão presentes na amostra. Além de uma menor área total dos picos, resultante da diluição com os triglicerídeos, a área de eluição dos sesquiterpenos apresentará menor número de picos, enquanto a de diterpenos apresentará os picos dos ácidos graxos, identificados como seus respectivos ésteres metílicos, uma vez que as amostras devem ser esterificadas antes da análise por CG-EM (VEIGA JR. et al, 1997). Para a detecção de ésteres metílicos de ácidos graxos saturados, como o palmitato e o estearato de metila, foram utilizados os íons de m/ z 74 e de m/z 87. Para a detecção de ésteres graxos insaturados, o íon de m/z 55 é bastante adequado, com um íon adicional de m/z 69, para os mono-insaturados, como o oleato de metila, e de m/z 67 para os di-insaturados, como o linoleato de metila.
No caso dos ésteres metílicos graxos saturados, o íon de m/z 74, relativo ao rearranjo de Mc-Lafferty, é bastante específico. Já para os ésteres metílicos graxos insaturados o íon de m/z 55 é bastante comum, mas a presença de mais de uma insaturação torna o restante do espectro pouco característico desta classe de substância, devendo sua estrutura ser confirmada por um conjunto maior de fragmentos.
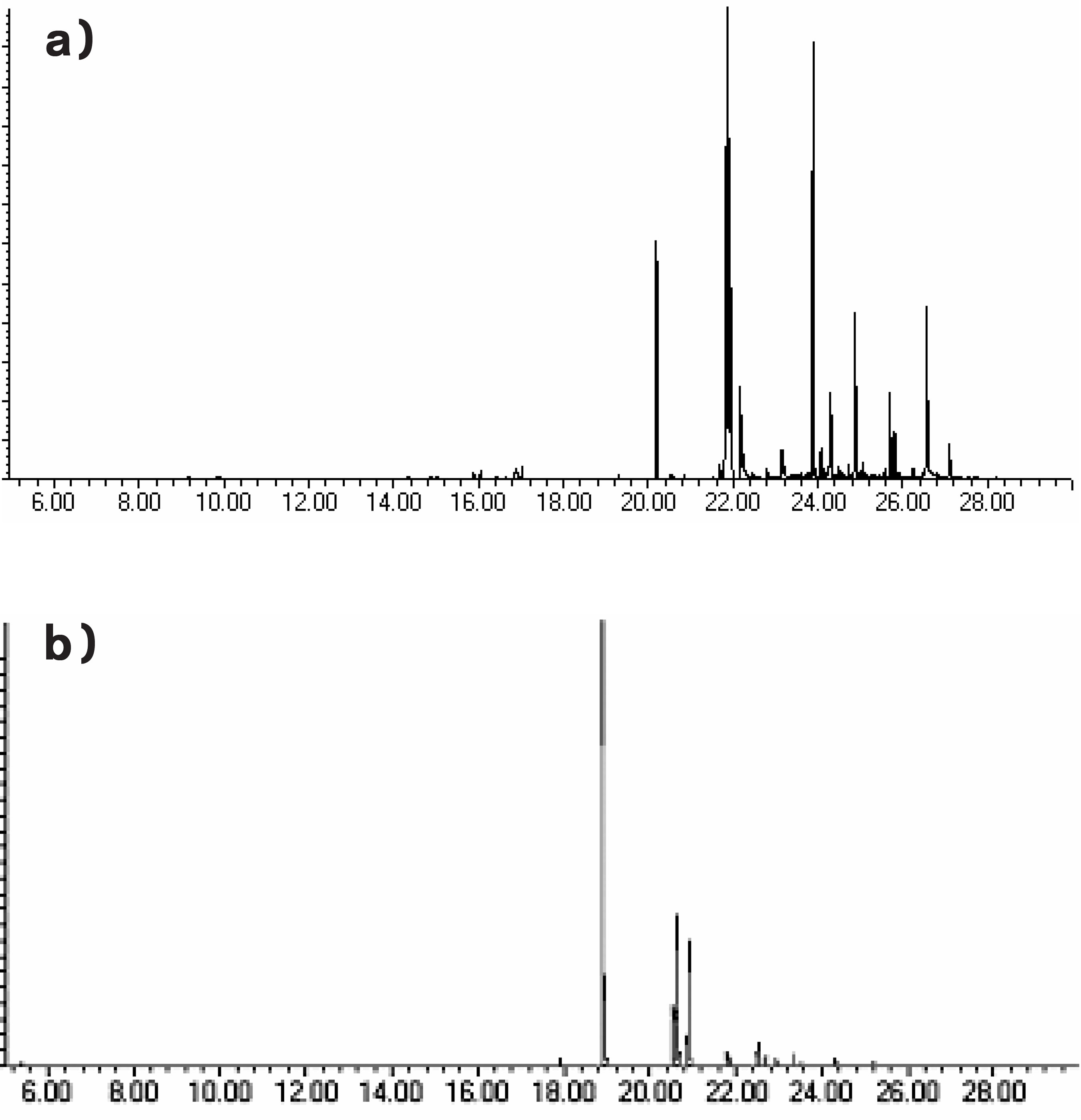
A Figura 3 ilustra um caso de diluição por adição de óleo vegetal onde são percebidos, através do MSI, picos específicos de ésteres graxos metílicos saturados. A Figura 3A apresenta o CIT do óleo comercial analisado, enquanto a Figura 3B ilustra o monitoramento simultâneo dos íons de m/z 74 e de m/z 87.
O MSI também pode ser utilizado quando se deseja localizar rapidamente um pico de interesse em uma matriz complexa (como são, por exemplo, os óleos de copaíba). Neste caso, utiliza-se um fragmento que seja bastante específico para a molécula de interesse, geralmente proveniente de rearranjo, e pesquisa-se a região do cromatograma onde se espera a eluição desta substância.
Algumas vezes uma substância especifica desperta o interesse em um extrato, como um marcador biológico ou um constituinte que apresenta atividade biológica. Caso haja necessidade de quantificá-la através de cromatografia em fase gasosa, o pico correspondente da substância não deve estar co-eluindo com nenhuma outra substância do extrato. Neste caso, a utilização do MSI será particularmente útil para se verificar se há sobreposição de picos. No caso dos óleos de copaíba, o copalato de metila é um dos principais marcadores, por estar presente em todos os óleos analisados em amplo estudo recente (VEIGA JR., 2004). Na Figura 1, pode-se visualizar o pico do copalato de metila como o principal constituinte da amostra, eluindo em 28,00 minutos. Na Figura 4, a região entre 27,50 e 28,50 está expandida (4a), para que se observe mais claramente o pico do copalato de metila. Somente quando se utiliza o monitoramento seletivo dos íons de m/z 114, bastante específico para o copalato de metila, e de m/z 257, característico de outro diterpeno (caurenoato de metila), observa-se que, na verdade, o pico principal não contém somente o copalato de metila, mas uma mistura dos dois diterpenos (Figura 4B).
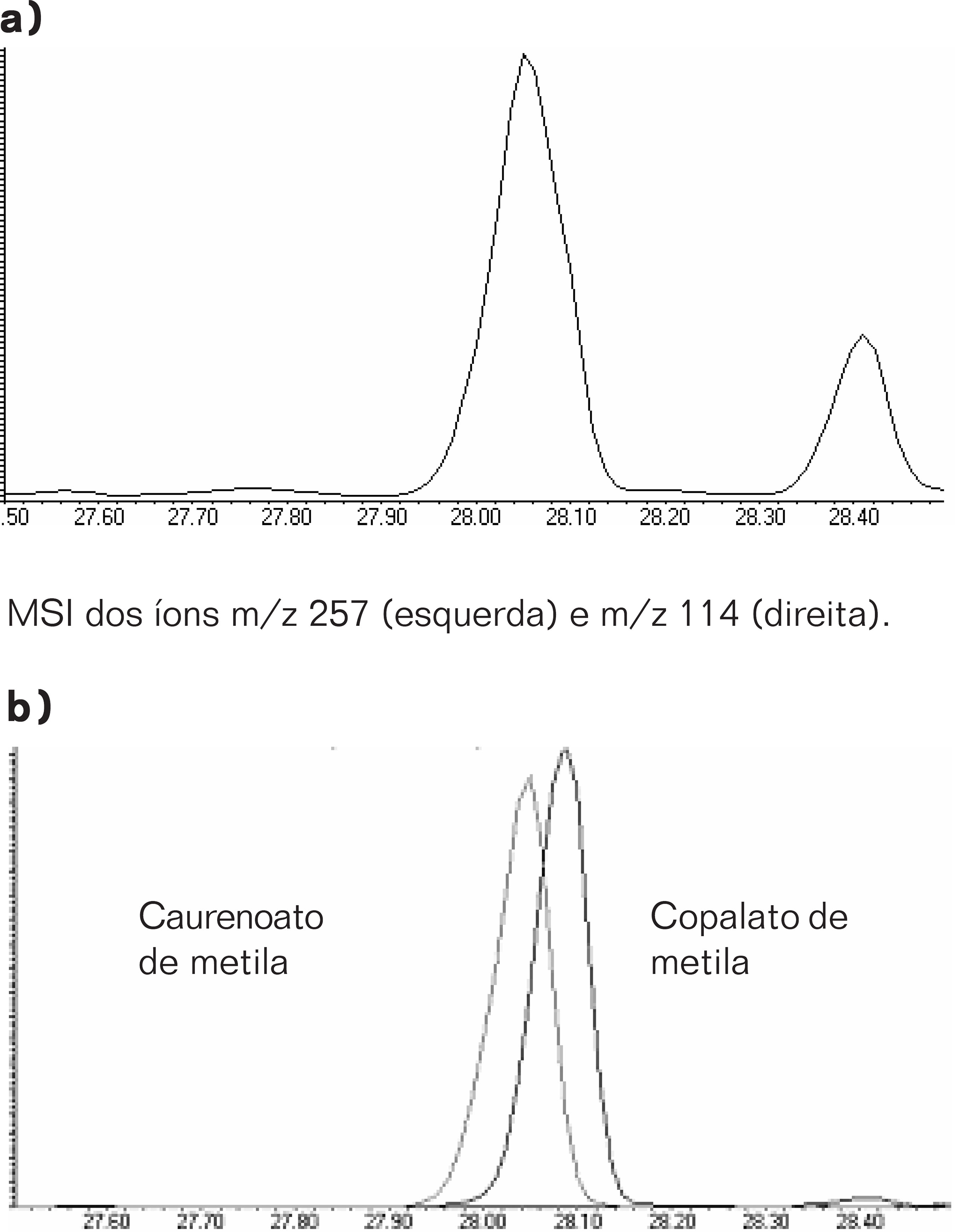
Os íons monitorados no exemplo anterior (Figura 4), de m/z 114 e de m/z 257, são originados das reações de fragmentação ilustradas na Figura 5, a seguir, onde se observam também as estruturas das moléculas dos respectivos ésteres metílicos dos dois ácidos diterpênicos.
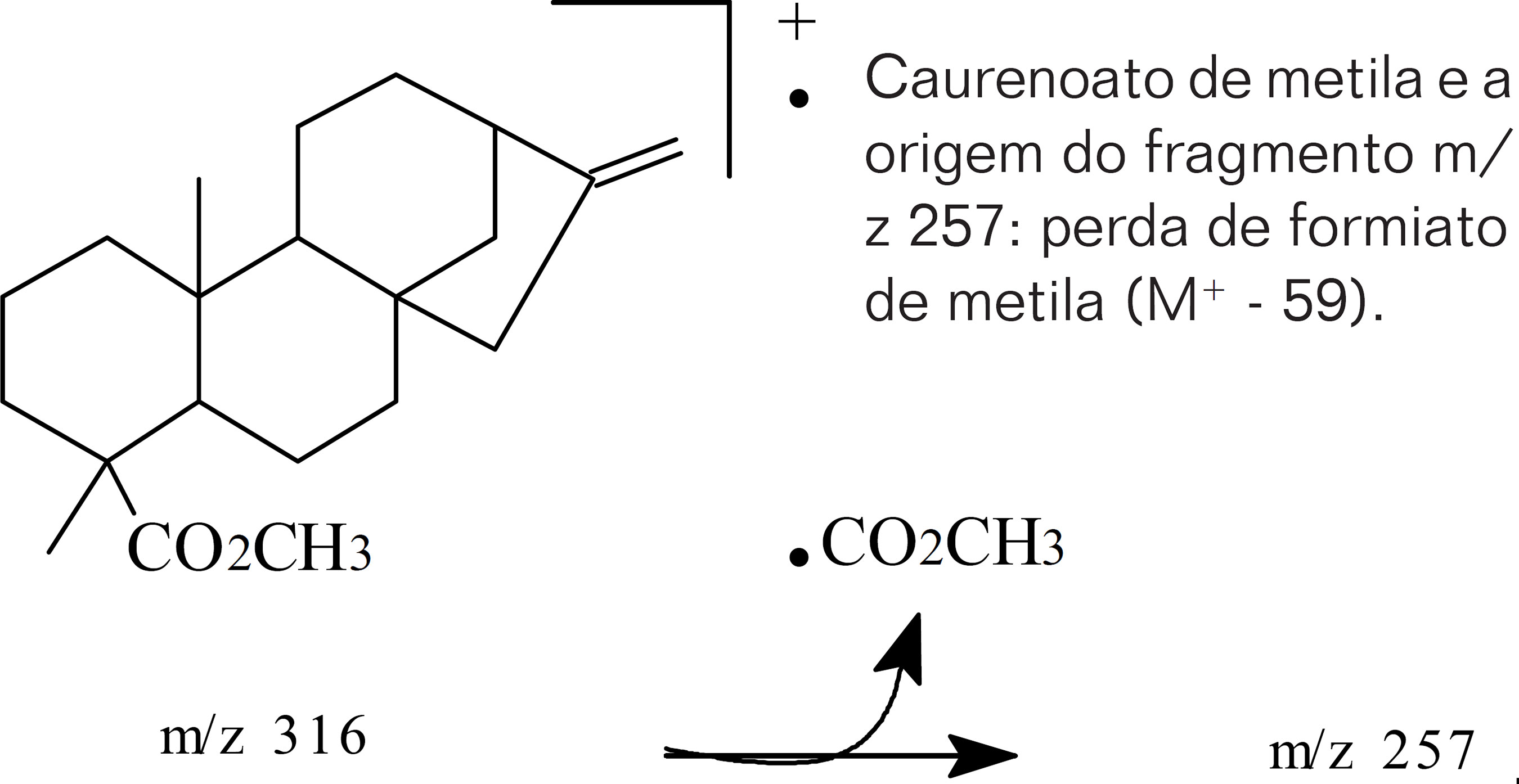
Observa-se, portanto, uma grande utilidade desta metodologia para uma rápida detecção de moléculaschave em óleos de copaíba, sendo elas adulterantes ou marcadoras biológicas da própria espécie ou gênero.
Agradecimentos:
Os autores agradecem ao CNPq, FAPERJ, FUJB e CAPES.
Referências
BASILE, A.C.; SERTIÉ, J.A.; FREITAS, P.C.D.; ZANINI, A.C. Anti-inflammatory activity of oleoresin from Brazilian Copaifera. Journal of Ethnopharmacology, v.22, p.101-109, 1988.
FERNANDES, R.M.; PEREIRA, N.A.; PAULO, L.G. Antiinflammatory activity of copaiba balsam. Revista Brasileira de Farmácia, v.73, p.53-56, 1992.
FREISE, F.W. Einige Klarstellungen hinsichtlich des brasilianischen Copaivabalsams. Süddeutsche Apotheker-Zeitung v.77, p.11-14, 1937.
LIMA, S.R.M.; VEIGA JR, V.F., CHRISTO, H.B., PINTO, A.C., FERNANDES, P.D. In vivo and in vitro studies on the anticancer activity of Copaifera multijuga Hayne. Phytotherapy Research, v.17, p.1048-1053, 2003.
SIQUEIRA, D.S.; PEREIRA, A.S.; AQUINO-NETO, F.R.; CABRAL, J.A.; FERREIRA, C.A.C.; SIMONEIT, B.R.T.; ELIAS, V.O. Determinação de Compostos de Massa Molecular Alta em Folhas de Plantas da Amazônia. Quimica Nova, v.26, p.633-640, 2003.
TAPPIN, M.R.R.; PEREIRA, J.F.G.; LIMA, L.A.; SIANI, A.C.; MAZZEI, J.L.; RAMOS, M.F.S. Análise Química Quantitativa para a Padronização do Óleo de Copaíba por Cromatografia em Fase Gasosa de Alta Resolução. Quimica Nova v.27, p.236-240, 2004.
VEIGA JR, V.F.; PATITUCCI, M.L.; ROCHA, J.; ZOGHBI, M.G.B.; PINTO, A.C. Detecção de Classes de Terpenos: Utilização Alternativa de Cromatografia Gasosa de Alta Resolução. Quimica Nova v.18, p.262-266, 1995.
VEIGA JR., V.F.; PATITUCCI, M.L.; PINTO, A.C. Controle de Adulteração de Óleos de Copaíba por Cromatografia Gasosa de Alta Resolução. Quimica Nova, v.20, p.612-615, 1997.
VEIGA JR, V.F.; ZUNINO, L.; CALIXTO, J.B.; PATITUCCI, M.L.; PINTO, A.C. Phytochemical and Anti-Oedematogenic Studies of Commercial Copaiba Oils Available in Brazil. Phytotherapy Research, v.15, p.476-480, 2001.
VEIGA JR., V.F.; PINTO, A.C. O Gênero Copaifera. Quimica Nova, v.25, p.273-286, 2002.
VEIGA JR., V.F. O gênero Copaifera: Estudos fitoquímicos de 8 espécies classificadas e de 127 óleos de copaíba. Rio de Janeiro, 400p. Tese (Doutorado) - Instituto de Química, Universidade Federal do Rio de Janeiro, 2004.