Artigo original
A cromatografia líquida a vácuo na análise qualitativa e quantitativa de flavonóides em Achyrocline satureioides
Vacuum Liquid Chromatography in the Qualitative and Quantitative Flavonoid Analyses in Achyrocline satureioides
Resumo
O isolamento de substâncias a partir de drogas vegetais é realizado com freqüência empregando-se métodos cromatográficos, sendo a cromatografia em coluna a mais utilizada. Uma variante da cromatografia em coluna é a cromatografia líquida a vácuo, por ser uma técnica eficiente e de baixo custo, podendo ser empregada com fins analíticos qualitativos ou mesmo quantitativos. Através de extratos semipurificados, e com auxílio da cromatografia líquida a vácuo, isolou-se 3-O-metilquercetina de Achyrocline satureioides (Lam.) DC., Asteraceae, obtendose um teor de 1,21%.
- Unitermos:
- Achyrocline satureioides.
- Asteraceae.
- 3-O-metilquercetina.
- Cromatografia líquida a vácuo.
Abstract
The isolation of pharmacologically active compounds from vegetable sources is usually done by chromatographic methods, and the column chromatography is frequently employed. A variant of this methodology includes the vacuum liquid chromatography that could be used for qualitative or even quantitative analytic works, given that it presents high efficiency and low cost. The present study reports the isolation of 3-O-methylquercetin (1,21% yield) from semi-purified extracts of Achyrocline satureioides (Asteraceae) using the technique of vacuum liquid chromatography.
- Key words:
- Achyrocline satureioides.
- Asteraceae.
- Vaccum Liquid Chromatography.
- 3-O- methylquercetin.
Intodução
Entre os métodos modernos de análise, a cromatografia possui papel relevante devido à capacidade de: separação, identificação, além de auxiliar na quantificação de substâncias. Por si só ou associada a outras técnicas instrumentais de análise, como a espectrofotometria, espectrometria de massas e mais recentemente com a cromatografia líquida associada à ressonância magnética nuclear de prótons ou mesmo Carbono-13 (HOSTETTMANN et al., 2003), tem ampliado o seu emprego como método principal de análise.
A cromatografia líquida de alta eficiência (CLAE) possui vantagens inerentes ao método como: rapidez, eficiência e sensibilidade (SZEPESI, 1990), porém o custo do equipamento pode inviabilizar trabalhos de controle de qualidade rotineiros nas indústrias em geral.
Assim, a cromatografia líquida a vácuo (CLV) foi proposta inicialmente por Targett et al. (1979), como método alternativo com finalidade de separação de pequenas e grandes quantidades de misturas de substâncias. Os autores demonstraram que o sistema era eficiente e que não havia perdas na separação, sendo empregada com fins analíticos, qualitativos e quantitativos, mesmo com misturas de substâncias. Mello e Petrovick (2000) empregaram a CLV na separação de polifenóis a partir de extratos hidroetanólicos de carqueja [Baccharis trimera (Less.) DC.], como método auxiliar ao controle de qualidade.
Como modelo experimental inicial para o método de análise qualitativa e quantitativa empregando a CLV, utilizou-se extrato semipurificado de marcela [Achyrocline satureioides (Lam.) DC.] na análise de substâncias flavonoídicas.
Material e Métodos
Geral: Foi empregado espectrômetro Varian modelo Gemini 2000BB, 300 MHz para obtenção de espectros de RMN 1-D (1H, 13C) e 2-D (1H/1H-COSY). Os solventes deuterados foram Isotec®. Os espectros de massas ESI/MS/MS foram obtidos em um espectrômetro de massa triplo quádruplo Quattro II. A cromatografia em camada delgada (CCD) foi realizada com folhas de alumínio (gel de sílica 60 F254, 0,20 mm, Merck) com fase móvel: acetato de etila:tolueno:ácido fórmico:água (50:50:10:5; V/V); detecção: luz ultravioleta a 254 nm e vapores de hidróxido de amônio e 3-O-metil-quercetina e quercetina (Merck) como substâncias de referência. A cromatografia em camada delgada preparativa (CCDP) foi realizada em placas de 20 x 20 cm com 0,75 mm de espessura, com gel de sílica PF254 (Merck) no mesmo sistema eluente anterior.
Droga vegetal: A espécie Achyrocline satureioides (droga vegetal) foi coletada no município de Mandaguari, PR, Brasil, em 16/04/00, identificada pela Profa. Dra. Cássia Mônica Sakuragui e, um exemplar encontra-se depositado no herbário da Universidade Estadual de Maringá sob número HUM 5270.
Extração e isolamento: Com as inflorescências secas (92,3 g) foi preparado extrato por turbólise (15 min) em álcool 70% na proporção de 1:10 (m/ V). Após, o extrato foi filtrado e o volume completado obtendo-se o extrato total (ET). O ET foi concentrado sob pressão reduzida e liofilizado (46,6 g), retomado em água (100 mL) e fracionado com acetato de etila (10 x 100 mL). A fase orgânica foi eliminada por pressão reduzida em evaporador rotatório e após, liofilizada. A fração acetato de etila liofilizada (12,32 g) foi tratada com clorofórmio, resultando nas frações liofilizadas: clorofórmica (FCL; 1,49 g), aquosa (FAQ; 1,26 g) e pastosa (FP; 7,35 g). A FAQ (1,26 g) foi cromatografada por cromatografia líquida a vácuo em gel de sílica com 10 mL em proporções volumétricas de n-hexano e n-butanol (9,0:1,0; 8,5:1,0 e 8,0:1,5). A FAQ-2 (tubos 4-12) apresentou duas fases, sendo que o sobrenadante foi recolhido, concentrado, fornecendo após CCDP, a substância 1 (5,3 mg; Rf = 0,50; pó amorfo amarelo 1). 1H-NMR (300 MHz: CD3OD, d): 3,78 (O-Me, s), 6,19 (H-6, d, J= 2,4 Hz), 6,38 (H-8, d, J= 2,4 Hz), 6,90 (H-5’, d, J= 8,4 Hz), 7,53 (H-6’, dd, J= 2,1 e 8,4 Hz), 7,62 (H-2’, d, J= 2,1 Hz). 13C-NMR (75 MHz: CD3OD, d): 60,51 (O-CH3), 94,70 (C-8), 99,75 (C-6), 105,84 (C-10), 116,42 (C-2’), 116,45 (C-5'), 122,31 (C-1'), 122,91 (C-6'), 139,53 (C-3), 146,46 (C-3'), 149,96 (C-4'), 158,00 (C-2), 158,41 (C-9), 163,09 (C-5), 165,92 (C-7), 180,01 (C-4).
Cromatografia líquida a vácuo (CLV): o sistema da CLV foi o mesmo empregado por Mello e Petrovick (2000) nas seguintes condições: coluna de vidro (20 mm Æ x 140 mm h); gel de sílica 60 (70-230 mesh ASTM, Merck); compressor/aspersor de ar a 51 kPa (~380 mmHg). 9,0 g de gel de sílica 60 foram empacotados na coluna e, a seguir, no topo da coluna, forma adicionados 1,26 g da FAQ.
Resultados e Discussão
Após as análises por CCD das frações semi-purificadas (FCL, FAQ e FR), a fração aquosa (FAQ) apresentou características de substâncias flavonoídicas. Através do uso da CLV, a fração FAQ-2 forneceu uma fase sobrenadante, que foi purificada por CCDP, obtendo-se a substância 1.
A substância 1 (Rf = 0,50) apresentou extinção de fluorescência em CCD sob luz UV254 e intensamente amarelada com vapores de amônio. O espectro de massas de 1 revelou [M+H]+ m/z 317, foi compatível com a fórmula molecular C16H12O7. A análise de RMN 1H apresentou um singleto em d 3,78 ppm, característico de grupamento metoxila (O-CH3). A presença de dois dubletos em d 6,19 e 6,38 ppm (4J = 2,4 e 2,4 Hz) é um padrão característico dos hidrogênios H-6 e H-8 do anel A, respectivamente. Observa-se, ainda, pelo espectro de 2D-COSY (1H/1H) uma correlação entre os sinais em d 6,90, 7,53 e 7,62 ppm, típico de um sistema AMX, correspondendo aos hidrogênios H-5’ (J = 8,4 Hz), H-6’ (J = 8,4 e 2,1 Hz) e H-2’ (J = 2,1 Hz), respectivamente. Os dados de RMN 13C foram semelhantes àqueles obtidos por Roitman e James (1985) apresentando em 60,51 ppm um sinal característico de metoxila. As pequenas variações obtidas nos espectros relacionam-se com o tipo de solvente empregado. Assim, comparando-se os dados obtidos com os da substância 1, a mesma foi identificada como sendo 3-O-metilquercetina. Essa substância já foi isolada anteriormente de Aspelnium viride Huds. (Voirin e Jay, 1974), de Gutierrezia microcephala (DC.) A. Gray (Roitman e James, 1985) e de Achyrocline satureioides (Lam.) DC. e Achyrocline alata (H.B.K.) DC. (Ferraro et al., 1981; Simões e Bauer, 1983; Bauer et al., 1987).
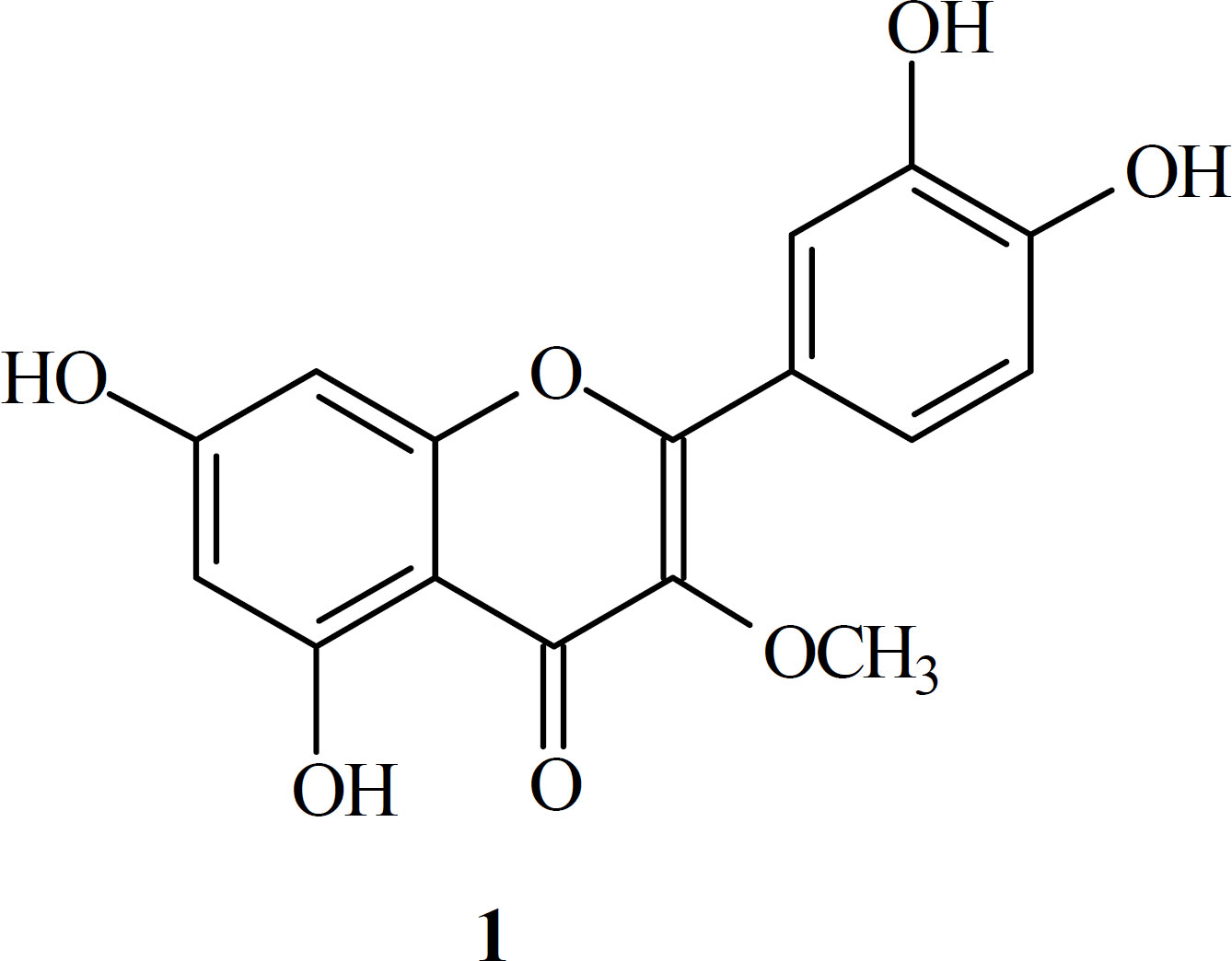
O isolamento da substância 3-O-metil-quercetina confirma a utilização da cromatografia líquida a vácuo como um possível método analítico e quantitativo para o extrato de marcela. Essa forma de análise já foi discutida por Coll e Bowden (1986) e Pelletier et al. (1986). Os autores aplicaram a CLV, modificando parcialmente o sistema, na separação de misturas de terpenos e alcalóides puros, respectivamente, obtendo bons resultados, tanto qualitativo como quantitativo.
Outras aplicações da CLV foram realizadas por Schroeder et al. (1996) e Villasenor et al. (1996) que utilizaram a CLV no isolamento do antibiótico pirrolosporina A, produzido por Micromonospora sp., além do espinasterol (esterol antigenotóxico) das flores de Cucurbita maxima Duchesne, respectivamente, bem como Cuesta-Rubio et al. (2001) que empregaram a CLV no isolamento de benzofenonas poliisopreniladas.
Assim, a CLV pode ser empregada em diferentes tipos de análises, tornando-se necessário o desenvolvimento individualizado para cada extrativo vegetal. No entanto, a validação do método CLV deve ser feita através de uma metodologia reprodutível, confiável, como a cromatografia líquida de alta eficiência, conforme estabeleceram De Souza et al. (2002) para Achyrocline satyureioides (Lam.) DC. O teor obtido de 3-O-metil-quercetina, aplicando-se a CLV, para cada 100 g de droga vegetal foi de 1,21%. Evidentemente que a validação do método é necessária, porém, como passo inicial ao uso rotineiro, e devidamente estabelecido, o método poderá ser validado e empregado sistematicamente pela indústria farmacêutica como alternativa a outros métodos.
Agradecimentos: Este trabalho foi auxiliado pelo Conselho Nacional de Desenvolvimento Científico e Tecnológico - CNPq. Os autores agradecem a A. Arantes pelo suporte técnico laboratorial.
Referências
BAUER, L.; SIMÕES, C.M.O.; SIQUEIRA, N.C.S.; SCHENKEL, E.P.; SILVA, G.A.A.B.; ALICE, C.B. Flavonoids of the inflorescences of Achyrocline alata. Revista Latinoamericana de Química, v.18, n.3, p.91, 1987.
COLL, J.C.; BOWDEN, B.F. The application of vacuum liquid chromatography to the separation of terpene mixtures. Journal of Natural Products, v.49, n.5, p.934-936, 1986.
CUESTA-RUBIO, O.; VELEZ-CASTRO, H.; FRONTANA-URIBE, B.A.; CÁRDENAS, J. Nemorosone, the major constituent of floral resins of Clusia rosea. Phytochemistry, v.57, p.279-283, 2001.
DE SOUZA, K.C.B.; SCHAPOVAL, E.E.S.; BASSANI, V.L. LC determination of flavonoids: separation of quercetin, luteolin and 3-O-methylquercetin in Achyrocline satureioides preparations. Journal of Pharmaceutical and Biomedical Analysis, v.28, p.771-777, 2002.
FERRARO, G.E.; NORBEDO, C.; COUSSIO, J.D. Polyphenols from Achyrocline satureioides. Phytochemistry, v.20, n.8, p.2053-2054, 1981.
HOSTETTMANN, K.; QUEIROZ, E.F.; VIEIRA, P.C. Princípios ativos de plantas superiores. São Carlos: EdUFSSCar, 2003. p. 101-146.
MELLO, J.C.P.; PETROVICK, P.R. Quality control of Baccharis trimera (Less.) DC. (Astearaceae) hydroalcoholic extracts. Acta Farmaceutica Bonaerense, v.19, n.3, p.211-215, 2000.
PELLETIER, S.W.; CHOKSHI, H.P.; DESAI, H.K. Separation of diterpenoid alkaloid mixtures using vacuum liquid chromatography. Jornal of Natural Products, v.49, n.5, p.892-900, 1986.
ROITMAN, J.N.; JAMES, L.F. Chemistry of toxic range plants highly oxygenated flavonol methyl ethers from Gutierrezia microcephala. Phytochemistry, v.24, n.4, p.835-848, 1985.
SCHROEDER, D.R.; COLSON, K.L.; KLOHR, S.E.; LEE, M.S.; MATSON, J.A.; BRINEN, L.S.; CLARDY, J. Pyrrolosporin A, a new antitumor antibiotic from Micromonospora sp C39217-Rr109-7: II. Isolation, physico-chemical properties, spectroscopic study and X-ray analysis. Journal of Antibiotics, v.49, n.9, p.865-872, 1996.
SIMÕES, C.M.O.; BAUER, L. Investigação químico-farmacológica de Achyrocline satureioides (Lam.) DC., Compositae. In: SIMPÓSIO NACIONAL DE FARMACOLOGIA E QUÍMICA DE PRODUTOS NATURAIS, 2., 1983, João Pessoa, PB. Anais. João Pessoa:UFPB, 1983. p.415-419.
SZEPESI, G. HPLC in Pharmaceutical Analysis. Boca Raton: CRC Press, v.1, p.3-26, 1990.
TARGETT, N.M.; KILCOYNE, J.P.; GREEN, B. Vacuum liquid chromatography: an alternative to common chromatographic methods. Journal of Organic Chemistry, v.44, n.26, p.4962-4964, 1979.
VILLASENOR, I.M.; LEMON, P.; PALILEO, A.; BREMNER, J.B. Antigenotoxic spinasterol from Curcubita maxima flowers. Mutation Research, v.360, n.2, p.89-93, 1996.
VOIRIN, B.; JAY. M. Sur la présence de méthyl-3 quercétine chez Asplenium viride. Phytochemistry, v.13, p.275-276, 1974.