Artigo Original
Estudo fitoquímico de folhas de Croton cajucara Benth e determinação da sua propriedade antioxidante
Phytochemical investigation of the leaves of Croton cajucara Benth and its antioxidative properties
Resumo
O estudo fitoquímico realizado com os extratos hexânico (EH), clorofórmico (EC) e metanólico (EM) obtidos de folhas de Croton cajucara Benth, resultou no isolamento de uma mistura hidrocarbônica apolar rica em triacontano, esteróides (β-sitosterol, estigmasterol e 3-O-glicopiranosilβ-sitosterol), flavonóides (3,7,4’-tri-O-metilcanferol e 3,7-di-O-metilcanferol), e um diterpeno do tipo 19-nor-clerodano (cajucarinolida). A investigação fitoquímica realizada com folhas de plantas com idades variando entre 1½ - 6 anos, revelou que a época de coleta e a idade da planta não provocam variação na quantidade produzida do flavonóide 3,7,4’-tri-O-metilcanferol (0,005%), tendo sido observadas variações nos percentuais de isolamento das misturas hidrocarbônica (0,11 - 0,28%) e esteroidal (0,01 - 0,15%). Em função da difícil solubilização dos extratos EH, EC e EM nos solventes biológicos, a atividade antioxidante só foi avaliada (utilizando-se como fonte de radical livre o DPPH) após dissolução em sistemas microemulsionados (SME) contendo a mistura de tensoativos Tween 80/ Span 20. O sistema SME-1 rico em água (60%) dissolveu satisfatoriamente o extrato polar (EM). Ambos os sistemas SME-3 e SME-4 (5% de água) dissolveram bem o extrato apolar (EH). O extrato de polaridade média EC também apresentou solubilidade satisfatória no sistema SME-4; tendo sido observado diferença significativa nos valores de EC50 (280 mg/mL para EC solubilizado no sistema SME-3 e 362 mg/ mL para SME-4).
- Unitermos:
- Croton cajucara.
- Composição Química.
- Variação Sazonal.
- Sistemas Microemulsionados.
- Propriedade Antioxidante.
Abstract
Phytochemical studies on the hexane (EH), chloroform (EC) and methanol (EM) extracts obtained from the leaves of Croton cajucara Benth resulted in the isolation of the known compounds β-sitosterol, stigmasterol, sitosterol-3-O-β-glucoside, kaempferol 3,4’,7-trimethyl ether, kaempferol 3,7-dimethyl ether, diterpene cajucarinolide and a non-polar hydrocarbon mixture which was rich in triacontan. The content of the hydrocarbon mixture and steroids varied according to both plant age and season of the year (ranging from 0.11 - 0.28% and 0.01 - 0.15%, respectively). Meanwhile, the seasonal evaluation of the plants leaf aging from 1½ to 6 years old showed that neither age nor the year period have affected the contents of kaempferol 3,4’,7-trimethyl ether, which was present as 0.005% in the leaves of plants along the whole age period. Due to the poor solubility of the EH, EC and EM extracts, the antioxidant effect was evaluated (DPPH-method) after their incorporation to microemulsion systems (SME) performed with a mixture of the surfactants Tween 80 and Span 20. The polar extract (EM) showed higher solubility in the SME-1 system (60% water). Both SME-3 and SME-4 systems (5% water) dissolved the non-polar extract EH. However, the chloroform extract showed higher solubility in the SME-4 system, what seems to affect the EC50 values (362 mg/mL) compared with the values for SME-3 system (280 mg/mL).
- Key Words:
- Croton cajucara.
- Chemical Constituents.
- Seasonal Variety.
- Microemulsions Systems.
- Antioxidant Properties.
Introdução
Croton cajucara Benth (Euphorbiaceae), vulgarmente conhecido por “sacaca”, representa um recurso medicinal de grande importância no tratamento e cura de várias doenças (MACIEL et al., 2002a, 2002b). De acordo com informações etnobotânicas, as folhas desta espécie são comercializadas em feiras livres da cidade de Belém-PA com indicação hepatoprotetora (MACIEL et al., 2002a, 2002b). No entanto, comprovou-se que o uso abusivo deste Croton pode acarretar hepatite tóxica (MACIEL et al., 2002a, 2002b; SOARES, 2004; VEIGA Jr. et al., 2005). Casos de hepatite aguda, crônica e fulminante foram notificados em pacientes da região Amazônica, que fizeram uso da sacaca no controle de peso corporal e redução de níveis elevados de colesterol (MACIEL et al., 2002b; SOARES, 2004; VEIGA Jr. et al., 2005). No entanto, apesar destes relatos sobre a toxidez, vem se comprovando ao longo das últimas duas décadas, que substâncias isoladas das cascas do caule e das folhas de C. cajucara, bem como extratos (obtidos de folhas ou cascas do caule deste Croton) são terapeuticamente eficazes, sem que efeitos tóxicos relevantes sejam evidenciados. Citando apenas alguns exemplos, ações antiinflamatória, hipoglicêmica, hipolipidêmica, antiulcerogênica, cardiovascular, anticâncer, antimutagênica e citotóxica foram amplamente investigadas (AGNER et al., 1999; AGNER et al., 2001; CAMPOS et al., 2002; Costa et al., 2007; FARIAS et al., 1996; FARIAS et al., 1997; FARIAS et al., 2005; HIRUMA-LIMA et al., 1999; HIRUMA-LIMA et al., 2002; KHAN et al., 2009; MACIEL et al., 2000; MACIEL et al., 2006a; PERAZZO et al., 2007; SANTOS et al., 2006; SILVA et al., 2001a, 2001b, 2001c; SILVA et al., 2005; SOUZA et al., 2006). Além disso, estudos de toxicidade aguda e subcrônica, realizados com o clerodano majoritário trans-desicrocrotonina isolado das cascas do caule de C. cajucara, revelaram baixa toxicidade (RODRÍGUEZ et al., 2004; SOUZA-BRITO et al., 1998).
Em decorrência da grande representatividade da espécie C. cajucara na medicina tradicional da região Amazônica do Brasil e, mais recentemente, pela expansão do seu uso em outras regiões do país (VEIGA Jr. et al., 2005), focamos a ampliação do seu estudo. O presente trabalho resultou no isolamento e caracterização de constituintes químicos isolados de extratos obtidos de folhas de C. cajucara, tendo sido realizado um monitoramento da variação na produção (verificado pelos percentuais nos isolamentos) dos constituintes químicos presentes em árvores com idades variáveis, coletadas em épocas e ambientes diferentes, bem como na avaliação da ação antioxidante de extratos veiculados em nanosistemas do tipo microemulsão.
Microemulsões são sistemas coloidais termodinamicamente estáveis e opticamente isotrópicos contendo água, óleo, tensoativo e, frequentemente, um cotensoativo (FLORENCE, 2005). Estas formulações vêm sendo utilizadas como sistemas de liberação de fármacos devido a inúmeras vantagens, podendo-se destacar: o aumento da capacidade de solubilização de fármacos e a diminuição de efeitos adversos (FORMARIZ et al., 2005; OLIVEIRA et al., 2004; LAWRENCE; REES, 2000). O aumento da biodisponibilidade de fármacos está correlacionado com a solubilização de substâncias pouco solúveis, bem como com a diminuição da dose administrada, garantindo além de vantagens econômicas, a diminuição de efeitos adversos (KAWAKAMI et al., 2002).
Material e Métodos
A identificação botânica de C. cajucara Benth foi feita por Nelson A. Rosa do Museu Paraense Emílio Goeldi, em cujo herbário a exsicata foi depositada, sob código 247. As coletas de C. cajucara foram realizadas em áreas nativas ou cultivadas. As coletas das plantas cultivadas, com idades variando entre 1½ - 6 anos, foram realizadas no Sítio Tamuassaú, localizado há poucos quilômetros de Belém-PA. O material de árvores com 1½ anos de idade foi coletado em novembro de 1993; uma das árvores foi cultivada em área exposta ao sol e a outra em área sombreada por árvores vizinhas (semelhante à área nativa). Neste mesmo sítio, em junho de 1995, o material foi coletado de um espécime com 3 anos de idade, cultivado em área exposta ao sol. Árvores com idades entre 4-6 anos foram coletadas distintamente; a primeira delas (origem nativa) foi realizada em 1985 em Bragança-PA, o material vegetal moído e hermeticamente armazenado em saco plástico sob refrigeração de ar condicionado, até a ocasião de seu uso em 1993, apresentando perfeito estado de conservação. A segunda coleta neste grupo de árvores (área exposta ao sol) foi realizada em junho de 1993 no sítio Tamuassaú em Belém-PA e a terceira coleta (área nativa) foi realizada em Jacundá-PA, em abril de 1994. Após cada coleta, o material vegetal foi separado por partes (folhas, galhos, caule, raízes e cascas do caule), seco em estufa a temperatura de 40 oC. O pulverizado de cada parte coletada foi extraído por percolação, com solventes em gradiente de polaridade crescente. Os filtrados foram concentradas sob pressão reduzida, para originar os extratos hexânico (EH), clorofórmico (EC) e metanólico (EM) para cada material coletado. Todas as amostras foram submetidas a processos cromatográficos no período entre 1993 - 1995.
Nas separações cromatográficas em coluna aberta utilizou-se como adsorvente gel de sílica (35-70 e 70-230 Mesh). As cromatografias de camada fina (CCF) foram efetuadas utilizando-se gel de sílica 60H. Para revelação das placas em CCF foram utilizados vapores de iodo, solução de sulfato cérico, ácido sulfúrico/metanol 1:1 e reagente de Dragendorff. O critério de pureza adotado foi a obtenção de um único e uniforme sinal em CCF, variando-se o sistema de solvente empregado. De cada planta coletada utilizou-se cerca de 1 kg de folhas na obtenção de EH e EC. Como exemplo, para 1 kg de folhas de árvores coletadas em área nativa, obteve-se 14,6 g de EH e 28,2 g de EC. EM foi obtido de folhas de árvores coletadas em área nativa. Estes extratos foram submetidos à cromatografia em gel de sílica, conforme descrito na Figura 1.

Os espectros na região do infravermelho (IV) foram registrados em espectrofotômetro Perkin-Elmer, modelo 16 PC com transformada de Fourier. Foram utilizadas pastilhas de KBr para as substâncias sólidas contendo aproximadamente 1% de amostra. Os espectros de ultravioleta (UV) foram registrados em espectrofotômetro GBC UV/VIS 911A CG Analitica Ltda. Os pontos de fusão foram determinados em um bloco Kofler (Jasco DIP-370), com um termômetro não aferido previamente. Os espectros de massas (EM) foram registrados em espectrômetro CG/MS Finnigan-4000 e VG Auto Spec Q-70eV (baixa resolução). Os espectros de ressonância magnética nuclear de hidrogênio (RMN de 1H) e de carbono-13 (RMN de 13C) foram registrados em espectrômetro Varian, modelo Gemini, operando a 300 e 75,4 Hz, respectivamente, bem como em espectrômetro Bruker, operando a 200 (RMN de 1H) e 50 MHz (RMN de 13C). O padrão utilizado como referência interna foi o sinal do próprio solvente empregado para solubilizar as amostras.
O fracionamento e isolamento a partir da mistura hidrocarbônica e (MH) foi monitorado utilizandose a mesma metodologia descrita na Figura 1, obtendo-se 2,8 g da MH (1,9 g proveniente do EH e 0,9 g do EC) provenientes de folhas das árvores com 4-6 anos de idade, a partir de 1 kg de material vegetal, em diferentes coletas; 1,6 g da MH (1,1 g no EH e 0,5 g no EC) de folhas da árvore com 3 anos de idade (1 kg de material vegetal); 1,02 g da MH (1,0 g no EH e 0,02 g no EC) da árvore com 1½ ano (cultivada em ambiente exposto ao sol, partindo-se de 0,9 kg de material vegetal); e 2,3 g (2,0 g proveniente do EH e 0,3 g do EC) da árvore com 1½ ano (0,9 kg de material vegetal) cultivada em área sombreada por árvores vizinhas (semelhante ao ambiente nativo).
Obtenção dos sistemas microemulsionados: As microemulsões testadas foram preparadas utilizando a mistura Tween 80 e Span 20 (3:1) como tensoativo, miristato de isopropila (IPM) como óleo (fase orgânica) e água bidestilada de acordo com metodologia previamente descrita (GOMES et al., 2006). Em apenas um dos sistemas testados (SME-4) não se utilizou etanol como cotensoativo, nos demais sistemas (SME-1 e SME-4) o etanol foi utilizado na razão C/T = 1 (Tabela 1). Os diagramas de fase foram obtidos a partir da titulação com água bidestilada e fase oleosa (quando necessário) de misturas prédeterminadas contendo tensoativo/cotensoativo.
| Componente | Massa obtida (%) | ||
| SME-1 | SME-3 | SME-4 | |
| Tween 80 | 13,12 | 18,75 | 22,50 |
| Span 20 | 4,38 | 6,25 | 7,50 |
| Etanol | 17,50 | 25,00 | ¾ |
| IPM | 5,00 | 45,00 | 65,00 |
| Água bidestilada | 60,00 | 5,00 | 5,00 |
Avaliação da atividade antioxidante: Na metodologia empregada para a avaliação da atividade antioxidante utilizou-se como fonte de radical livre o DPPH (2,2-difenilpicril-hidrazila) (MENSOR et al., 2001). As soluções estoque foram preparadas em metanol na concentração de 1 mg/ mL. O ensaio foi realizado em microplacas de 96 poços, no volume total de 100 μL. Foram feitas diluições dos extratos para as concentrações de 710, 71, 7,1 e 0,71 μg/mL, que foram adicionadas às microplacas, juntamente com uma solução 0,3 mM de DPPH (em metanol). Após o tempo de 30 minutos de repouso no escuro, foi feita a leitura das microplacas em leitora Elisa a 490 nm. Foram realizados 3 ensaios independentes, todos em triplicata. O percentual antioxidante foi calculado a partir da seguinte equação:
%AA = 100−(A amostra - A branco) × 100 / A controle
onde:
A amostra = absorbância da amostra correspondente ao extrato com DPPH
A branco = absorbância do branco correspondente ao extrato sem DPPH
A controle = absorbância da solução pura de DPPH 0,3 mM
A atividade antioxidante foi expressa em valores de CE50 ± dp, obtidos através do gráfico que relaciona o percentual de atividade antioxidante (%AA) contra a concentração da substância ensaiada.
Resultados e Discussão
O fracionamento cromatográfico do extrato hexânico (EH) conduziu ao isolamento de uma mistura de hidrocarbonetos (frações F1-12 do EH e F1-7 do extrato CHCl3), em que o triacontano (sólido de coloração branca) é o componente majoritário com percentual elevado (65%). As frações F25-26 (eluídas com hexano:AcOEt 98:2) forneceram, após re-fracionamento cromatográfico, 1,0 g de um sólido amorfo correspondente à coocorrência de b-sitosterol e estigmasterol, na proporção 89:11, evidenciado por RMN. Estes esteróides foram caracterizados por dados espectroscópicos, estando de acordo com dados previamente reportados na literatura (PERES et al., 1997). Observou-se na região de IV os seguintes máximos de absorções: 3425 cm-1 (grupo hidroxila), 2936 e 2867 (grupos CH2 e CH3), 1465 e 1379 cm-1 (ligações C-H alifáticas), 1640 e 958 cm-1 (olefina trans dissubstituída). O RMN de 1H apresentou hidrogênios olefínicos em d 5,34 [d largo (J = 5,2 Hz)], 5,14 [dd (J = 8,4 e 15,2 Hz)] e 5,00 [dd (J = 8,8 e 15,2 Hz); carbinólico em δ 3,51 (m); metílicos e metilênicos na faixa entre 0,66-2,24 ppm]. A baixa intensidade dos duplos dubletos em 5,14 (H-23) e 5,00 (H-22) ppm (correspondentes ao estigmasterol), quando comparada com a intensidade do sinal de hidrogênio olefínico em 5,34 ppm (H-6 de β-sitosterol e estigmasterol) apontou o β-sitosterol como componente principal na mistura (89%). No espectro de RMN de 13C, os sinais correspondentes aos carbonos característicos do estigmasterol são visivelmente menos intensos ou nem aparecem. Também, as intensidades dos hidrogênios olefínicos H-6, H-22 e H-23 [δ 5,34 H-6 (d largo); 5,20 H-23 (dd) e 5,00 H-22 (dd) ppm] de uma amostra autêntica de estigmasterol, são equivalentes entre si, corroborando com a sugestão do β-sitosterol como o componente majoritário na mistura esteroidal (ME) oriunda de folhas de C. cajucara. Os deslocamentos químicos (δ) 23,1, 36,5 e 45,9 ppm, correspondentes aos carbonos C-28, C-20 e C-24 respectivamente, são exclusivos do β-sitosterol e os δ 129,4 (C-23) e 138,0 (C-22) ppm são exclusivos do estigmasterol.
As frações F27-29 (provenientes do EH; eluídas com 3-4% de AcOEt em hexano), bem como o grupo de frações F30-36 (provenientes do EC; eluídas com 2-4% de AcOEt em hexano) forneceram uma mistura do flavonóide 3,7,4’-tri-O-metilcanferol (visualmente de coloração amarelo-ouro) ainda com presença de β-sitosterol e estigmasterol. As análises de CCF de F27-29 e F30-36 revelaram um único sinal em diferentes sistemas de eluição, evidenciando o mesmo Rf para ME e o flavonóide. No entanto, diferenças significativas nas colorações foram obtidas com o de reagentes sulfato cérico ou ácido sulfúrico-MeOH como reveladores, fixando a coloração para ME e amarela para 3,7,4’-tri-O-metilcanferol. Adicionalmente, a ME apresentou solubilidade diferenciada em acetona, sendo o flavonóide muito mais solúvel neste solvente; o que permitiu a dissolução seletiva das frações F27-29 e F30-36. O processo foi repetido até que a ME estivesse praticamente separada do flavonóide, tendo sido necessário, finalizando-se a purificação do flavonóide com uma microcoluna em gel de sílica (frações de 10 mL; eluente: gradiente 1-4% de AcOEt em hexano), resultando no isolamento de 190,0 mg de ME e 35,1 mg de 3,7,4’-tri-O-metilcanferol (provenientes das frações originais F27-29) e 138,0 mg de ME e 63,8 mg do flavonóide (frações F30-36). O espectro de IV deste flavonóide mostrou um máximo de absorção característico de carbonila α,β-insaturada em 1659 cm-1. Apesar do grupo OH não ter sido claramente evidenciado no espectro de IV, foi apontado pela coloração marrom-escuro em CCF, quando revelado com o FeCl3, bem como no espectro de UV em solução metanólica de hidróxido de sódio. Neste espectro, a hidroxila fenólica foi evidenciada pelos deslocamentos batocrômicos dos máximos de absorção 290 (deslocamento de 17 nm com acentuado aumento na intensidade da banda) e 371 nm (deslocamento de 22 nm com diminuição da intensidade da banda). O espectro de UV em solução metanólica mostrou bandas de absorção (273 e 349 nm) características de flavonóides do tipo flavona ou flavonol 3-O-substituído (MARKHAM; MABRY, 1975; MARKHAM, 1982). A regeneração das curvas em meio neutro foi evidenciada comparando-se as respostas no espectro de UV pelo uso de MeOH + NaOH / MeOH + HCl. A possibilidade de existência da subunidade fenólica na estrutura química deste flavonóide é reforçada pelos máximos de absorção em 1601, 1585 e 1498 cm-1 característicos de região aromática no IV. No espectro de RMN de 1H, o sinal deste hidrogênio hidroxílico aparece em 12,67 ppm, indicando a formação de ponte de hidrogênio intramolecular (pelo deslocamento químico em campo muito baixo). Neste espectro, a presença de grupos metoxilas foi constatada pelos sinais em 3,90 (s, 3H), 3,88 (s, 3H) e 3,86 (s, 3H) ppm e, no espectro de RMN de 13C pelos sinais em 60,0; 55,7; 55,3 ppm. A carbonila α,β-insaturada (observada no espectro de IV em 1659 cm-1) foi confirmada pelo deslocamento químico em 178,7 ppm (RMN de 13C).
A constante de acoplamento J = 2,2 Hz observada nos deslocamentos químicos δ 6,45 (d, 1H) e 6,36 (d, 2H) sugeriu o acoplamento meta para os hidrogênios H-8 e H-6 do anel A, definindo então a posição de um dos três grupos metoxilas, que estaria localizado no carbono C-7 do anel A, com o outro grupo metoxila ocupando a posição C-4’ do anel B. Dessa forma, justificam-se os dois dubletos (cada um integrando 2 hidrogênios) em 8,10 e 7,03 ppm (acoplamento orto, J = 9,2 Hz). A regeneração das curvas no espectro de UV em meio neutro também está de acordo com a ausência de sistemas orto ou para substituídos; assim como o efeito batocrômico, com diminuição da intensidade da banda I evidenciada pela adição de NaOH (indicativo de que poderia existir OCH3 na posição C-4’). Por eliminação, o último grupo metoxila estaria ocupando a posição C-3. A posição C-5 não foi vista como uma segunda opção porque a presença de hidroxila fenólica (teste positivo com FeCl3) requeria o grupo OH localizado em C-5, já que as posições C-7 e C-4’ estariam ocupadas por metoxilas. A ausência de singleto integrando um hidrogênio na faixa entre 6,30-6,60 ppm no RMN de 1H eliminou a possibilidade deste flavonóide ser do tipo flavona, restando conseqüentemente, a estrutura do flavonol 3,7,4’-tri-O-metilcanferol, de grande ocorrência natural (DREYER, 1978). O espectro de massas deste flavonol mostrou o pico do íon molecular de m/z 328 [M]+, confirmando a estrutura proposta. Os fragmentos de íons m/z 327 e 285 são consistentes com a localização do grupo metoxila na posição C-3. O fragmento de íon m/z 135 (pico base) confirmou a presença de metoxila no anel B (Figura 2).

A maioria dos flavonóides apresenta no espectro de UV dois máximos de absorção que ocorrem entre 240-285 e 300-550 nm, chamados de banda II e banda I, respectivamente (MARKHAM; MABRY, 1975; MARKHAM, 1982). A absorção referente a banda II origina-se do sistema benzoil do anel A e a banda I do sistema cinamoil do anel B (Figura 3). Dentre as classes de flavonóides mais amplamente distribuídos na natureza encontram-se as flavonas, os flavonóis e as flavanonas (Figura 3) que apresentam, em sua grande maioria, o padrão de hidroxilação característico de flavonóides, onde o anel A pode ser do tipo floroglucinol (1,3,5-triidroxibenzeno) ou resorcinol (1,3-diidroxibenzeno) e o anel B, aparece hidroxilado nas posições 4’, 3’, 4’ ou 3’, 4’, 5’. Numerosos derivados destes constituintes fundamentais são conhecidos pelo número distinto de hidroxilas, metoxilas e pela presença ou não, de ligações glicosídicas (MARKHAM; MABRY, 1975; MARKHAM, 1982).

O grupo de frações F63-89 (provenientes do EC; eluído com 12-40% de AcOEt em hexano; Figura 1), forneceu 57,6 mg do diterpeno 19-nor-clerodano cajucarinolida, previamente isolado das cascas do caule de Croton cajucara (ICHIHARA et al., 1992; MACIEL et al., 1998a), bem como 10,9 mg de um outro constituinte químico com características de flavonóide polar. Estes componentes foram purificados via recristalizações em clorofórmio, tendo apresentado, após purificação os seguintes rendimentos: 0,001% (flavonóide polar) e 0,006% (diterpeno do tipo clerodano cajucarinolida). Este clerodano possui atividade antiinflamatória (ICHIHARA et al., 1992) e citotóxica (MACIEL et al., 2007). Não há até o momento atual, nenhum trabalho relatando o isolamento desta substância em outra espécie de Croton, ou mesmo, em outro gênero.
As avaliações preliminares da estrutura química do flavonóide polar presente nas frações F63-89, mostraram em CCF a presença de hidroxila fenólica pelo resultado positivo com FeFl3; carbonila α,β-insaturada (1661 cm1) e hidroxila (3257 cm-1) no espectro de IV; e bandas de absorções em 273 e 353 nm no espectro de UV, características de flavonóides do tipo flavona ou flavonol (MARKHAM; MABRY, 1975; MARKHAM, 1982) do tipo 3-O-substituído. No espectro de RMN de 1H, observouse hidroxila quelada em 11,99 ppm (singleto, 1 H) e dois grupos metoxilas com sinais em 3,15 e 3,11 ppm. Para esta substância, havendo substituição na posição C-4’, faltaria incluir mais um grupo substituinte já que só aparecem no espectro de RMN de 1H dois sinais de grupo metoxila e um sinal de hidroxila quelada. No entanto, constatou-se um total de quatro substituições (posições C-3, C-5, C-7 e C-4’). A ausência de singleto integrando um hidrogênio, na faixa entre δ 6,30-6,60 no espectro de RMN de 1H, eliminou a possibilidade de estrutura flavonica, restando, consequentemente, a possibilidade de flavonol. Desta forma, foram propostas quatro estruturas isoméricas para este flavonóide (Figura 4). Como a ligação de hidrogênio intramolecular do hidrogênio fenólico com a carbonila provocaria deslocamento químico para campo mais baixo, no espectro de RMN de 1H, esta ligação poderia existir entre o grupo hidroxila posicionado no carbono C-3 (II e IV, Figura 4) ou no carbono C-5 (I e III). Na primeira opção, ocorre formação de anel de cinco membros, com o sinal relativo ao hidrogênio fenólico aparecendo em torno de 10 ppm; na segunda possibilidade, há formação de anel de 6 membros e o sinal do hidrogênio fenólico seria registrado acima ou em torno de 12 ppm (MARKHAM; MABRY, 1975). Como o sinal observado para a hidroxila quelada foi registrado em 11,99 ppm, estabeleceu-se o posicionamento deste grupo na posição C-5, eliminando-se, portanto, as possibilidades estruturais II e IV.

O espectro de UV em solução metanólica de hidróxido de sódio indicou que a hidroxila não poderá ocupar a posição C-7 porque não há surgimento de uma nova banda na faixa entre 320-335 nm (DREYER, 1978; MARKHAM; MABRY, 1975; MARKHAM, 1982). Somada às informações anteriores, este resultado elimina a estrutura III como uma possibilidade, induzindo o seguinte padrão de substituição: OH posicionadas em C-5 e C-4’ e grupo metoxila (OMe) posicionado em C-7 e C-3 (estrutura I, Figura 4). A hidroxila da posição C-4’ foi confirmada pelos deslocamentos batocrômicos da banda II, nos espectros de UV. Em solução metanólica de hidróxido de sódio ocorreu deslocamento batocrômico de 43 nm e em solução metanólica de cloreto férrico, ocorreu deslocamento batocrômico de 39 nm e surgimento de novas bandas em 360 e 308 nm. A substância corresponde, portanto, ao flavonol 3,7-di-O-metilcanferol (Figura 5), previamente reportado na literatura (VALESI, 1972).

A fração F114 (proveniente do EC; eluída em AcOEt; Figura 1) foi purificada em microcoluna de gel de sílica com sistema de eluição variando entre 50-100% de AcOEt em hexano. Neste re-fracionamento (eluente: AcOEt) obteve-se uma substância polar de característica esteroidal. O espectro de IV mostrou absorção forte em 3415 cm-1 (grupo hidroxila), justificando a polaridade relativamente alta desta substância. O espectro de RMN de 1H, apresentou absorção de hidrogênio olefínico [5,21 ppm (d largo, J = 5,2 Hz)], hidrogênios carbinólicos (3,04 - 3,69 ppm) e hidrogênios metílicos e metilênicos (0,52 - 2,29 ppm). Estas informações, somadas com o grande número de sinais de absorção na região de hidrogênios carbinólicos, sugeriram a estrutura de um esteróide glicosilado. Os sinais em 100,8; 76,2; 75,6; 73,3; 69,9 e 61,5 ppm (RMN de 13C) são característicos de glicosídeos esteroidais, onde o açúcar é a glicose. A subunidade estrutural glicose foi identificada pelos sinais em 4,25 (d, J = 7,7 Hz); 3,69 (dd, J = 12,0 e 3,0 Hz); 3,59 (dd, J = 12,0 e 4,5 Hz); 3,43 (m) e 3,163,04 (m) ppm, no espectro de RMN de 1H. O espectro de RMN de 13C evidenciou uma concordância significativa para o β-sitosterol, concluindo-se pela identidade do esteróide glicosilado como 3-O-glicopiranosil-β-sitosterol, amplamente reportado na literatura (BILIA et al., 1996; PERES et al., 1997).
Variação dos teores de constituintes químicos de folhas de Croton cajucara
A variação dos teores dos constituintes químicos isolados de folhas de C. cajucara resultou de um estudo preliminar com as cascas do caule, galhos, caule, raízes e folhas deste Croton, em que a presença do diterpeno trans-desidrocrotonina (constituinte majoritário das cascas do caule deste Croton) era monitorada segundo a sazonalidade. Para tanto, esta espécie vegetal de origem nativa ou cultivada, foi coletada em diferentes épocas e ambientes de plantio (MACIEL et al., 1998b; MACIEL et al., 2000). Paralelamente a este estudo, foi possível comprovar que a mistura β-sitosterol e estigmasterol ocorre em todas as partes de C. cajucara Os teores máximos observados foram: 0,01% para raízes e cascas do caule; 0,02% para caule e galhos, e 0,15% para folhas. A Tabela 2 mostra a variação sazonal desta mistura esteroidal.

| Tipo de Árvore | Local de Coleta | Teor Isolado |
| Árvores com idades variando entre | Bragança-PA | folhas: 0,120 % |
| 4-6 anos (nativas) | (Ano: 1985) | caule: 0,001 % |
| Árvores com idades variando entre | Sítio Tamuassaú-PA | folhas: 0,030 % |
| 4-6 anos (cultivadas*) | (1993) | caule: n.o. |
| Árvores com idades variando entre | Jacundá-PA | cascas: traços |
| 4-6 anos | (1994) | caule: 0,021% |
| Árvore com 3 anos de idade | Sítio Tamuassaú-PA | folhas: 0,080 % |
| (cultivada*) | (1995) | cascas: 0,012 % |
| Árvore com 1 ano e % | Sítio Tamuassaú-PA | folhas: 0,010% ; galhos: 0,02% |
| de idade (cultivada*) | (1993) | cascas: 0,011%; raízes: 0,017% |
| Árvore com 1 ano e % | Sítio Tamuassaú-PA | folhas: 0,15%; galhos: 0,01% cascas: |
| de idade (cultivada**) | (1993) | 0,006%; raízes: 0,003 % |
| *cultivadas em área exposta ao sol. **área sombreada por árvores vizinhas; n.o. (não observado). | ||
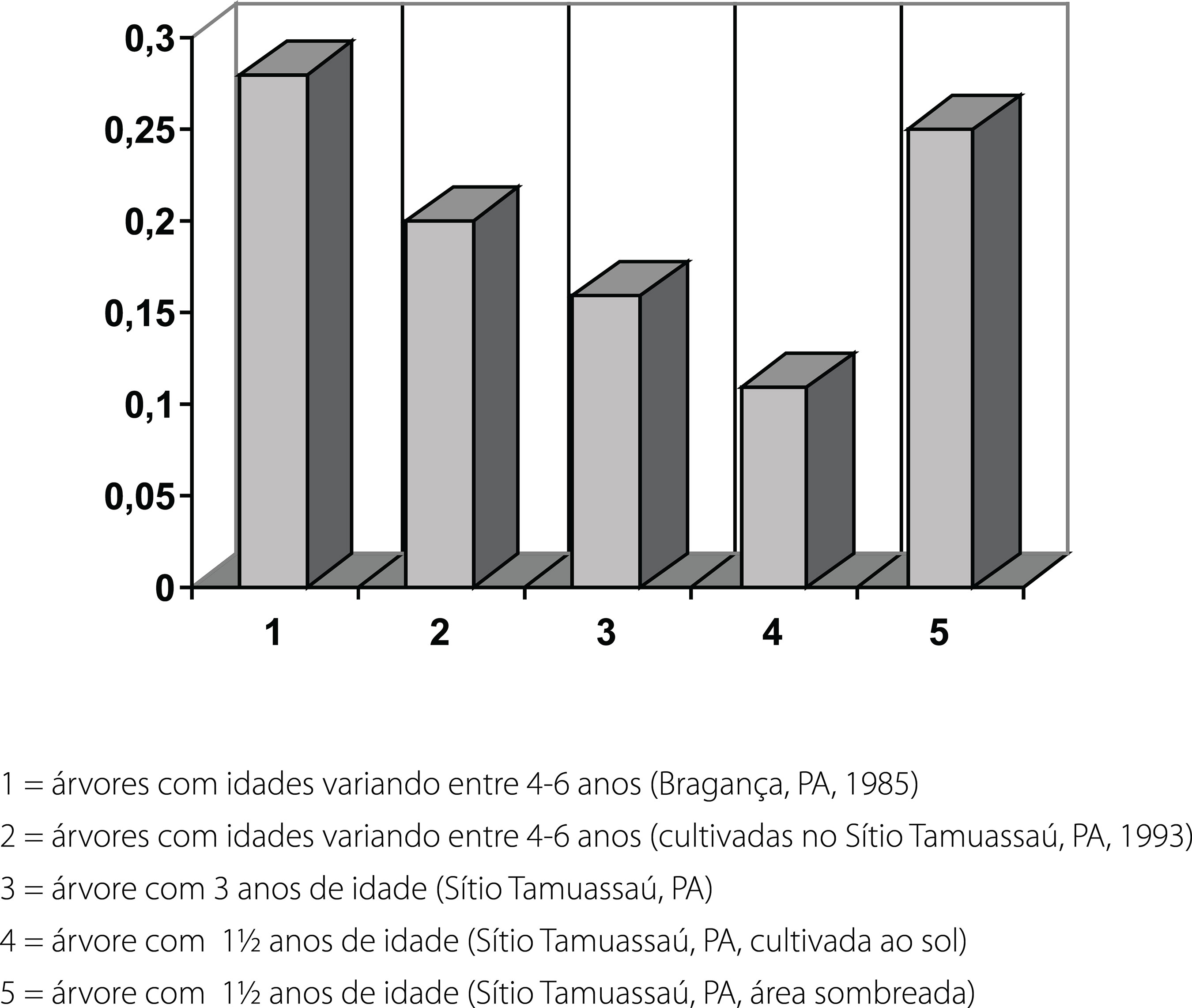
A Figura 6 mostra a variação sazonal de uma mistura hidrocarbônica rica em triacontano, presente nas folhas de árvores com idades diferentes. As coletas nas árvores com idades variando entre 4-6 anos (Figura 6, no 1) em 1985 (Bragança-PA) levaram ao isolamento da MH com rendimentos de 0,28%, e do flavonóide 3,7,4’tri-O-metilcanferol (0,009%). As árvores com idades variando entre 4-6 anos (Figura 6, no 2) foram cultivadas em área exposta ao sol, tendo sido coletadas em junho de 1993 (Sítio Tamuassaú, localizado há poucos quilômetros de Belém-PA). Nestas árvores o rendimento de MH foi 0,20% e 0,005% para o flavonóide. A árvore com 3 anos de idade (Figura 6, no 3), também cultivada em área exposta ao sol, gerou a coleta em junho de 1995 (Sítio Tamuassaú-PA). Nesta, o rendimento de MH foi 0,16% e do flavonóide 0,005%. A árvore com idade de 1½ ano (Figura 6, no 4), cultivada em área exposta ao sol, coletada em novembro de 1993 (Sítio Tamuassaú-PA), produziu MH com rendimento de 0,11%, com 0,006 % para o flavonóide. A árvore com idade de 1½ ano (Figura 6, no 5) foi cultivada em área sombreada por árvores vizinhas, tendo sido coletada em novembro de 1993 (Sítio Tamuassaú-PA). Nesta árvore o rendimento de MH foi 0,25% (Figura 6) e do flavonóide 0,005%. As plantas com idades entre 4-6 anos levaram ao rendimento de 0,28% de MH, o que foi compatível com o valor de 0,25% observado para a árvore com 1½ ano cultivada em área sombreada; apontando para o fato da idade da planta aparentemente não influenciar na quantidade de MH produzida. No entanto, o ambiente em que a árvore é cultivada influencia no rendimento total de isolamento da MH. A ocorrência do flavonóide 3,7,4’-tri-O-metilcanferol foi detectada em todos EH e EC de folhas de árvores com idade diferentes, não havendo variações significativas nos teores desta substância segundo a época de coleta, o ambiente de cultivo ou ainda, a idade da planta.
Atividade antioxidante das folhas de Croton cajucara e o processo de microencapsulamento
Diversos metabólitos especiais presentes nas plantas apresentam atividade antioxidante, sendo cada vez mais reconhecidos como importantes na captura de radicais livres formados em diferentes etapas do metabolismo que envolve processos de oxidação; estes diretamente relacionados ao processo de envelhecimento, às doenças degenerativas e especialmente ao câncer. No entanto, a utilização prática de muitos produtos naturais ainda é limitada, em decorrência da baixa solubilização em solventes biológicos. Para minimizar este tipo de problema, a biodisponibilização de produtos naturais pode ser otimizada via controle da liberação de fármacos com vantagens significantes na redução da dose terapêutica e diminuição de efeitos adversos. Neste contexto, a microencapsulação de fármacos permite: (a) o aumento de maneira racional e efetiva da eficácia terapêutica, bem como a diminuição da toxicidade dos fármacos pela redução dos picos de concentração plasmática máxima, objetivando manter em nível constante o fármaco no sangue; (b) o controle e prolongação da liberação do fármaco, reduzindo a frequência de doses; (c) a otimização da atividade biológica, resultando em doses mais baixas devido a sítio-especificidade e a proteção da substância terapêutica de efeitos deletérios dos fluidos do organismo (BERKLAND et al., 2002). Desta forma, a nanotecnologia farmacêutica representa uma das fronteiras científicas para o desenvolvimento de sistemas nanométricos carreadores de fármacos, contribuindo para o avanço no desenvolvimento de produtos farmacêuticos. Diversos trabalhos comprovaram o aumento da eficácia e a redução da toxicidade de substâncias bioativas de origem natural ou sintética, administrados em lipossomas (Ratner, 2002), sistemas nanoparticulados (BERKLAND et al., 2002; FENG et al., 2004) ou micropartículas (GUPTE; CIFTCI, 2004; RIBEIRO-COSTA et al., 2004).
Atualmente, estamos otimizando a utilização de ingredientes bioativos naturais em sistemas nanoencapsulados do tipo microemulsão (ME) (GOMES et al., 2006; ROSSI et al., 2007). Estas formulações têm viabilizando melhoras na solubilização das moléculas, assim como redução da dose terapêutica e diminuição de efeitos adversos (AZEVEDO et al., 2005; DALMORA et al., 2001; FORMARIZ et al., 2005; LYONS et al., 2000; OLIVEIRA et al., 2004). Uma das grandes vantagens no uso de microemulsões é a existência de microdomínios de diferentes polaridades no seio de uma solução unifásica, que permite a solubilização de substâncias hidrossolúveis ou lipossolúveis (LEE et al., 2003; OLIVEIRA et al., 2004). No presente trabalho, a avaliação da atividade antioxidante dos extratos EH, EC e EM obtidos das folhas de árvores jovens (AJ, 1½ ano de idade) e adultas (AD, 4-6 anos) de C. cajucara. Para tanto, estes extratos foram solubilizados nos seguintes sistemas microemulsionados: SME-1, SME-3 e SME-4 (Tabela 1). A avaliação da atividade antioxidante foi realizada com a metodologia que emprega a geração do radical livre DPPH e a leitura das microplacas foi feita em um aparelho leitor Elisa a 490 nm. Os resultados obtidos mostraram que todos os extratos testados apresentaram atividade antioxidante. A atividade antioxidante foi expressa em valores de CE50 ± dp (Tabela 1), obtidos através do gráfico que relaciona o percentual de atividade antioxidante (%AA) com a concentração da substância testada. Os resultados obtidos mostraram que os extratos de AJ foram mais ativos do que os das árvores adultas. Os sistemas SME-1 e SME-4 foram os que melhor solubilizaram o extrato mais polar (EM). Ambos os sistemas SME-3 e SME-4 solubilizaram bem o extrato menos polar es EH. Já a solubilização de EC teve seu melhor resultado com o sistema isento de cotensoativo (SME-4), quando se observou uma diferença significativa nos valores de EC50 (Tabela 3). A composição química de cada extrato e os resultados de CE50 obtidos levam a concluir que os flavonóides 3,7,4’-tri-O-metilcanferol e 3,7-di-O-metilcanferol contribuem significativamente para o potencial antioxidativo das folhas de C. cajucara.
| Árvores Jovens | CE50 (mg/mL) |
| EH-AJ-SME-4 | 446,07±52,22 |
| EH-AJ-SME-3 | 413,00±11,07 |
| EC-AJ-SME-3 | 279,96±38,26 |
| EC-AJ-SME-4 | 362,63±15,27 |
| EM-AJ-SME-1 | 275,11±25,84 |
| EM-AJ-SME-4 | 232,60±22,60 |
| Árvores Adultas | CE50 (mg/mL) |
| EM-AD-SME-1 | 348,05±3,70 |
| EM-AD-SME-4 | 321,83±22,1 |
| AJ = Árvores Jovens (1½ ano de idade); AD = árvores adultas (4-6 anos de idade); EH = extrato hexânico; EC = extrato clorofórmico; EM = extrato metanólico. |
|
Considerações Finais
Evidenciou-se no presente trabalho, que a composição química de folhas de C. cajucara é significativamente diferente da que foi observada para as cascas do caule desta espécie. O 19-nor-clerodano cajucarinolida foi a única substância comum entre estas duas partes da planta, sendo o maior rendimento deste clerodano isolado a partir das folhas (0,006%; contra 0,0003% das cascas) (MACIEL et al., 2000). Além deste clerodano, isolou-se das folhas deste Croton, uma mistura esteroidal, onde o componente majoritário foi o β-sitosterol, com rendimentos variando entre 0,01 - 0,15%, os dois flavonóides 3,7,4’-tri-O-metilcanferol (rendimento médio de 0,005%) e 3,7-di-O-metilcanferol (0,001%); além de um esteróide glicosilado, o 3-O-glicopiranosil-β-sitosterol (0,006%). Fatores sazonais não interferem nos teores de isolamento do metabólito 3,7,4’-tri-O-metilcanferol, contudo influenciam nos teores dos constituintes das misturas hidrocarbônica e esteroídica. Sistemas microemulsionados (SME) contendo como tensoativo a mistura Tween 80/ Span 20 foram obtidos para a biodisponibilização dos extratos EH, EC e EM obtidos de folhas de Croton cajucara. Estes foram solubilizados nos sistemas SME-1, SME-2 e SME-3, possibilitando a avaliação da atividade antioxidante. Os resultados obtidos mostraram que os flavonóides (3,7,4’-tri-O-metilcanferol e 3,7-di-O-metilcanferol) contribuem significativamente para o potencial antioxidativo destes extratos.
É importante enfatizar que equívocos com relação ao uso tradicional de C. cajucara (folhas são comercializadas com indicações terapêuticas de cascas) encontram-se documentados (MACIEL et al., 2002b; VEIGA Jr. et al., 2005), bem como efeitos hepatotóxicos causados pelo uso abusivo desta espécie de Croton (SOARES, 2004). No entanto, os resultados quimiofarmacológicos divulgados para esta espécie não trazem evidências cabais que comprometam seu uso medicinal (MACIEL et al., 2000; MACIEL et al., 2006b; COSTA et al., 2007; SALATINO et al., 2007). Ao contrário, doses reduzidas (25 - 50 mg) de trans-desicrocrotonina exercem controle de índices glicêmicos e reduzem índices elevados de colesterol (SILVA et al., 2001a,b,c), além de exercerem efeito cardioprotetor (SILVA et al., 2005) e outros (COSTA et al., 2007; SALATINO et al., 2007). Desta forma, o investimento em pesquisas com o Croton cajucara é promissor e deve ser aprofundado objetivando-se a consolidação da validação científica desta planta.
Dados físicos e químicos das substâncias isoladas de folhas de Croton cajucara
Mistura esteroidal (b-sitosterol e estigmasterol): sólido branco; ponto de fusão: 132-133oC. CCF: sistema de eluição: hexano-AcOEt (7:3) - Rf = 0,5; reagentes reveladores utilizados: H2SO4/ MeOH (1:1) e Sulfato Cérico. IV νmax cm-1 (KBr): 3425; 2936; 2867; 1640; 1465; 1379; 1241; 1192; 1133; 1052; 1022; 958; 838; 800. RMN de 1H, CDCl3, 300 MHz, J em Hz: 5,34 (d largo, J = 5,2); 5,14 (dd, J = 15,2; 8,4); 5,00 (dd, J = 15,2; 8,8); 3,51 (m); 0,66-2,24 (m). RMN de 13C, CDCl3, 75,4 MHz: 37,3 (C1); 31,7 (C-2); 71,8 (C-3); 42,3 (C-4); 140,8 (C-5); 121,7 (C-6); 31,9 (C-7); 31,9 (C-8); 50,2 (C-9); 36,1 (C-10); 21,1 (C-11); 39,8 (C-12); 42,3 (C-13); 56,8 (C-14); 24,3 (C-15); 28,2 (C-16); 56,1 (C-17); 11,8 (C-18 do β-sitosterol); 11,9 (C-18 do estigmasterol); 19,3 (C-19); 36,5 (C-20 do β-sitosterol); 40,5 (C-20 do estigmasterol); 18,8 (C-21 do β-sitosterol); 21,1 (C-21 do estigmasterol); 34,0 (C-22 do β-sitosterol); 138,0 (C-22 do estigmasterol); 26,2 (C-23 do β-sitosterol); 129,4 (C-23 do estigmasterol); 45,9 (C-24 do β-sitosterol); 51,2 (C-24 do estigmasterol); 29,2 (C-25 do β-sitosterol); 31,7 (C-25 do estigmasterol); 19,8 (C-26 do β-sitosterol); 21,1 (C-26 do estigmasterol); 19,0 (C-27); 23,1 (C-28 do β-sitosterol); 25,2 (C-28 do estigmasterol); 11,9 (C-29).
Flavonóide 3,7,4’-tri-O-metilcanferol: sólido amarelo cristalino; ponto de fusão: 146oC. CCF: sistema de eluição: hexano-AcOEt (7:3) - Rf = 0,5; reagentes reveladores utilizados: H2SO4/ MeOH (1:1); Sulfato Cérico e FeCl3 (presença de hidroxila fenólica). IV νmax cm-1 (KBr): 3078; 3000; 2916; 2847; 1659; 1601; 1585; 1498; 1440; 1428; 1379; 1344; 1317; 1259; 1204; 1177; 1140; 1093; 1029; 1000; 943; 830. UV λmax nm (MeOH): 273 e 349. UV λmax nm (MeOH-NaOH): 290 e 371. UV λmax nm (MeOH-NaOHHCl): 271 e 349. EM m/z (intensidade relativa %): 328 (28); 327 (29); 285 (31); 239 (13); 167 (18); 159 (22); 150 (90); 145 (29); 142 (19); 138 (16); 135 (100); 132 (23); 127 (15); 119 (50); 108 (9); 107 (23); 95 (37); 92 (44); 76 (38); 77 (75); 55 (27). RMN de 1H, CDCl3, 300 MHz, J em Hz: 6,36 (H-6, d, J = 2,2); 6,45 (H-8, d, J = 2,2); 8,10 (H-2’,6’, d, J = 9,2); 7,03 (H-3’,5’, d, J = 9,2); 3,90 ( 3 x OCH3, s); 12,67 (OH, s). RMN de 13C, CDCl3, 75,4 MHz: 155,8 (C-2); 138,8 (C-3); 178,7 (C-4); 162,0 (C-5); 97,7 (C-6); 165,4 (C-7); 92,1 (C-8); 156,7 (C-9); 106,0 (C-10); 122,8 (C-1’); 130,1 (C-2’,6’); 114,0 (C-3’,5’); 161,6 (C-4’); 60,0 (C-3-OMe); 55,3 (C-7OMe); 55,7 (C-4’-OMe).
Flavonóide 3,7-di-O-metilcanferol: sólido amarelo; ponto de fusão: 247oC. CCF: sistema de eluição: hexano-AcOEt (1:1) - Rf = 0,5; reagentes reveladores utilizados: H2SO4/ MeOH (1:1); Sulfato Cérico e FeCl3 (presença de hidroxila fenólica). IV νmax cm-1 (KBr): 3257; 1616; 1601; 1500; 1434; 1374; 1346; 1286; 1228; 1173; 1138; 1000; 942; 878; 825. UV λmax nm (MeOH): 273 e 353. UV λmax nm (MeOH-NaOH): 277 e 396. UV λmax nm (MeOHAlCl3): 277; 392; 360; 308. RMN de 1H, CDCl3, 300 MHz, J em Hz: 5,55 (H-6, d, J = 2,2); 5,89 (H-8, d, J = 2,2); 7,28 (H-2’,6’, d, J = 9,0); 6,25 (H-3’,5’, d, J = 9,0); 3,15 (H-7-OMe, s); 3,11 (H-3’-OMe); 11,99 (OH-5, s). RMN de 13C, CDCl3, 75,4 MHz: 179,6 (C-4); 161,0 (C-5); 98,4 (C-6); 166,6 (C-7); 92,8 (C-8); 157,7 (C-9); 131,2 (C-2’,6’); 116,4 (C-3’,5’); 161,0 (C-4’); 56,4 (C-7-OMe); 60,2 (C-3’-OMe).
Clerodano cajucarinolida: sólido amorfo; ponto de fusão: 202-204oC. CCF: sistema de eluição: CH Cl -AcOEt-MeOH (7,2: 2,6: 0,2) - Rf = 0,5; reagentes reveladores utilizados: Sulfato Cérico; Dragendorff (presença de carbonila α,β-insaturada e/ou lactona). IV νmax cm-1 (KBr): 3273; 2978; 1752; 1662; 1617; 1477; 1454; 1330; 1283; 1216; 1185; 1159; 1139; 1110; 1051; 1005; 879. UV λmax nm (MeOH): 218 e 245. RMN de 1H, CDCl : CD OD (4:1), 300 MHz, J em Hz: 2,07 (H-1α, t, J = 14,7); 2,49 (H-1β, d largo); 5,92 (H-3, s largo); 3,07 (H-5, t largo, J = 11,6); 2,25 (H-6α, dq, J = 12,6; 3,5); 1,23-1,15 (H-6β); 1,85 (H7α); 1,70-1,65 (H-7β); 1,70-1,65 (H-8); 1,82 (H-10), 2,24 (H-11A); 2,66 (H-11B, dd, J = 14,7; 9,8); 5,28 (H-12, t largo, J = 8,0); 7,11 (H-14, t, J = 1,5); 6,17 (H-15, s largo); 1,10 (H 17, d, J = 6,5); 1,98 (H-18, d, J = 1,2). RMN de 13C, CDCl3: CD3OD (4:1), 75,4 MHz: 40,1 (C-1); 196,7 (C-2); 127,0 (C3); 165,9 (C-4); 40,3 (C-5); 28,5 (C-6); 30,4 (C-7); 41,7 (C8); 51,5 (C-9); 46,4 (C-10); 39,0 (C-11); 72,1 (C-12); 136,9 (C-13); 144,0 (C-14); 98,6 (C-15); 169,5 (C-16); 17,8 (C-17); 22,6 (C-18); 177,2 (C-20).
Esteróide 3-O-glicopiranosil-β-sitosterol: sólido branco; ponto de fusão: 240oC. CCF: sistema de eluição: AcOEt-MeOH (9:1) - Rf = 0,4; reagente revelador utilizado: H2SO4/ MeOH (1:1). IV νmax cm-1 (KBr): 3415; 2934; 1637; 1462; 1372; 1256; 1166; 1107; 1073; 1022; 957; 886; 800.
RMN de 1H, CDCl3-CD3OD (2:1), 300 MHz, J em Hz: 5,21 (H-6, d largo, J = 5,2); 3,99 (H-3, m); 0,48-2,28 (hidrogênios metílicos e metilênicos). Subunidade Glicose: 4,25 (H-1’, d, J = 7,7); 3,08 (H-2’, m); 3,27 (H-3’, dd, J = 6,8; 2,5); 3,43 (H-4’, m); 3,14 (H-5’, m); 3,59 (H-6’a, dd, J = 12,0; 4,5); 3,69 (H-6’b, dd, J = 12,0; 3,0). RMN de 13C, CDCl3-CD3OD (2:1), 75,4 MHz: 37,0 (C-1); 31,6 (C-2); 78,9 (C-3); 42,0 (C-4); 140,1 (C-5); 121,8 (C-6); 31,6 (C-7); 31,6 (C-8); 50,0 (C-9); 36,4 (C10); 20,8 (C-11); 39,5 (C-12); 42,0 (C-13); 56,5 (C-14); 24,0 (C-15); 28,9 (C-16); 55,8 (C-17); 11,5 (C-18); 19,4 (C-19); 35,8 (C-20); 18,6 (C-21); 33,7 (C-22); 25,9 (C-23); 45,6 (C-24); 29,3 (C-25); 20,8 (C-26); 18,9 (C-27); 22,8 (C-28); 11,6 (C-29). Subunidade Glicose: 100,8 (C-1’); 73,3 (C-2’); 76,2 (C-3’); 69,9 (C-4’); 75,6 (C-5’); 61,5 (C-6’). RMN de 13C, DMSO-d6, 75,4 MHz: 36,8 (C-1); 31,4 (C-2); 77,0 (C-3); 41,9 (C-4); 140,5 (C5); 121,2 (C-6); 33,4 (C-7); 33,4 (C-8); 49,6 (C-9); 36,2 (C-10); 20,6 (C-11); 38,3 (C-12); 41,9 (C-13); 56,2 (C-14); 25,5 (C-15); 28,8 (C-16); 55,5 (C-17); 11,8 (C-18); 19,1 (C-19); 36,8 (C-20); 18,6 (C-21); 35,5 (C-22); 27,8 (C-23); 45,2 (C-24); 29,3 (C-25); 19,7 (C-26); 18,9 (C-27); 23,8 (C-28); 11,7 (C-29). Subunidade Glicose: 100,8 (C-1’); 73,5 (C-2’); 76,8 (C-3’); 70,2 (C-4’); 76,7 (C-5’); 61,2 (C-6’).
Agradecimentos
Os autores agradecem aos Programas PRODOC/CAPES e PDS-CNPq, bem como a FAPERJ.
Referências
AGNER, A.R.; MACIEL, M.A.M.; PINTO, A.C.; PAMPLONA, S.G.S.R.; CÓLUS, I.M.S. Investigation of genotoxic activity of trans-dehydrocrotonin, a clerodane diterpene from Croton cajucara. Teratogen Carcinogen Mutagen, v.19, p.377-384, 1999.
AGNER, A.R.; MACIEL, M.A.M.; PINTO, A.C.; CÓLUS, I.M.S. Antigenotoxicity of trans-dehydrocrotonin, a clerodane diterpene from Croton cajucara. Planta Medica, v.67, p.815-819, 2001.
ALVIANO, W.S.; MENDONÇA-FILHO, R.R.; ALVIANO, D.S.; BIZZO, H.R.; SOUTO-PADRÓN, T.; RODRIGUES, M.L.; BOLOGNESE, A.M.; ALVIANO, C.S.; SOUZA, M.M.G. Antimicrobial activity of Croton cajucara Benth linalool-rich essential oil on artificial biofilms and planktonic microorganisms. Oral Microbiology and Immunology, v.20, p.101-105, 2005.
ARAÚJO, V.C.; CORRÊA, G.C.; MAIA, J.G.S.; SILVA, M.L.; GOTTLIEB, O.R.; MARX, M.C.; MAGALHÃES, M.T. Óleos essenciais da Amazônia contendo linalol. Acta Amazônica, v.1, p.45-47, 1971.
AZEVEDO, C.H.M.; CARVALHO, J.P.; VALDUGA, C.J.; MARANHÃO, R.C. Plasma kinetics and uptake by tumor of a cholesterol-rich microemulsion (LDE) associated to etoposide oleate in patients with ovarian carcinoma. Gynecologic Oncology, v.97, p.178-182, 2005.
BERKLAND, C.; KING, M.; COX, A.; KIM, K.K.; PACK, D.W. Precise control of PLG microsphere size provides enhanced control of drug release rate. Journal of Controlled Release, v.82, p.137-147, 2002.
BILIA, A.R.; MENDEZ, J.; MORELLI, I. Phytochemical investigations of the Licania genus.1Flavonoids and triterpenoids from Licinia carii. Pharmaceutica Acta Helvetiae, v.71, p.191-197, 1996.
CAMPOS, A.R.; ALBUQUERQUE, F.A.A.; RAO, V.S.N; MACIEL, M.A.M.; PINTO, A.C. Investigations on the antinociceptive activity of crude extracts from Croton cajucara leaves in mice. Fitoterapia, v.73, p.116-120, 2002.
COSTA, M.P.; SANTOS MAGALHÃES, N.S.; GOMES, F.E.S.; MACIEL, M.A.M. Uma revisão das atividades biológicas da trans-desidrocrotonina, um produto natural obtido de Croton cajucara. Revista Brasileira de Farmacognosia, v.17, p.275-286, 2007.
DALMORA, M.E.; DALMORA, S.L.; OLIVEIRA, A.G. Inclusion complex of piroxicam with β-cyclodextrin and incorporation in cationic microemulsion. In vitro drug release and in vivo topical anti-inflammatory effect. International Journal of Pharmaceutics, v.222, p.45-55, 2001.
DREYER, D.L. Kaempferol methyl ethers from flowers of Dodonaea viscosa. Revista Latinoamericana de Química, v.9, p.97-98, 1978.
FARIAS, R.A.F.; NETO, M.F.O.; VIANA, G.S.B.; RAO, V.S.N. Effects of Croton cajucara extract on serum lipids of rats fed a high fat diet. Phytotherapy Research, v.10, p.697-699, 196.
FARIAS, R.A.F.; RAO, V.S.N.; VIANA, G.S.B.; SILVEIRA, E.R.; MACIEL, M.A.M.; PINTO, A.C. Hypoglycemic effect of trans-dehydrocrotonin, a nor-clerodane diterpene from Croton cajucara. Planta Medica, v.63, p.558-560, 1997.
FARIAS, R.A.F.; GONZÁLEZ, R.P.; LEYVA, A.; MAIA, L.S.; MACIEL, M.A.M.; PINTO, A.C.; VEIGA JR., V.F.; PESSOA, C.; MORAES, M.O. Chromatographic fractions from Croton cajucara inhibit cell proliferation and induce differation in a human leukemia cell line. Journal of Cancer Integrative Medicine, v.3, p.75-80, 2005.
FENG, S.S.; RUAN, G.; LI, Q.T. Fabrication and characterizations of a novel drug delivery device liposomes-in-microsphere (LIM). Biomaterials, v.25, p.5181-5189, 2004.
FLORENCE, A.T. Nanoparticle uptake by the oral route: Fulfilling its potential? Drug Discovery Today, v.2, p.75-81, 2005.
FORMARIZ, T.P.; URBAN, M.C.C.; SILVA JR., A.A.; GREMIÃO, M.P.D.; OLIVEIRA, A.G. Microemulsões e fases líquidas cristalinas como sistemas de liberação de fármacos. Revista Brasileira de Ciências Farmacêuticas, v.41, p.301-313, 2005.
GOMES, F.E.S.; ANJOS, G.C.; DANTAS, T.N.C.; MACIEL, M.A.M.; ESTEVES, A.; ECHEVARRIA, A. Obtenção de nanoformulações do tipo microemulsão objetivando a biodisponibilização de Anacardium occidentale e sua eficiência como agente antioxidante. Revista Fitos, v.2, p.82-88, 2006.
GUPTE, A. ; CIFTCI, K. Formulation and characterization of Paclitaxel, 5-FU and Paclitaxel + 5-FU microspheres. International Journal Pharmaceutics, v.276, p.93-106, 2004.
HIRUMA-LIMA, C.A.; GRACIOSO, J.S.; NUNES, D.S.; SOUZA-BRITO, A.R.M. Effects of an essential oil from the bark of Croton cajucara Benth. on experimental gastric ulcer models in rats and mice. Journal of Pharmacy and Pharmacology, v.51, p.341-346, 1999.
HIRUMA-LIMA, C.A.; GRACIOSO, J. S.; BIGHETTI, E. J. B.; GRASSI-KASSISSE, D.M.; NUNES, D. S.; SOUZA-BRITO, A.R.M. Effect of essential oil obtained from Croton cajucara Benth. on gastric ulcer healing and protective factors of the gastric mucosa. Phytomedicine, v.9, p.523-529, 2002.
ICHIHARA, Y.; TAKEYA, K.; HITOTSUYANAGI , Y.; MORITA, H.; OKUYAMA, S.; SUGANUMA, M.; FUJIKI, H.; MOTIDOME, M.; ITOKAWA, H. Cajucarinolide and isocajucarinolide: antiinflammatory diterpenes from Croton cajucara. Planta Medica, v.58, p.549-551, 1992.
KAWAKAMI, K.; YOSHIKAWA, T.; MOROTO, Y.; KANAOKA, E.; TAKAHASHI, K.; NISHIHARA, Y.; MASUDA, K. Microemulsion formulation for enhanced absorption of poorly soluble drugs. I. Prescription design, Journal of Controlled Release, v.81, p.65-74, 2002.
KHAN, M.T.H.; ATHER, A.; PINTO, A.C.; MACIEL, M..A.M. Potential benefits of the 19-nor-clerodane trans-dehydrocrotonin on the central nervous system. Revista Brasileira de Farmacognosia, v.19(1A), p.7-13, 2009.
LAWRENCE, M.J.; REES, G.D. Microemulsion-based media as novel drug delivery systems. Advanced Drug Delivery Reviews, v.45, p.89-121, 2000.
LEE, P.J.; LANGER, R.; SHASTRI, V.P. Novel microemulsion enhancer formulation for simultaneous transdermal delivery of hydrophilic and hydrophobic drugs. Pharmaceutical Research, v.20, p.7-27, 2003.
LEMOS, T.L.G.; MACHADO, M.I.L.; DE MENEZES, J.E.S.A.; DE SOUSA, C.R. Essential oil of Croton cajucara Benth. Journal of Essential Oil Research, v.11, p.411-412, 1999.
LOPES, D.; BIZZO, H.R.; SÁ SOBRINHO, A.F.; PEREIRA, M.V.G. Linalool-rich essential oil from leaves of Croton cajucara Benth. Journal of Essential Oil Research, v.12, p.705-708, 2000.
LYONS, K.C.; CHARMAN, W.N.; MILLER, R.; PORTER, C.J.H. Factors limiting the oral bioavailability of N-acetylglucosaminyl-N-acetylmuramyl dipeptide (GMDP) and enhancement of absorption in rats by delivery in a water-in-oil microemulsion, International Journal of Pharmaceutics, v.199, p.17-28, 2000.
MACIEL, M.A.M.; PINTO, A.C.; BRABO, S.N.; SILVA, M.N. Terpenoids from Croton cajucara. Phytochemistry, v.49, p.823-828, 1998a.
MACIEL, M.A.M.; PINTO, A.C.; BRADO, S.N.; ARRUDA, A.C. Estudo da variação dos teores de terpenóides bioativos isolados das cascas do caule de Croton cajucara, nativos e cultivados no estado do Pará. Revista Universidade Rural, Série Ciências Exatas e da Terra, v.18/20, p.17-34, 1998b.
MACIEL, M.A.M.; PINTO, A.C.; ARRUDA, A.C.; PAMPLONA, S.G.S.R.; VANDERLINDE, F.A.; LAPA, A.J.; ECHEVARRIA, A.; GRYNBERG, N.F.; CÓLUS, I.M.S.; FARIAS, R.A.F.; COSTA, A.M.L.; RAO, V.S.N. Ethnopharmacology, phytochesmistry and pharmacology: a successful combination in the study of Croton cajucara. Journal of Ethnopharmacology, v.70, p.41-55, 2000.
MACIEL, M.A.M.; PINTO, A.C.; VEIGA JR, V.F., MARTINS, J.R.; GRYNBERG, N.F.; ECHEVARRIA, A.; LAPA, A.J.; VANDERLINDE, F.A. Croton cajucara as an alternative to traditional medicine in a modern health system. In: Phytochem. Pharmacol. II Serie Recent Progress in Mededicinal Plants, v.8, p.459-475, 2002a.
MACIEL, M.A.M.; PINTO, A.C.; VEIGA JR, V.F. Plantas Medicinais: a necessidade de estudos multidiscilplinares. Química Nova, v.25, p.429-438, 2002b.
MACIEL, M.A.M.; DANTAS, T.N.C.; CÂMARA, J.K.P.; PINTO, A.C.; VEIGA JR., V.F.; KAISER, C.R.; PEREIRA, N.A.; CARNEIRO, C.M.T.S.; VANDERLINDE, F.A.; LAPA, A.J.; AGNER, A.R.; CÓLLUS, I.M.S.; ECHEVARRIA-LIMA, J.; GRYNBERG, N.F.; ESTEVES-SOUZA, A.; PISSINATE, K.; ECHEVARRIA, A. Pharmacological and biochemical profiling of lead compounds from traditional remedies: the case of Croton cajucara. In: Advances in Phytomedicine (Lead molecules from natural products, Discovery and New Trends), Eds. Khan, M.T.H.; Ather, A., v.2, Ch. 14, p.229-257, 2006a.
MACIEL, M.A.M.; CORTEZ, J.K.P.C.; GOMES, F.E.S. O gênero Croton e aspectos relevantes de diterpenos clerodanos. Revista Fitos, v.2, p.54-73, 2006b.
MACIEL, M.A.M.; MARTINS, J.R.; PINTO, A.C.; KAISER, C.R.; ESTEVES-SOUZA, A.; ECHEVARRIA, A. Natural and semisynthetic clerodanes of Croton cajucara and their cytotoxic effects against Ehrlich carcinoma and human k562 leukemia cells. Journal of the Brazilian Chemical Society, v.18, p.391-396, 2007.
MARKHAM, K.R.; MABRY, T. Ultraviolet-visible and proton magnetic resonance spectroscopy of flavonoids, In: Harborne JB, Mabry TJ and Mabry H (eds.) The Flavonoids. New York: Academic Press, Part 1, p.45, 1975.
MARKHAM, K.R. Techniques of flavonoid identification, London: Academic Press, p.38-113, 1982.
MENSOR, L.L.; MENEZES, F.S.; LEITÃO, G.G.; REIS, A.S.; SANTOS, T.C.; COUBE, C.S.; LEITÃO, S.G. Screening of Brazilian plant extracts for antioxidant activity by the use of DPPH free radical method. Phytoterapy Research, v.15, p.127-130, 2001.
OLIVEIRA, A.G.; SCARPA, M.V.; CORREA, M.A.; CERA, L.F.R.; FORMARIZ, T.P. Microemulsões: estrutura e aplicações como sistema de liberação de fármacos. Química Nova, v.27, p.131-138, 2004.
PERAZZO, F.F.; CARVALHO, J.C.T.; RODRIGUES, M.; MORAIS, E.K.L.; MACIEL, M.A.M. Comparative anti-inflammatory and antinociceptive effects of terpenoids and an aqueous extract obtained from Croton cajucara Benth. Revista Brasileira de Farmacognosia, v.17, p.521-528, 2007.
PERES, M.T.; MONACHE, F.D.; CRUZ, A.B.; PIZZOLATTI, M.G.; YUNES, R.A. Chemical composition and antimicrobial activity of Croton urucurana Baillon. Journal of Ethnopharmacology, v.56, p.223-226, 1997.
RATNER, B.D. Reducing capsular thickness and enhancing angiogenesis around implant drug release systems. Journal Controlled Release, v.78, p.211-218, 2002.
RIBEIRO-COSTA, R.M.; ALVES, A.J.; SANTOS, N.P.; NASCIMENTO, S.C.; GONÇALVES, E.C.P.; SILVA, N.H.; HONDA, N.K.; SANTOS-MAGALHÃES, N.S. In vitro and in vivo properties of usnic acid encapsulated into PLGA-microspheres. Journal of Microencapsulation, v.21, p.371-384, 2004.
RODRÍGUEZ, J.A.; HIRUMA-LIMA, C.A.; SOUZA-BRITO, A.R.M. Antiulcer activity and subacute toxicity of transdehydrocrotonin from Croton cajucara. Human and Experimental Toxicology, v.23, p.455-461, 2004.
ROSA, M.D.S.; MENDONCA, R.R.; BIZZO, H.R.; RODRIGUES, I.D.; SOARES, R.M.A.; SOUTO-PADRON, T.; ALVIANO, C.S.; LOPES, A.H.C.S. Antileishmanial activity of a linalool-rich essential oil from Croton cajucara. Antimicrob Agents Chemother, v.47, p.1895-1901, 2003.
ROSSI, C.G.F.T.; DANTAS, T.N.C.; NETO, A.A.D.; MACIEL, M.A.M. Microemulsões: uma abordagem básica e perspectivas para aplicabilidade industrial. Revista da Universidade Rural, Série Ciências Exatas e da Terra, v.26, n.1/2, p.45-66, 2007.
SALATINO, A.; SALATINO, M.L.F.; NEGRI, G. Traditional uses, chemistry and pharmacology of Croton species (Euphorbiaceae). Journal of the Brazilian Chemical Society, v.18, p.11-33, 20SANTOS, F.V.; MESQUITA, S.F.P.; FARIA, M.J.S.S.; POERSH, A.; MACIEL, M.A.M.; PINTO, A.C.; MORIMOTO, H.K.; CÓLUS, I.M.S. Absence of mutagenicity in somatic and germ cells of mice submitted to subchronic treatment with an extract of Croton cajucara Benth. (Euphorbiacae). Genetic and Molecular Biology, v.29, p.159-165, 2006.
SILVA, R.M.; SANTOS, F.A.; RAO, V.S.N.; MACIEL, M.A.M.; PINTO, A.C. Blood glucoseand triglyceride-lowering effect of trans-dehydrocrotonin, a diterpene from Croton cajucara Benth., in rats. Diabetes, Obesity and Metabolism, v.3, p.452-456, 2001a.
SILVA, R.M.; SANTOS, F.A.; MACIEL, M.A.M.; PINTO, A.C.; RAO, V.S.N. Effect of trans-dehydrocrotonin, a 19-nor-clerodane diterpene from Croton cajucara on experimental hypertriglyceridaemia and hypercholesterolaemis induced by Triton WR 1339 (tyloxapol) in mice. Planta Medica, v.67, p.763-765, 2001b.
SILVA, R.M.; SANTOS, F.A.; RAO, V.S.N.; MACIEL, M.A.M.; PINTO, A.C. The lipid-lowering effect of trans-dehydrocrotonin from Croton cajucara Benth. in mice fed on high-fat diet. Journal of Pharmacy and Pharmacology, v.53, p.535-539, 2001c.
SILVA, R.M.; OLIVEIRA, F.A.; CUNHA, K.M.A.; MAIA, J.L.; MACIEL, M.A.M.; PINTO, A.C.; NASCIMENTO, N.R.F.; SANTOS, F.A.; RAO, V.S.N. Cardiovascular effects of trans-dehydrocrotonin, a diterpene from Croton cajucara. Vascular Pharmacology, v.43, p.11-18, 2005.
SOARES, M.C.P. Would Sacaca, Croton cajucara Benth (Euphorbiaceae) be an hepatotoxic plant like Germander, Teucrium chamaedrys L. (Labiatae)? Revista da Sociedade Brasileira de Medicina Tropical, v.37, p.96-97, 2004.
SOUZA-BRITO, A.R.M.; RODRÍGUEZ, J.A.; HIRUMA-LIMA, C.A.; HAUN, M.; NUNES, D.C. Antiulcerogenic activity of trans-dehydrocrotonin from Croton cajucara. Planta Medica, v.64, p.126-129, 1998.
SOUZA, M.A.A.; SOUZA, S.R.; VEIGA JR., V.F.; CORTEZ, J.K.P.C.; LEAL, R.S.; DANTAS, T.N.C.; MACIEL, M.A.M. Composição química do óleo fixo de Croton cajucara e determinação das suas propriedades fungicidas. Revista Brasileira de Farmacognosia, v.16 (supl.), p.599-610, 2006.
VALESI, A.G.; RODRIGUEZ, E.; VANDER-VELDER, G.; MABRY, T.J. Methylated flavonols in Larrea cuneifolia. Phytochemistry, v.11, p.2821-2826, 1972.
VEIGA JR., V.F.; PINTO, A.C.; MACIEL, M.A.M. Plantas medicinais: cura segura? Química Nova, v.28, p.519-528, 2005.